
 研發(fā)追蹤
研發(fā)追蹤
 2015-04-03
2015-04-03
 4171
4171
來源:新康界/金伊??? 2015年04月03日
2015年03月份美國FDA共審批通過8種新藥蝶押,1類新分子實(shí)體藥物2個余二;新生物藥物2個应结;3類新劑型藥物1個;夏跷;5類新規(guī)格或新生廠商藥物2個击困;新生物仿制藥1個久耍。
2015年03月份美國FDA審批通過新藥
2015年3月美國FDA審批通過一個新分子實(shí)體藥物粹龄,為日本第一三共公司研發(fā)的抗凝血新分子實(shí)體藥物Savaysa(Edoxaban);審批通過二個新生物藥物洪业,為諾華公司研發(fā)的銀屑病新生物藥Cosentyx(Secukinumab)和NPS 制藥研發(fā)的甲狀旁腺機(jī)能減退新生物藥 Natpara(重組人甲狀旁腺激素)撼遵。同時還有一個有意義的審批藥物是AbbVie公司研發(fā)的3類新劑型藥物Duopa,用于帕金森病的治療峭桅。Duopa是卡比多巴/左旋多巴組成的混懸液甜杰,給藥時需要利用CADD-Legacy? 1400 泵將藥物直接輸注進(jìn)小腸柑爸,從而避免胃酸對藥物的降解。
表12015年03月份美國FDA審批通過新藥
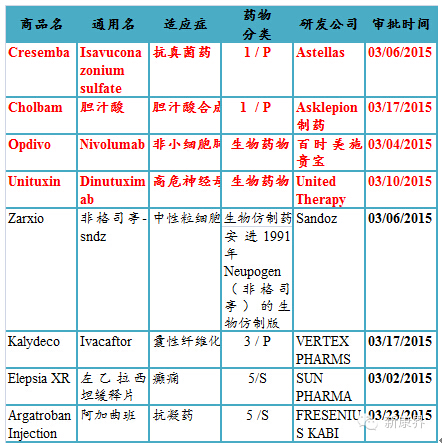
注:1)化學(xué)新藥分類:1類新分子實(shí)體化合物盒音;3類新劑型竖配; 5類藥物新 規(guī)格或新生產(chǎn)商;
2)審批分類:P優(yōu)先評審里逆;S常規(guī)評審
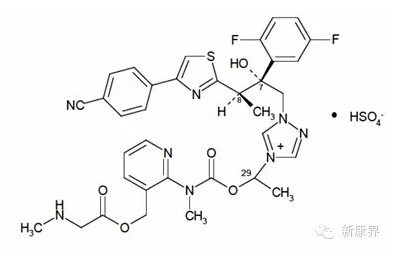
(一)抗真菌新分子實(shí)體藥物Cresemba(Isavuconazonium sulfate)
2015年03月06日,美國FDA優(yōu)先審批批準(zhǔn)Astellas公司研發(fā)的抗真菌新分子實(shí)體藥物Cresemba(Isavuconazonium sulfate/艾沙康唑硫酸鹽)上市用爪,用于治療侵入性曲霉病和毛霉菌病原押。Cresemba(艾沙康唑硫酸鹽)是艾沙康唑的前提藥物,進(jìn)入體內(nèi)后代謝為艾沙康唑進(jìn)而發(fā)揮抗真菌的作用偎血。Cresemba共有口服和注射兩種劑型诸衔,Cresemba口服膠囊含有186mg艾沙康唑硫酸鹽, Cresemba注射劑含有372mg艾沙康唑硫酸鹽。

(二)膽汁酸合成障礙新分子實(shí)體藥物Cholbam
2015年031月17日颇玷,美國FDA批準(zhǔn)Asklepion制藥公司研發(fā)的膽汁酸合成障礙新分子實(shí)體藥物Cholbam上市笨农。Cholbam是一種膽汁酸,用于治療因單一酶缺乏而導(dǎo)致膽汁酸合成障礙的兒科及成年患者及用于過氧化物酶體蔡(包括齊薇格譜系障礙)谒亦。患有這些罕見疾病的患者體內(nèi)缺乏用來合成膽酸的酶旬效,膽酸的缺乏導(dǎo)致膽汁流量減少炬费,從而致使有毒的膽汁酸中間體潛在積聚于肝臟內(nèi)(膽汁阻塞)及對飲食中的脂肪和脂溶性維生素吸收不良。如果不進(jìn)行治療讯匈,患者將不能生長艾蜓,并會發(fā)生危及生命的肝損傷。Cholbam為口服膠囊劑型策坏,共有50mg和250mg兩種規(guī)格零反。
(三)非小細(xì)胞肺癌新生物藥 Opdivo (Nivolumab)
2015年03月04日,美國FDA批準(zhǔn)百時美施貴寶研發(fā)的新生物藥Opdivo(Nivolumab)用于治療化療后仍惡化的轉(zhuǎn)移性鱗狀非小細(xì)胞肺癌的治療烈肉。Opdivo(Nivolumab) 為人源化單克隆抗體迫讨,是PD-1(programmed death 1,程序性死亡-1受體) 抑制劑類藥物辙哪,最早于2014年12月03日通過美國FDA審批用于的黑色素瘤的治療垦祭。
(四)高危神經(jīng)母細(xì)胞瘤新生物藥Unituxin (Dinutuximab)
2015年03月10日,美國FDA批準(zhǔn)United Therapy公司研發(fā)的高危神經(jīng)母細(xì)胞瘤新生物藥Unituxin (Dinutuximab)上市沽澜。神經(jīng)母細(xì)胞瘤是一種罕見的癌癥籍胯,它形成于不成熟的神經(jīng)細(xì)胞。這種疾病通常起始于腎上腺离福,但還可能在腹部杖狼、胸部或脊柱附近的神經(jīng)組織發(fā)展炼蛤。神經(jīng)母細(xì)胞瘤通常發(fā)生在五歲以下的兒童身上。Unituxin (Dinutuximab)是一種GD2-結(jié)合單克隆抗體蝶涩,臨床上與粒細(xì)胞-巨噬細(xì)胞集落刺激因子(GM-CSF)理朋、白介素-2(IL-2)、13-順-視黃酸(RA)聯(lián)用绿聘。Unituxin (Dinutuximab)被批準(zhǔn)用作綜合治療方案的一部分嗽上,包括手術(shù)、化療及放射治療熄攘,適用于對之前一線多種藥物兽愤、綜合治療至少達(dá)到部分響應(yīng)的患者。
附:美國FDA審批新藥說明
美國FDA審批新藥主要是根據(jù)藥物化學(xué)類型和治療潛能來進(jìn)行分類的挪圾。新藥按化學(xué)類型主要分為:1類新分子實(shí)體化合物(NME)浅萧,創(chuàng)新性最強(qiáng)。指在美國從未作為藥品批準(zhǔn)或銷售的活性成分哲思,可以是單一成分版挣,也可以是立體異構(gòu)混合物中的一部分;2類新的衍生物柴羞。從已上市的活性成分(即所謂“專利”藥)化學(xué)衍生而來婆裹,即已在美國上市的活性成分的酯、鹽或其它非共價鍵衍生物,或者是去修飾基團(tuán)的母體化合物未在美國批準(zhǔn)上市的稳嘁;3類新劑型纫脚。含有已上市活性成分的新劑型或新處方,其適應(yīng)癥可以與上市產(chǎn)品相同眶逐,也可以不同况颈;4類新組合物。含有兩種或兩種以上已上市的活性成分的品種洗吉,上市產(chǎn)品中尚無這種組合勾奇;5類藥物新規(guī)格或新生產(chǎn)商;6類新適應(yīng)癥蔼魁。由同一家公司或其他公司在美國批準(zhǔn)或上市的具有新用途的復(fù)制品摆野;7類已上市但未經(jīng)NDA批準(zhǔn)的藥品。適應(yīng)癥已與上市產(chǎn)品相同凛驮,也可不同裆站;8類變?yōu)榉翘幏剿帲?/span>10類適應(yīng)癥不同的新的新藥申請。
治療潛能類分P類和S類兩種黔夭,是相互獨(dú)立的兩類宏胯,即所有的分類中只能包含其中的一個字母。P類:優(yōu)先評審,治療上有突破肩袍。指1)能有效地治療或診斷某種疾病杭棵,而任何上市產(chǎn)品能給予這種病適當(dāng)?shù)闹委熀驮\斷;或2)較上市產(chǎn)品更有效氛赐、更安全地改善某種疾病的治療魂爪;3)具有適中的、客觀的超過上市藥品的優(yōu)越性艰管。如①明顯給病人帶來較大方便(如減少給藥次數(shù))滓侍,②消除干擾、必要的危險和副作用牲芋,③對特定的人群組疾病有效(如老年和兒童病人粗井,或?qū)σ延眠^的藥不能耐受的)等。S類:常規(guī)評審钢谍。治療效果類似已上市的產(chǎn)品。
?

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 214
214

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方Info
醫(yī)藥魔方Info  2024-11-25
2024-11-25
 216
216

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 222
222
 熱門資訊
熱門資訊