
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥智網(wǎng)
藥智網(wǎng)  2019-07-09
2019-07-09
 4129
4129
7月1日倡怎,國家衛(wèi)健委和國家中醫(yī)藥管理局公布了《第一批國家重點(diǎn)監(jiān)控合理用藥藥品目錄(化藥及生物制品)》(以下簡稱“第一批國家重點(diǎn)監(jiān)控藥品目錄”或“目錄”)炼缰。這讓業(yè)內(nèi)長期眾所紛紜的“國輔目錄”有了個(gè)結(jié)果膳沽。同時(shí)酬苇,多家醫(yī)藥媒體從具體產(chǎn)品銷售額葡缰、市場份額遏插、相關(guān)企業(yè)等方面對“第一批國家重點(diǎn)監(jiān)控藥品目錄”進(jìn)行解讀...
7月1日验残,國家衛(wèi)健委和國家中醫(yī)藥管理局公布了《第一批國家重點(diǎn)監(jiān)控合理用藥藥品目錄(化藥及生物制品)》(以下簡稱“第一批國家重點(diǎn)監(jiān)控藥品目錄”或“目錄”)捞附。這讓業(yè)內(nèi)長期眾所紛紜的“國輔目錄”有了個(gè)結(jié)果。同時(shí)您没,多家醫(yī)藥媒體從具體產(chǎn)品銷售額鸟召、市場份額、相關(guān)企業(yè)等方面對“第一批國家重點(diǎn)監(jiān)控藥品目錄”進(jìn)行解讀氨鹏。而觀點(diǎn)主要集中在這幾項(xiàng):涉及“第一批國家重點(diǎn)監(jiān)控藥品目錄”的產(chǎn)品銷量及企業(yè)業(yè)績在未來會(huì)受到?jīng)_擊欧募;醫(yī)保受限、臨床使用監(jiān)管趨嚴(yán)仆抵;后續(xù)還會(huì)有更多“國家重點(diǎn)監(jiān)控藥品目錄”出臺槽片。
鑒于此,筆者今日想說的是肢础,本次入圍“第一批國家重點(diǎn)監(jiān)控藥品目錄”有20個(gè)品種还栓,據(jù)公開數(shù)據(jù)顯示,其2018年銷售額總計(jì)達(dá)600多億元埂体,產(chǎn)品(奧拉西坦)年銷售額最高近67億氓暖。也就是說,這20個(gè)產(chǎn)品在《第一批國家重點(diǎn)監(jiān)控合理用藥藥品目錄(化藥及生物制品)》洛续、《關(guān)于控制公立醫(yī)院醫(yī)療費(fèi)用不合理增長的若干意見》(國衛(wèi)體改發(fā)(2015)89號)账姜、《合理醫(yī)療用藥范圍管理辦法》等政策出臺之前,就已賺的盆滿缽滿绞宿。尤其是在國家強(qiáng)調(diào)“輔助用藥臨床應(yīng)用管理規(guī)定”的這幾年插涛,銷量雖有下滑的傾向,但仍為億級大品種鞋伸。在市銷售的20個(gè)品種叉弱,其銷售額或斷崖式下跌,實(shí)屬“命運(yùn)使然”艰欲,相關(guān)企業(yè)或早已作出了預(yù)判庐冤,并備有應(yīng)對之策。但目前處于“報(bào)生產(chǎn)”的“重點(diǎn)監(jiān)控”類品種是否會(huì)走向“出師未捷身先死”的結(jié)局呢?
多個(gè)億級藥品還沒出場泡徙,或遭遇“落幕”
據(jù)藥智“藥品注冊與受理”數(shù)據(jù)庫統(tǒng)計(jì)橱鹏,目前國內(nèi)有多家藥企對上述20個(gè)品種進(jìn)行“報(bào)生產(chǎn)”的申請,受理號總計(jì)超1000個(gè)堪藐,其包括“退審”莉兰、“不批準(zhǔn)”、“在審評審批中”礁竞、“制證完畢”糖荒、“不批準(zhǔn)”等辦理狀態(tài)。涉及的具體數(shù)據(jù)且不深究苏章,1000多個(gè)受理號中“未出場”的產(chǎn)品背后是大批企業(yè)的巨額成本。按著“第一批國家重點(diǎn)監(jiān)控藥品目錄”的邏輯奏瞬,只要是入圍的產(chǎn)品枫绅,其臨床使用、醫(yī)保限制等方面均會(huì)受到嚴(yán)重影響硼端。由此并淋,針對那些尚未“出世”的產(chǎn)品或提前“夭折”,而企業(yè)投進(jìn)去的成本也將覆水難收珍昨。
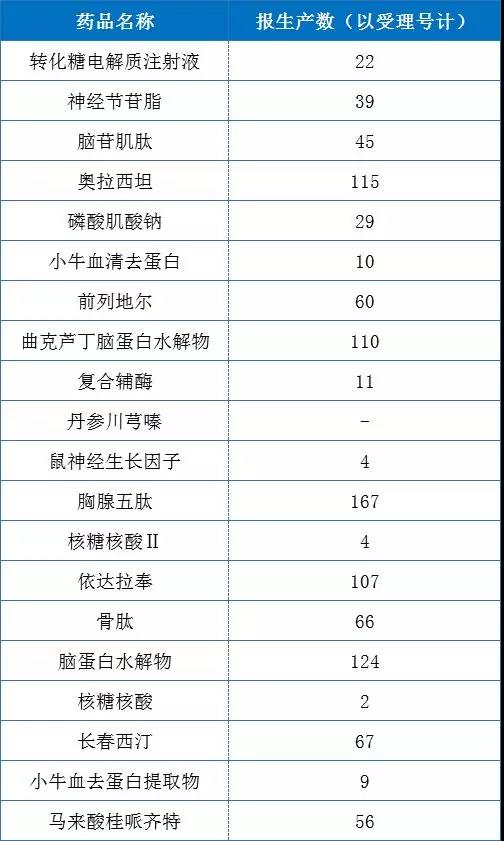
這種“不計(jì)成本”县耽、非科學(xué)立項(xiàng)式的仿制藥產(chǎn)品的扎堆申報(bào)現(xiàn)象在我國仿制藥市場長期存在,其產(chǎn)生的主要原因是我國企業(yè)對仿制藥的立項(xiàng)依據(jù)為“市場規(guī)奈史妫”徒浸。據(jù)“醫(yī)藥云端工作室”統(tǒng)計(jì),國內(nèi)目前有4300多家制劑生產(chǎn)企業(yè)描琉,擁有1.5萬個(gè)藥品躯琐,共計(jì)16.8萬個(gè)批文。能進(jìn)入醫(yī)療機(jī)構(gòu)的不到2000個(gè)穴厅,按相關(guān)管理規(guī)定囊古,一般是三級限制采1500個(gè),二級1200盹火,一級800個(gè)品規(guī)狠压,一個(gè)省其實(shí)常用藥也就是在5000個(gè)品規(guī)左右,銷量排在前10%的品種基本上能夠占據(jù)80%左右的銷售金額哗衫。簡言之相品,能真正進(jìn)入醫(yī)療機(jī)構(gòu),成為銷售“大品種”的機(jī)會(huì)并不多示婉。
再以目前過一致性評價(jià)的幾個(gè)典型產(chǎn)品為例征炼,苯磺酸氨氯地平作為289目錄產(chǎn)品,2016年以前有73個(gè)生產(chǎn)批文,共有29個(gè)受理號申報(bào)一致性評價(jià)谆奥。2016年以后苯磺酸氨氯地平只有獲批一個(gè)產(chǎn)品眼坏,是重慶藥友以舊6類申報(bào)的,暫無新4類廠家獲批酸些。截止至2019年6月宰译,苯磺酸氨氯地平已有8家通過一致性評價(jià)。2019年仍有12個(gè)受理號申報(bào)一致性評價(jià)魄懂;阿托伐他汀鈣有3家通過一致性評價(jià)沿侈。2019年新4類獲批的廠家有齊魯和興安藥業(yè),申報(bào)的仍有4家市栗;恩替卡韋在2019年有重慶藥友和百奧泰以“新4類”獲批缀拭。恩替卡韋目前已有10個(gè)批文、7家企業(yè)通過一致性評價(jià)填帽。然而蛛淋,這樣“集約式”地申報(bào)、過評蔗须,又為國內(nèi)降價(jià)趨勢創(chuàng)造了條件羊脾。說到底,在仿制藥的戰(zhàn)場上玛耿,科學(xué)立項(xiàng)是企業(yè)轉(zhuǎn)型的關(guān)鍵认畦,也是擺脫上述“尷尬”局面的前提。如特色產(chǎn)品線布局漱蔬、人才戰(zhàn)略御颇、技術(shù)引進(jìn)、數(shù)據(jù)評估等方面都是企業(yè)在立項(xiàng)時(shí)必須考慮的语诈。
業(yè)界對“目錄”還有這些看法
筆者在一段就說道了圈烘,本次入圍“第一批國家重點(diǎn)監(jiān)控藥品目錄”的20個(gè)品種,其銷售額隨后或斷崖式下跌该眨,實(shí)屬“命運(yùn)使然”筋氮。并且,還未“上場”的大批產(chǎn)品兢糯,或因立項(xiàng)失誤心唆,也將面臨“滑鐵盧”。
與此同時(shí)勘天,隨著“第一批國家重點(diǎn)監(jiān)控藥品目錄”的出臺怔揩,有業(yè)內(nèi)人士對其表述了這些觀點(diǎn)。即:
1.入圍的20個(gè)品種是各地方重點(diǎn)監(jiān)控脯丝、輔助用藥的成滩玻客伏伐,從品種上看,無新意可言晕拆。據(jù)醫(yī)藥經(jīng)濟(jì)報(bào)統(tǒng)計(jì)藐翎,“第一批國家重點(diǎn)監(jiān)控藥品目錄”相較于2015年版“安徽輔助用藥目錄”,在化藥及生物制品方面实幕,兩者的重合率為50%吝镣。
2.“目錄”出臺前,絕大多數(shù)產(chǎn)品的銷量總2015年已出現(xiàn)下滑昆庇。例如腦蛋白水解物末贾,近年來的市場增長率在2015年是出現(xiàn)峰值,隨后就逐年下滑整吆,從2017年開始出現(xiàn)負(fù)增長拱撵。
3.文件中針對“管理辦法”上,行業(yè)人士認(rèn)為衛(wèi)健委的通知绎揭,并沒有給出具體可操作的管理要求卑绢,仍然沿用之前的管理辦法,看不出從嚴(yán)管理稻悟、徹底杜絕的決心尸褪。
4.“第一批國家重點(diǎn)監(jiān)控藥品目錄”雖然沒有收錄中藥榄兑,但國家衛(wèi)健委將會(huì)同國家中醫(yī)藥局對重點(diǎn)監(jiān)控合理用藥藥品目錄進(jìn)行動(dòng)態(tài)調(diào)整碉榔。這意味著中藥注射劑仍有可能會(huì)被納入《重點(diǎn)監(jiān)控合理用藥藥品目錄》,評判標(biāo)準(zhǔn)有可能參考中藥注射劑再評價(jià)的臨床試驗(yàn)結(jié)果马窘。并且拄央,根據(jù)“第一批國家重點(diǎn)監(jiān)控藥品目錄文件”規(guī)定西醫(yī)要有一定年限的中醫(yī)藥專業(yè)知識學(xué)習(xí)及考核,才能開具中成藥處方寡专,也可以開具中藥飲片處方存睬。這無疑將中藥的使用門檻進(jìn)一步加大。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 凱萊英藥聞
凱萊英藥聞  2024-11-22
2024-11-22
 58
58

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 動(dòng)脈網(wǎng)
動(dòng)脈網(wǎng)  2024-11-22
2024-11-22
 56
56

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥明康德
藥明康德  2024-11-22
2024-11-22
 61
61
 熱門資訊
熱門資訊