
 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2023-05-08
2023-05-08
 2200
2200
5月3日,禮來宣布donanemab治療早期癥狀性阿爾茨海默踩濉(AD)患者的III期TRAILBLAZER-ALZ 2研究達(dá)到了主要終點(diǎn)刀脏。結(jié)果表明,donanemab能顯著減緩早期癥狀性AD患者的認(rèn)知功能下降牙勘,近一半受試者(47%)在1年內(nèi)沒有疾病進(jìn)展(定義為臨床癡呆評(píng)分沒有下降)停唐,而安慰劑組為29%柔些。禮來預(yù)計(jì)本季度向FDA遞交donanemab的上市申請(qǐng)瘤慕,以尋求加速批準(zhǔn)伞让。

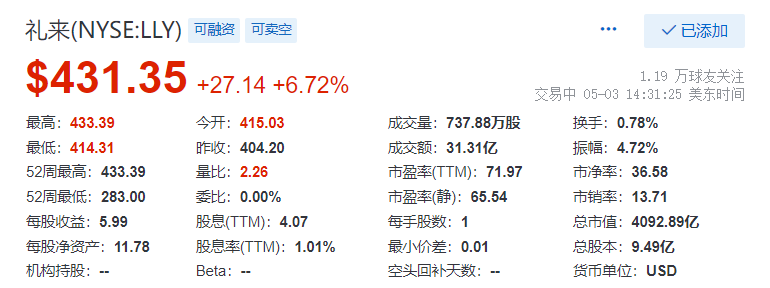
該消息公布后,禮來股價(jià)大漲6%鹰柄,市值突破4000億美元停濒,超越諾和諾德(3780.7億美元)成為純藥企市值第一名菲恢。
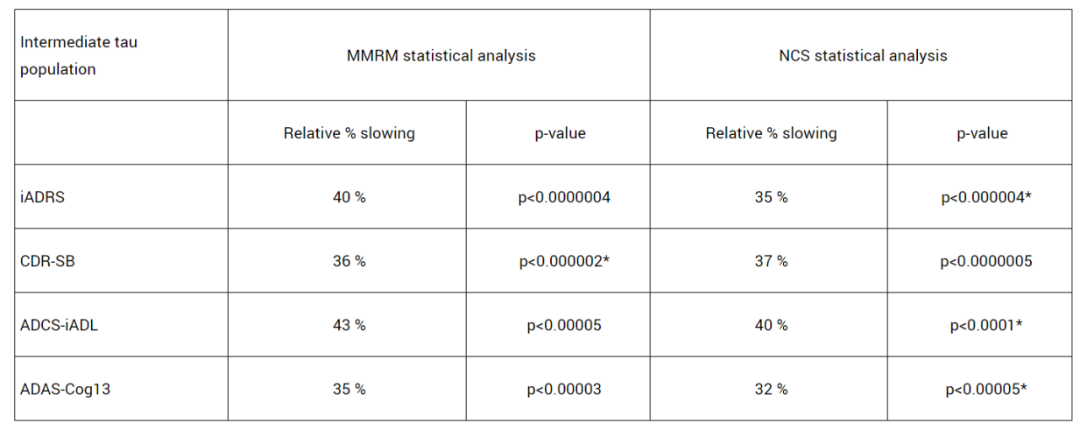
TRAILBLAZER-ALZ 2是一項(xiàng)隨機(jī)、雙盲衣右、安慰劑對(duì)照的III期臨床研究锁孟,主要分析人群(n=1182)為tau蛋白水平中等且有明顯AD臨床癥狀患者。主要終點(diǎn)是AD綜合評(píng)定量表(iADR茁瘦,評(píng)估患者的認(rèn)知能力和生活自理能力)評(píng)分從基線到18個(gè)月的變化品抽,關(guān)鍵次要終點(diǎn)包括基線至18個(gè)月的臨床癡呆評(píng)定量表(CDR-SB,評(píng)估患者的認(rèn)知能力)評(píng)分甜熔、AD協(xié)作研究日常生活能力量表(ADCS iADL)評(píng)分圆恤、AD認(rèn)知量表(ADAS-Cog13)評(píng)分的變化等。
結(jié)果顯示纺非,與安慰劑組相比哑了,接受donanemab治療組患者的iADRS評(píng)分下降速度減緩了35%(p<0.0001)赘方;18個(gè)月時(shí)烧颖,donanemab組CDR-SB評(píng)分較安慰劑組下降速度減緩了36%(p<0.0001);ADCS iADL評(píng)分顯示窄陡,18個(gè)月時(shí)炕淮,donanemab組疾病進(jìn)展速度延緩了40%(p<0.0001)。此外跳夭,donanemab將患者疾病進(jìn)展到下一階段的風(fēng)險(xiǎn)降低了39%(HR=0.61; p<0.001)涂圆。
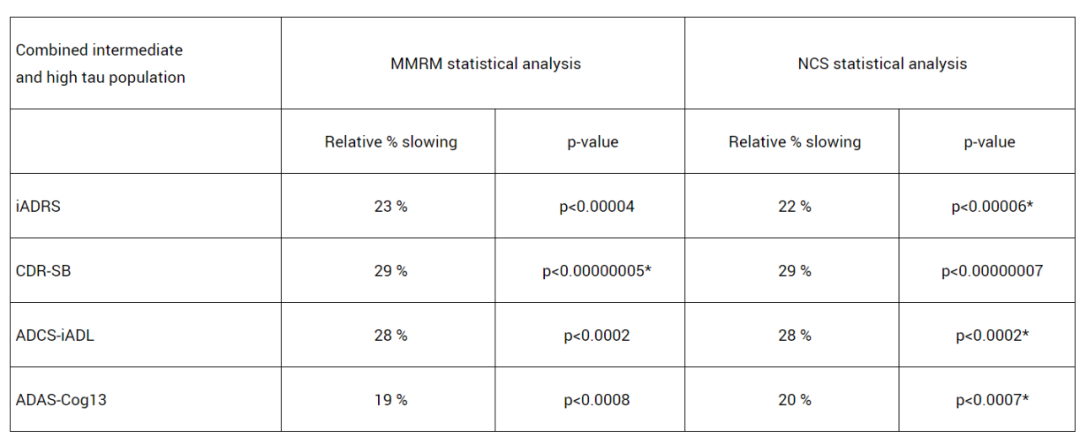
將tau蛋白水平中等人群與較高人群(n=552)結(jié)果合并分析后(n=1736),donanemab治療組仍在所有臨床終點(diǎn)中顯示出有積極結(jié)果(p<0.001)湃儒,其中CDR-SB評(píng)分和iADRS評(píng)分分別將下降速度減緩29%和22%还纤。
安全性方面,donanemab組有24%受試者出現(xiàn)淀粉樣蛋白相關(guān)影像學(xué)異常-水腫(ARIA-E)氯摆,有癥狀A(yù)RIA-E發(fā)生率為6%埠邻;donanemab組有31.4%患者出現(xiàn)腦微出血和淺表鐵質(zhì)沉積(ARIA-H),安慰劑組為13.6%峡冻。大多數(shù)ARIA的嚴(yán)重程度為輕度至中度苞惰,嚴(yán)重ARIA發(fā)生率為1.6%,包括兩例死于ARIA的受試者和經(jīng)歷嚴(yán)重ARIA后死亡的患者最奸;有8.7%患者出現(xiàn)輸液相關(guān)反應(yīng)咕诊,大多為輕度至中度。

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 256
256

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 234
234

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時(shí)間
醫(yī)藥時(shí)間  2024-11-18
2024-11-18
 57
57
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽