
 研發(fā)追蹤
研發(fā)追蹤
 Insight數據庫
Insight數據庫  2023-05-22
2023-05-22
 2559
2559
5 月 17 日犹狮,阿斯利康宣布,III 期臨床試驗 FLAURA2 獲得了高水平陽性結果嘉散,奧希替尼(Tagrisso蟹演,泰瑞沙?)聯(lián)合化療相較于奧希替尼單藥一線治療局部晚期(IIIB-IIIC 期)或轉移性(IV 期)EGFR 突變 NSCLC 中表現(xiàn)出具有統(tǒng)計學顯著性和臨床意義的 PFS 改善。
目前,OS 數據尚未成熟,將在后續(xù)分析中繼續(xù)評估唐断;安全性方面則與既往各藥物特征一致。阿斯利康將在后續(xù)醫(yī)學大會上公布 FLAURA2 數據杭抠。
這項臨床試驗的成功,意味著 EGFRm NSCLC 患者有望迎來更優(yōu)治療方案恳啥,延長其一線療法獲益時間偏灿。

截圖來自:阿斯利康官網
FLAURA2(登記號:NCT04035486)是一項隨機、開放標簽钝的、全球多中心 III 期臨床試驗翁垂,納入 586 名局部晚期(IIIB-IIIC 期)或轉移性(IV 期)EGFRm NSCLC 患者進行一線治療「廴啵患者接受每日一次奧希替尼 80 mg 聯(lián)合每三周一次化療(培美曲塞 [500 mg/m2] + 順鉑 [75 mg/m2] 或卡鉑[AUC5])减磷,持續(xù)四個周期;隨后每三周接受一次奧希替尼 + 培美曲塞維持治療宰孙。
這項試驗登記于 2019 年 6 月氏赴,在美國、歐洲坚哲、亞洲等 20 多個國家的 150 多個中心招募患者服酥,其中也包括了中國地區(qū)的 112 例患者。本次積極結果是對 PFS 主要終點的最終分析御欢。試驗仍在進行中找肤,將繼續(xù)評估 OS 的次要終點。
FLAURA2 試驗歷程
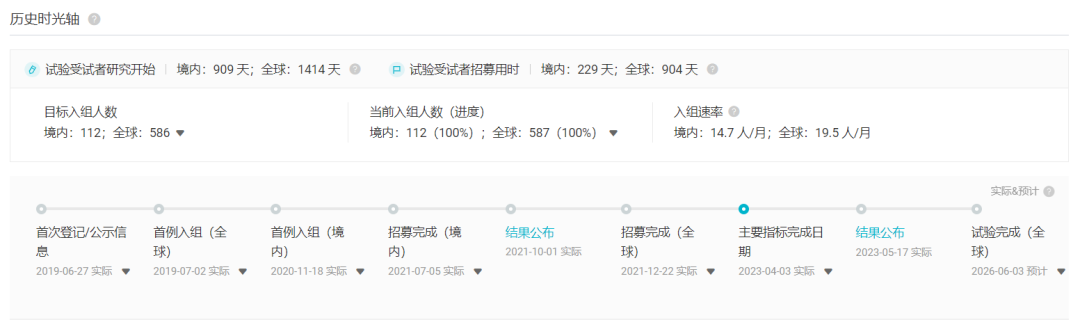
截圖來自:Insight 數據庫網頁版(http://db.dxy.cn/v5/home/)
奧希替尼作為首款獲批上市升碱、臨床證據最充分的三代 EGFR 抑制劑踩林,其單藥療法已經在中美日歐在內的 100 多個國家或地區(qū)獲批上市,獲批適應癥包括晚期 EGFRm NSCLC 二線是酣、一線治療以及早期 EGFRm NSCLC(IB/II/IIIA 期)輔助治療醋掖。
除了在晚期疾病狀態(tài)中評估奧希替尼與化療的聯(lián)合療法(FLAURA2 研究)之外,阿斯利康還瞄準早期肺癌開展了多項 III 期臨床黄刚,包括對于新輔助可切除環(huán)境(NeoADAURA 研究)车海、IA2-IA3 期輔助可切除環(huán)境(ADAURA2)和 III 期局部晚期不可切除環(huán)境(LAURA)。
同時隘击,針對耐藥問題侍芝,阿斯利康也在進行持續(xù)探索:聯(lián)用口服 MET 抑制劑賽沃替尼開展 II 期臨床 SAVANNAH 和 III 期臨床 SAFFRON,聯(lián)用多種其他藥物的 II 期臨床 ORCHARD埋同。不光奧希替尼聯(lián)合療法州叠,阿斯利康還基于自家平臺開發(fā)了 EGFR/c-MET 雙靶點 ADC 新藥 AZD9592棵红,同樣旨在解決耐藥問題。
在整體 NSCLC 布局方面咧栗,阿斯利康期望到 2030 年其商業(yè)化療法能夠覆蓋超 50% 的非小細胞肺癌患者逆甜,從當前臨床布局來看:
奧希替尼有望作為約 16% 的 EGFR 突變人群的基石療法,耐藥群體則有 AZD9592致板;
度伐利尤單抗在約 70% 的 IO 敏感不可切除疾病群體中持續(xù)建設領導地位交煞,后繼雙抗管線如 PD-1/TIGIT 雙抗 rilvegostomig、PD-1/CTLA-4 雙抗 volrustomig斟或、PD-1/TIM3 雙抗 sabestomig 則有望成為下一代 PD-(L)1 為患者提供改善熬鸟;
其他驅動基因突變約 12% 的患者,部分有度伐利尤單抗和 Dato-DXd 覆蓋肮插;而 2% 的 HER2 突變/過表達群體中則以 Enhertu 為首的 ADC 管線替代系統(tǒng)化療秸铣。同時,包括細胞療法在內的新平臺新管線也在持續(xù)推進晚惊。
阿斯利康肺癌領域布局
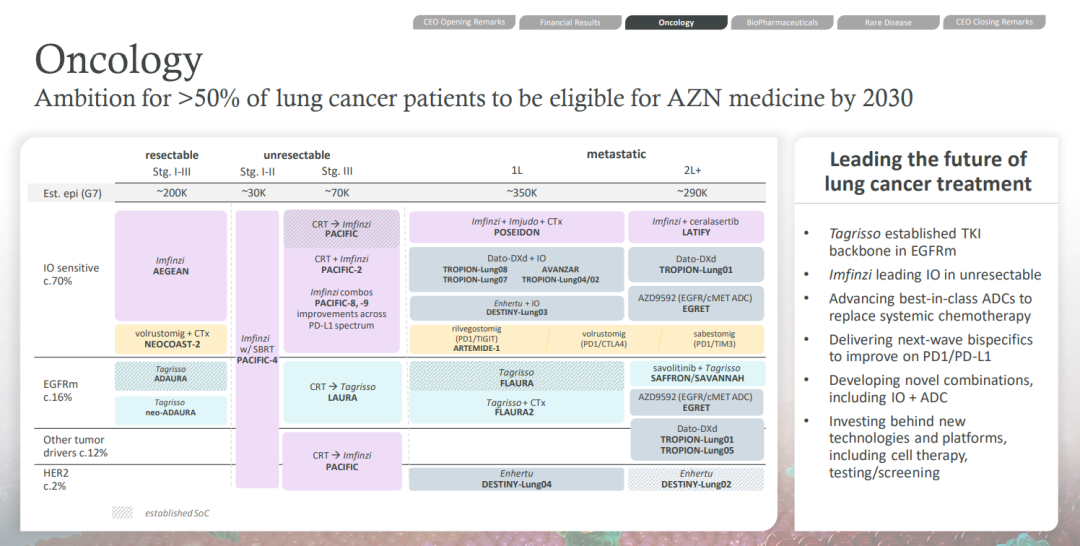
*Est. epi (G7) 即在歐美日 7 國的流行病學 截圖來自:阿斯利康 2023Q1 季報

 研發(fā)追蹤
研發(fā)追蹤
 藥研網
藥研網  2024-11-18
2024-11-18
 257
257

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 236
236

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 57
57