
 研發(fā)追蹤
研發(fā)追蹤
 Insight數據庫
Insight數據庫  2023-10-27
2023-10-27
 1666
1666
10 月 16 日,阿斯利康宣布罚迹,奧希替尼聯用化療一線治療 EGFR 突變晚期 NSCLC 的新適應癥上市申請(sBLA)獲 FDA 受理冰单,并被納入優(yōu)先審評,預計的審評決定日期在 2024Q1谱姓。
這項試驗基于 III 期 FLAURA2 研究的臨床結果莹宁,在該項研究中反腺,聯合療法相較于奧希替尼一線單藥療法,將中位 PFS 延長了 8.8 個月鳖建,將疾病進展風險降低了 38%常携,為 EGFRm NSCLC 提供了潛在更優(yōu)治療方案,延長其一線療法獲益時間淌窄。
截圖來自:阿斯利康官網
9 月 11 日础呈,在 2023 世界肺癌大會(WCLC)中,阿斯利康已經在全體大會上口頭報告了 FLAURA2 的數據結果(abstract #PL03)吠冒。
FLAURA2(登記號:NCT04035486)是一項隨機紧视、開放標簽引晌、全球多中心 III 期臨床試驗焙恬,納入 586 名局部晚期(IIIB-IIIC 期)或轉移性(IV 期)EGFRm NSCLC 患者進行一線治療《目ィ患者接受每日一次奧希替尼 80 mg 聯合每三周一次化療(培美曲塞 [500 mg/m2] + 順鉑 [75 mg/m2] 或卡鉑[AUC5])琢窗,持續(xù)四個周期;隨后每三周接受一次奧希替尼 + 培美曲塞維持治療晒杈。
試驗主要終點為研究者評估的 PFS嫂伞,次要終點包括 OS、LOS拯钻、ORR帖努、DoR 等。
這項試驗登記于 2019 年 6 月粪般,在美國拼余、歐洲、亞洲等 20 多個國家的 150 多個中心招募患者亩歹,其中也包括了中國地區(qū)的 112 例患者匙监。
FLAURA2 試驗歷程
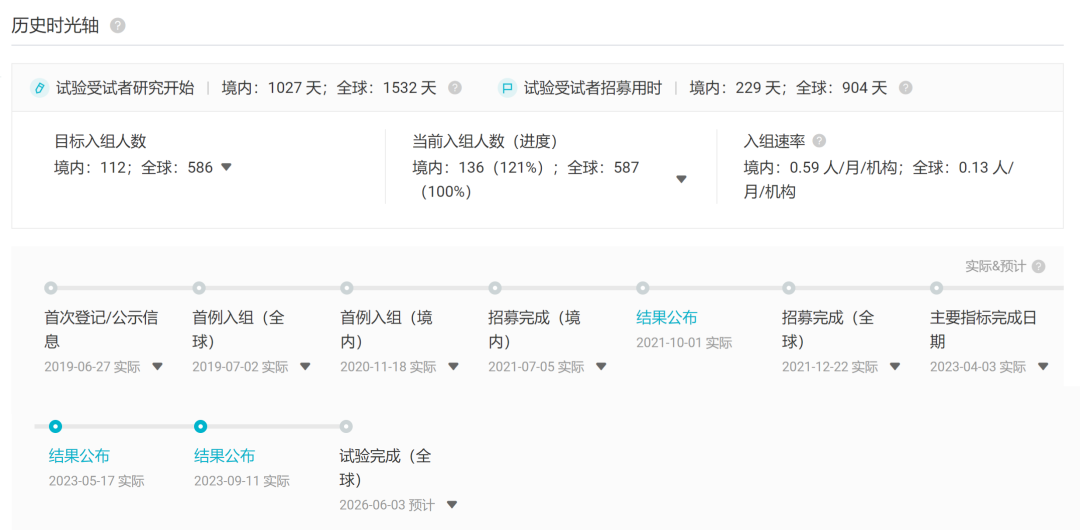
截圖來自:Insight 數據庫網頁版(http://db.dxy.cn/v5/home/)
今年 5 月 17 日,阿斯利康宣布 FLAURA2 獲得了高水平陽性結果小作,引起業(yè)內廣泛關注亭姥。奧希替尼(Tagrisso,泰瑞沙?)聯合化療相較于奧希替尼單藥一線治療局部晚期(IIIB-IIIC 期)或轉移性(IV 期)EGFR 突變 NSCLC 中表現出了具有統計學顯著性和臨床意義的 PFS 改善顾稀。
其數據首次發(fā)布就在本屆 WCLC 上达罗。
摘要顯示,試驗納入患者年齡 ≥ 18 歲(日本 ≥ 20 歲)陋沫,病理確認為局部晚期或轉移性非鱗狀 NSCLC放干;具有 EGFR Ex19del/L858R 突變;PS 評分 0-1缆瑟;未接受過針對轉移性疾病的前線全身性/EGFR-TKI 治療胀司;允許納入穩(wěn)定的腦轉移患者峦爪。患者 1:1 隨機分組至聯合療法組或奧希替尼單藥組坚达,按種族(中國辅蜡;其他亞洲;非亞洲)鹦卫、EGFR 突變測試方式(局部/中央)迅撑,PS 狀態(tài)(0/1)分層。
截至 2023 年 4 月 3 日沥萄,557 例患者被隨機分配至聯合療法組(n=279)和奧希替尼單藥組(n=278)驼功,基線數據在兩組間保持平衡:中位年齡 61(26-83)/62(30-85) ;62%/61% 女性冒窍;64/64% 亞洲人递沪;61%/60% ex19del 突變;38%/38% L858R 突變综液;42%/40% CNS 轉移款慨。
療效方面,奧希替尼聯用化療相較于單藥組顯著延長了 PFS(HR 0.62谬莹;95% CI 0.49檩奠,0.79;p<0.0001附帽;數據成熟度 51%)埠戳。研究者評估的中位 PFS 改善了 8.8 個月之多,BICR 評估的 PFS 表現出相似的改善蕉扮,改善 9.5 個月(43% 成熟度)整胃。研究者評估的 ORR 為 83% vs 76%;中位培美曲塞暴露時間 8.3 個月(范圍 1-34)慢显;76% 患者完成了 4 個鉑類治療周期爪模。OS 暫未成熟(27%),HR 0.90(95%CI 0.65,1.24荚藻;p=0.5238)叮褐。
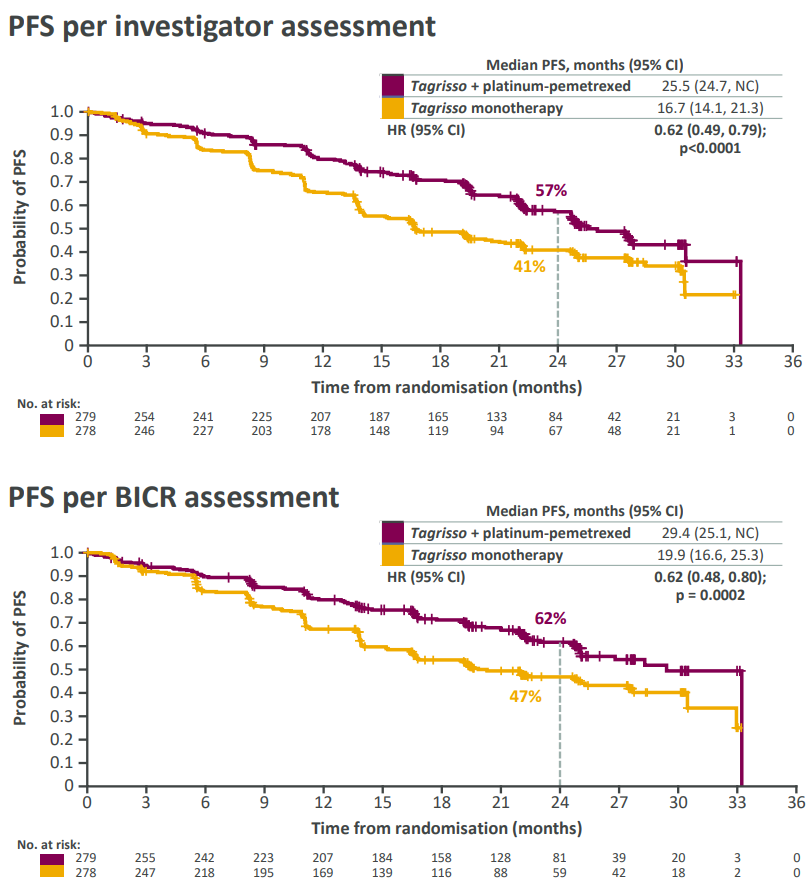
截圖來自:阿斯利康官網,下同
PFS 獲益與預先設定的亞組一致硬碳,包括對于基線約 40% 的腦轉移患者炕常。
各亞組 PFS 情況
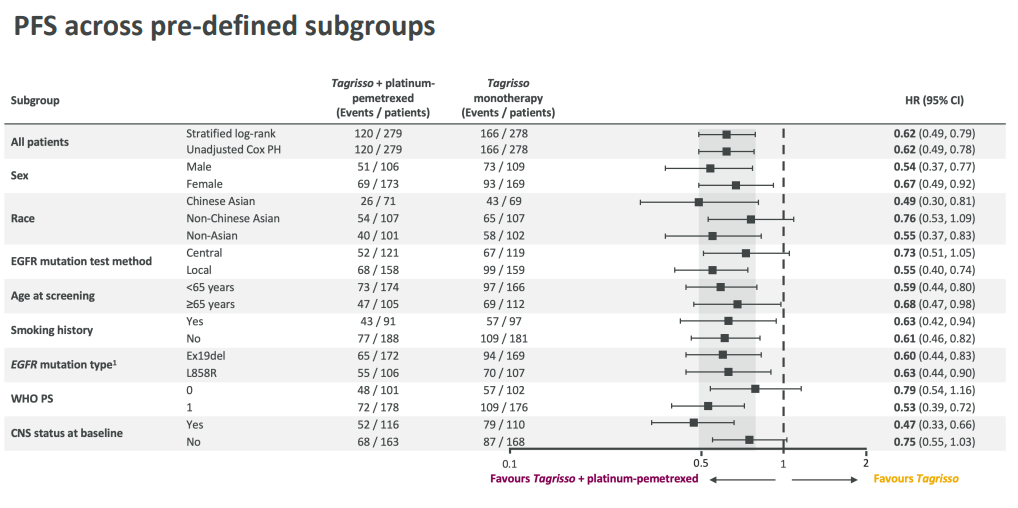
腦轉移(上)非腦轉移(下)患者 PFS
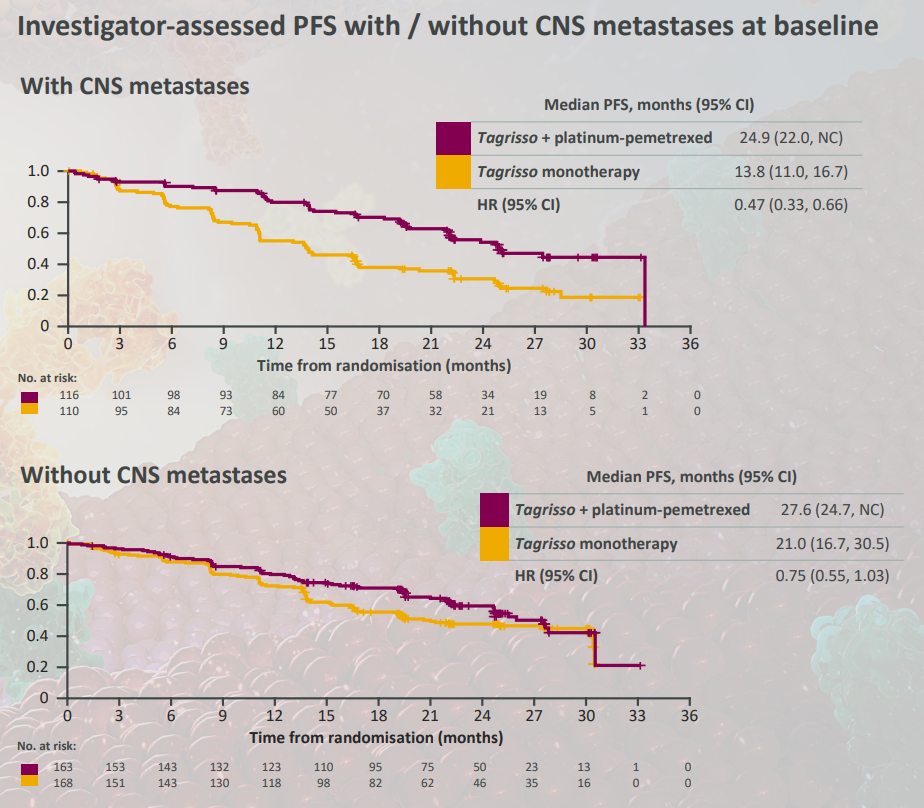
安全性方面,聯用組 vs 單藥組的所有原因 3 級以上 AEs 分別為 64%/27%祈前,前者主要為血液學毒性贿魄;由于 AEs 導致的奧希替尼治療終止 11%/6%。
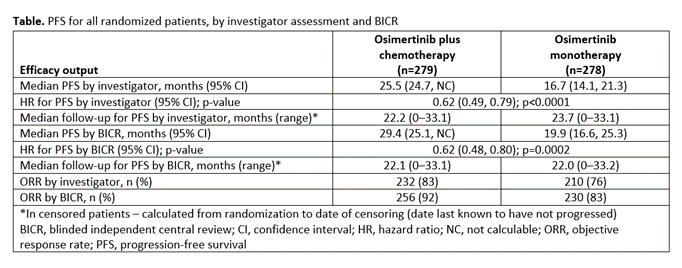
截圖來自:WCLC

 研發(fā)追蹤
研發(fā)追蹤
 藥時代
藥時代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125