
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥明康德
藥明康德  2024-05-23
2024-05-23
 381
381
羅氏(Roche)公司今天宣布富稻,美國FDA授予其在研口服小分子inavolisib聯(lián)合CDK4/6抑制劑Ibrance(palbociclib)和氟維司群(fulvestrant)突破性療法認定(BTD)舔庶,用于治療腫瘤帶有PIK3CA突變、激素受體(HR)陽性箱沦、人類表皮生長因子受體2(HER2)陰性局部晚期或轉移性乳腺癌成年患者辩恼,這些患者在完成輔助內(nèi)分泌治療后12個月內(nèi)發(fā)生復發(fā)。
HR陽性乳腺癌是所有乳腺癌中最常見的類型谓形,約占70%荸速。HR陽性乳腺癌指的是那些表達雌激素受體(ER)或/和孕激素受體(PR)的乳腺癌,這些受體能夠促進腫瘤生長柒谈。確診為HR陽性轉移性乳腺癌的患者通常面臨疾病進展和治療副作用的風險穴阱,因此這類患者需要額外的治療。PI3K信號通路在HR陽性乳腺癌中經(jīng)常失調(diào)胖辨,多是由于PIK3CA的激活突變所致爱蚣,這已被確定為對標準內(nèi)分泌療法與CDK4/6抑制劑聯(lián)合療法產(chǎn)生耐藥性的潛在機制之一。
美國FDA授予inavolisib聯(lián)合療法BTD主要是基于INAVO120臨床3期試驗的積極結果讹毁。該試驗是一項隨機间炮、雙盲焙厂、安慰劑對照研究,旨在評估與安慰劑加Ibrance和氟維司群相較毒奇,inavolisib聯(lián)合Ibrance和氟維司群在治療PIK3CA突變蔑辽、HR陽性、HER2陰性局部晚期或轉移性乳腺癌患者的療效和安全性沥葛,這些患者在治療期間或完成輔助內(nèi)分泌治療后12個月內(nèi)出現(xiàn)疾病進展触尚,且未接受過治療轉移腫瘤的系統(tǒng)性治療。該研究納入了325例患者齿穗,主要終點是研究者評估的無進展生存期(PFS)傲隶,定義為從隨機分組到疾病進展或患者因任何原因死亡的時間。次要終點包括總生存期窃页、客觀緩解率和臨床受益率跺株。
分析顯示,與安慰劑組合(PFS=7.3個月)相比脖卖,inavolisib聯(lián)合療法(PFS=15.0個月)將患者病情惡化或死亡的風險降低了57%乒省,(HR=0.43,95% CI:0.32-0.59畦木,p<0.0001)袖扛。目前總生存期數(shù)據(jù)尚不成熟,但已觀察到明顯的積極趨勢(分層HR=0.64十籍,95% CI:0.43-0.97蛆封,p=0.0338)」蠢酰總生存期的后續(xù)隨訪將持續(xù)到下一次分析惨篱。INAVO120試驗的數(shù)據(jù)也正在提交給包括歐洲藥品管理局(EMA)在內(nèi)的其他全球監(jiān)管單位。
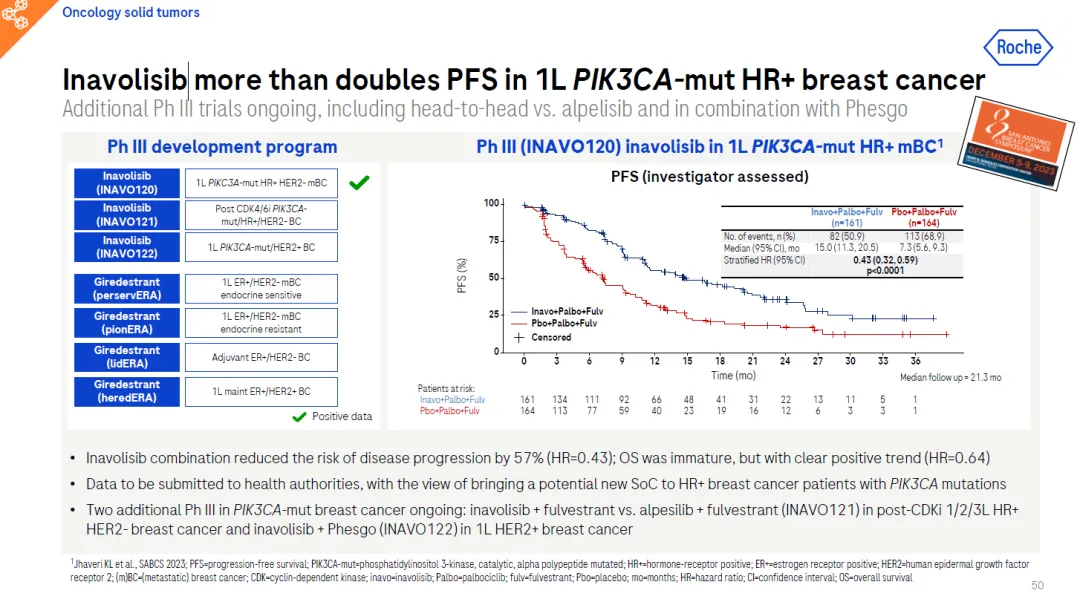
▲Inavolisib治療乳腺癌的試驗結果(圖片來源:參考資料[2])
Inavolisib聯(lián)合療法的耐受性良好幌侧,不良事件與此前研究的已知安全性特征一致令掠,未觀察到新的安全信號。
Inavolisib是一種口服療法整栏,具有高度的體外PI3Kα抑制效力和選擇性睹蜈,能夠特異性觸發(fā)PI3Kα蛋白突變體的分解。通過這種獨特的雙重作用機制着雪,inavolisib可能為HR陽性/HER2陰性牲课、PIK3CA突變的晚期乳腺癌患者提供耐受良好、持久的疾病控制和潛在改善的結局瞎励。約有40%的HR陽性乳腺癌患者帶有PIK3CA基因突變女灸,該突變可能導致腫瘤生長失控、疾病進展和對內(nèi)分泌治療的耐藥性蒜肥。
除INAVO120外但雨,羅氏目前還在進行另外兩項臨床3期研究蕉妇,以檢視inavolisib與不同藥物的組合療法對帶有PIK3CA突變的局部晚期或轉移性乳腺癌患者的作用,包含(1)INAVO122試驗檢視HR陽性/HER2陰性乳腺癌患者經(jīng)CDK4/6抑制劑和內(nèi)分泌聯(lián)合治療后螺谅,接受inavolisib與氟維司群聯(lián)合療法與接受PI3K抑制劑alpelisib加氟維司群聯(lián)合療法相較的療效腹忽。(2)INAVO122試驗則檢視inavolisib與帕妥珠單抗和曲妥珠單抗聯(lián)合皮下注射,與帕妥珠單抗加曲妥珠單抗皮下注射以及醫(yī)生選擇的內(nèi)分泌療法聯(lián)合相比砚作,用以作為HER2陽性疾病維持療法的作用窘奏。
參考資料:
[1] FDA grants Breakthrough Therapy Designation to Roche’s inavolisib for advanced hormone receptor-positive, HER2-negative breast cancer with a PIK3CA mutation. Retrieved May 21, 2024 from https://www.roche.com/media/releases/med-cor-2024-05-21
[2] Rche Reporting,Retrieved Feb 2, 2024 from https://assets.roche.com/f/176343/x/ac48d3ba3b/irp240201-a.pdf

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 70
70

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 72
72

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 74
74