
 產業(yè)資訊
產業(yè)資訊
 BiG生物創(chuàng)新社
BiG生物創(chuàng)新社  2024-05-29
2024-05-29
 817
817

圖1. ADC概念圖(來自宜聯(lián)生物官網(wǎng))
作者|小麥
2024年5月27日惯斥,宜聯(lián)生物宣布與BioNTech猛遍,達成一項預付款2500萬美元滴图、總額可能高達18億美元新的戰(zhàn)略合作協(xié)議癞埠。
據(jù)此項協(xié)議條款儡矫,BioNTech將獲得一項利用宜聯(lián)生物TMALIN? ADC技術平臺開發(fā)針對限定的某幾個前沿創(chuàng)新靶點的ADC產品的獨家選擇權及相應全球獨家許可啥闪。
這不是宜聯(lián)生物首次與BioNTech合作户寺,去年10月份膀娱,宜聯(lián)生物與BioNTech就HER3靶向ADC YL202達成一項總金額超10億美元的合作協(xié)議。
除此之外抢督,近年來稼注,宜聯(lián)生物還與羅氏写并、再鼎、輝瑞栓堕、復宏漢霖等藥企方頻頻達成合作于嚼,本文就宜聯(lián)生物管線和技術平臺做簡要盤點。
宜聯(lián)生物TMALIN技術平臺介紹
傳統(tǒng)ADC藥物仍有很多缺點裤爆,包括:1. 抵抗原表達靶點效果不佳处监;2. 需要ADC內吞,抗體范圍有限糕伐;3. 分子量大砰琢,穿透實體瘤效果差;4. 連接子不穩(wěn)定等(圖2)[1]良瞧。

圖2. ADC的局限
TMALIN全稱是Tumor_Microenvironment_Activable_LINker陪汽,是宜聯(lián)生物擁有獨立自主知識產權的新型ADC平臺技術,使用不可逆的嘧啶偶聯(lián)技術來防止經(jīng)典的基于馬來酰亞胺的接頭-有效載荷與白蛋白的交換反應褥蚯,可以解決現(xiàn)有ADC技術的缺陷(圖3)挚冤。
圖3. TMALIN技術平臺
TMALIN技術平臺有獨特的酶消化特性,具有在腫瘤微環(huán)境中細胞外溶解的能力赞庶,不依賴抗體內吞能力训挡,使ADC能夠豐富腫瘤微環(huán)境,增加腫瘤中有效載荷的比例和血液濃度歧强,并具有較高的治療指數(shù)澜薄,酶消化特性和腫瘤富集特性還可以使有效載荷在腫瘤組織中大大富集,產生較強的旁觀者效應摊册,在抗原表達低甚至無抗原表達的腫瘤中產生良好的抗腫瘤作用肤京。
此外,TMALIN技術平臺可利用細胞外腫瘤微環(huán)境和細胞內溶酶體雙重裂解機制找骏,形成的ADC具有極高的全身循環(huán)穩(wěn)定性腿逞、優(yōu)異的溶解性和優(yōu)異的化學穩(wěn)定性、耦合效率高(≥90%)許多優(yōu)點测捐,已在多個體內藥效模型與安全性評價實驗中汤钻,展現(xiàn)出相比于現(xiàn)有ADC技術更寬的藥物治療窗。
宜聯(lián)生物管線介紹
宜聯(lián)生物成立于2020年法简,研發(fā)管線包含多款ADC新藥荡唾,包括靶向B7H3 ADC YL201、HER3 ADC YL202蓝鹿、NaPi2b ADC YL205矩允、c-MET ADC YL211、DLL3 ADC YL212等(圖4)。
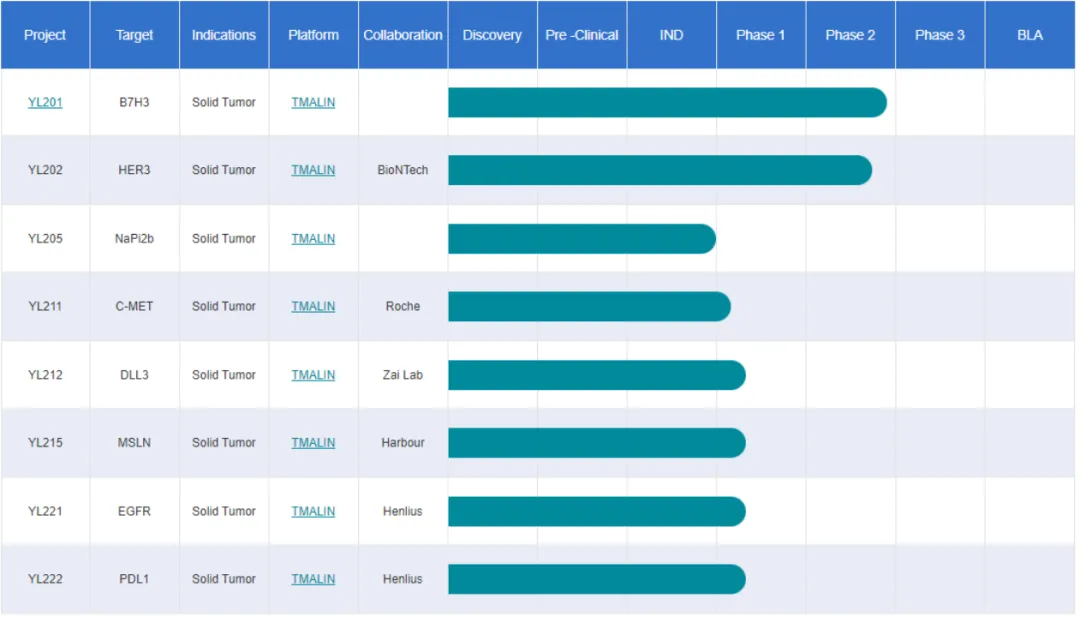
圖4. 宜聯(lián)生物研發(fā)管線(來自其官網(wǎng))
2.1 YL201
YL201是由宜聯(lián)生物研發(fā)的靶向B7-H3的ADC藥物燎厘,通過可裂解連接鏈將B7H3單抗與拓撲異構酶抑制劑YL0010014偶聯(lián)而得(圖5)[2]薇硬。
B7-H3靶點在食管癌上高表達,YL201結合宜聯(lián)生物TMALIN技術平臺腫瘤微環(huán)境和傳統(tǒng)溶酶體胞外胞內雙重裂解機制蠢琳,能有效殺傷食管癌腫瘤細胞啊终,并已在臨床前和臨床階段的數(shù)據(jù)中得到了驗證。
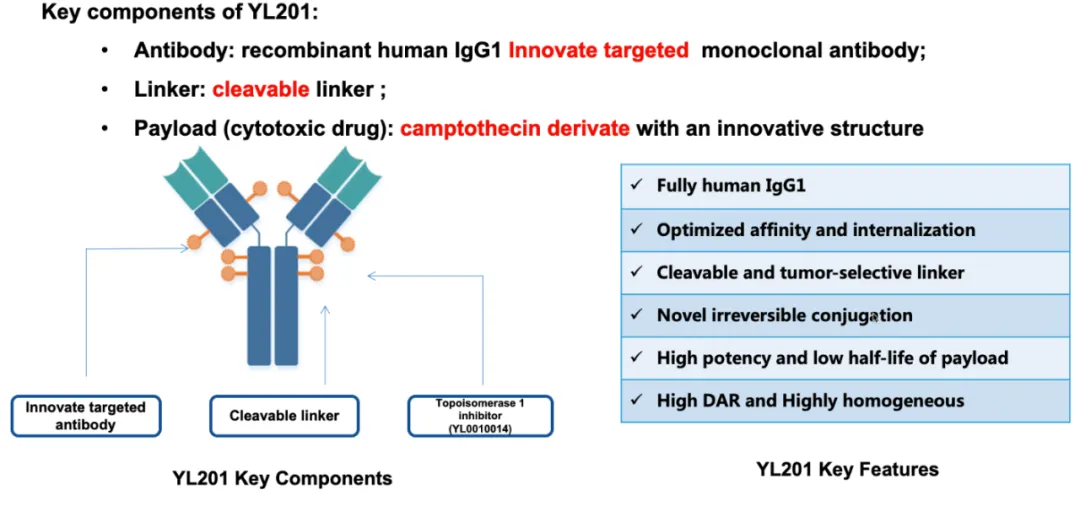
圖5. YL201的結構
YL201相繼于2022年4月和5月獲FDA和NMPA批準臨床傲须,并于2023年11月獲得美國FDA授予孤兒藥資格蓝牲,用于治療食管癌。
2.2 YL202:授權BioNTech泰讽,最高金額超10億美元
YL202是由宜聯(lián)生物研發(fā)的靶向HER3的ADC藥物例衍,HER3與明星靶點EGFR、HER2同屬HER家族已卸,研究表明佛玄,多數(shù)腫瘤中HER3都有高表達,包括非小細胞肺癌累澡、食管癌梦抢、結直腸癌、乳腺癌愧哟、卵巢癌和黑色素瘤等奥吩,而且HER3 的高表達往往也與疾病進展和/或預后不良有關,且和部分腫瘤的進展和轉移相關蕊梧。
去年AACR會議上划搓,Xu等人YL202的臨床前活性,研究結果顯示:YL202對腫瘤細胞表現(xiàn)出強大的反應性配亮、高度內化和強大的細胞毒性(圖6)[3]验脐。
YL202在多種癌癥類型的細胞系和患者來源的異種移植物(CDX和PDX)小鼠模型中也顯示出顯著的劑量依賴性抗腫瘤活性,并且可以誘導腫瘤完全消退吗罪,沒有可觀察到的毒性尚蔗。
在為期 28 天的食蟹猴研究中毛凶,YL202 顯示出穩(wěn)定的 PK 譜话贯,ADC 和 TAb 曲線重疊。使用食蟹猴的GLP毒性研究表明帘圣,YL202耐受性良好露使,重復給藥的計算治療指數(shù)(TI,HNSTD/MED)為~100饼酱。在達到最大耐受劑量 (MTD) 的劑量下未觀察到肺或血小板毒性發(fā)現(xiàn)答肤。
今年ASCO會議上YL202(BNT326)用于局部晚期或轉移性非小細胞肺癌和乳腺癌患者的首次人體 I 期試驗的初步結果被報道。
研究結果顯示:52例患者給藥,包括39例非小細胞肺癌愧杯,13例乳腺癌涎才,對于46例可評估療效患者,ORR為37%力九,DCR為93.5%(圖6)[4]耍铜。
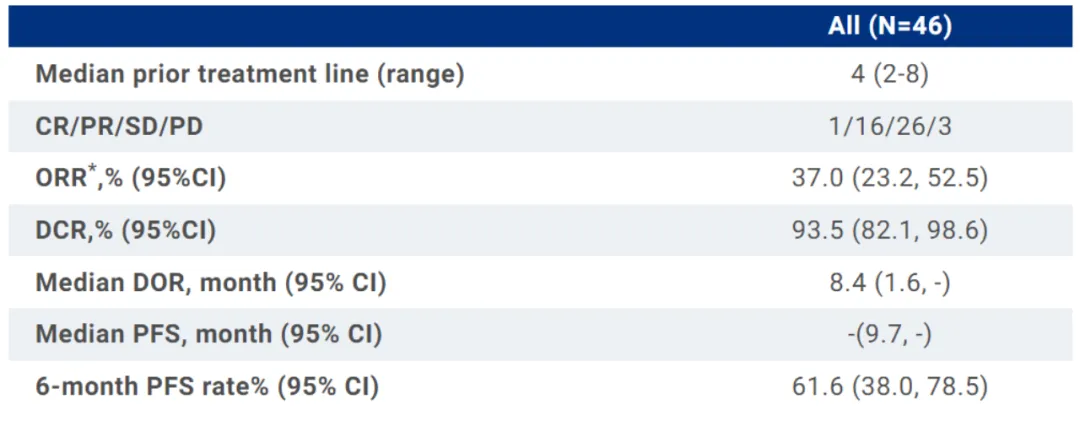
圖6. YL202臨床結果
2.3 YL205
YL205是由宜聯(lián)生物基于其TMALIN技術平臺研發(fā)的一種新型的NaPi2b靶向ADC,NaPi2b是由 SLC34A2 基因編碼跌前,是一種細胞表面鈉依賴性磷酸轉運蛋白棕兼,在某些癌癥(包括卵巢癌、肺癌抵乓、甲狀腺癌和乳腺癌)中高度表達伴挚,在正常組織中的表達有限。
YL205 是通過蛋白酶可切割接頭將抗 NaPi2b 人單克隆抗體與新型拓撲異構酶 1 抑制劑偶聯(lián)而得灾炭,藥物抗體比(DAR)為 8(圖7)茎芋。
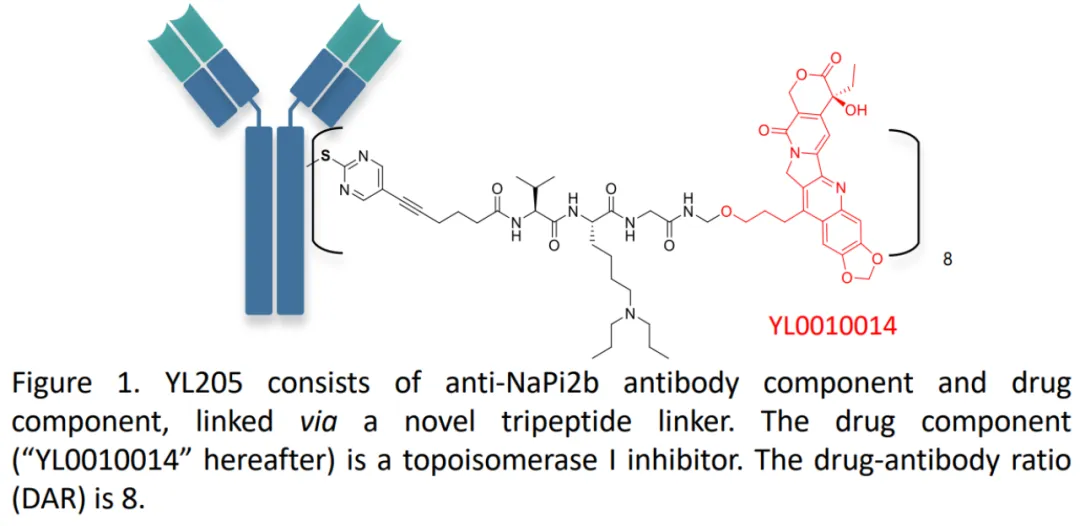
圖7. YL205的結構
今年AACR會議上,宜聯(lián)生物報道了YL205的臨床前活性蜈出,研究結果顯示败徊,YL205在表達 NaPi2b腫瘤細胞中表現(xiàn)出有效的內化和強大的細胞毒性(圖8)[5]。
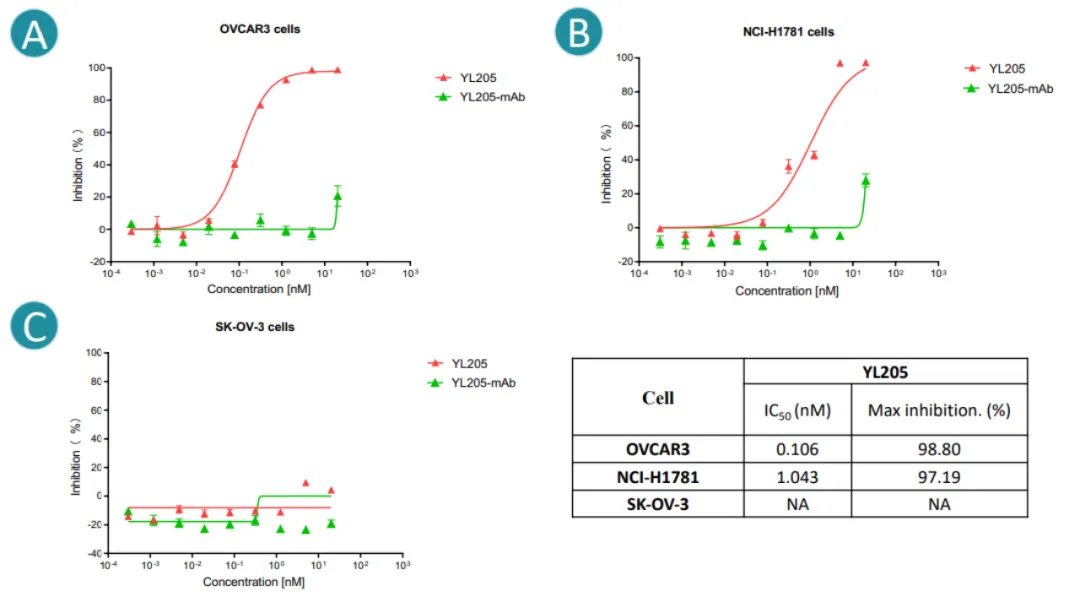
圖8. YL205在NaPi2b高OVCAR3細胞(A)和NaPi2b培養(yǎng)基NCI-H1781細胞 (B)中顯示出強大的細胞毒性呆逼,但在NaPi2b陰性的SK-OV-3細胞中無活性 (C)侣豌。
在體內,YL205耐受性良好嘲陋,以劑量依賴性方式有效抑制異種移植腫瘤生長(圖9)幼浩。
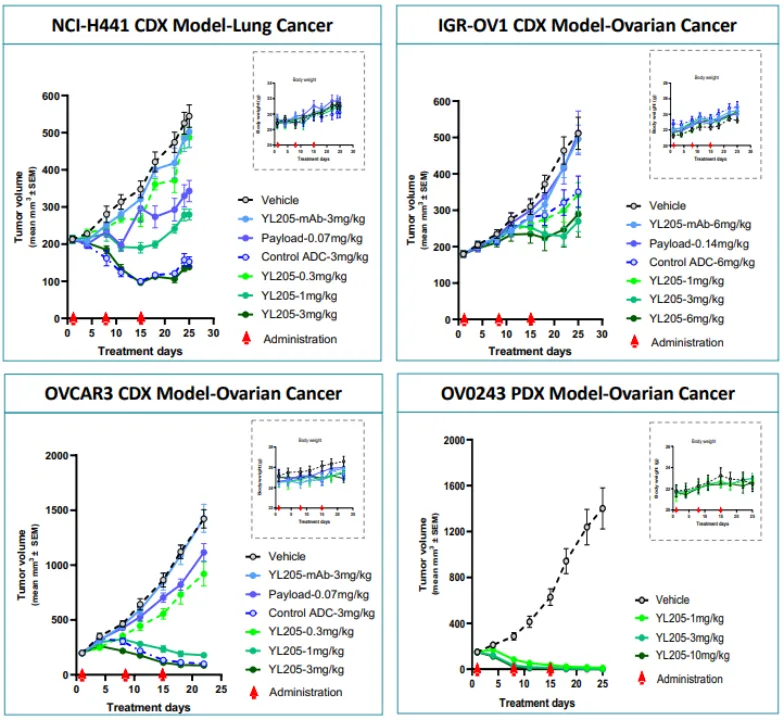
圖9. YL205在具有不同NaPi2b表達水平的異種移植模型中顯示出有效的抗腫瘤活性(低:NCI H441;高:OVCAR3、IGR-OV3 和 OV0243)
此外铸烈,YL205顯示出良好的PK特征软健,并在循環(huán)中保持高度穩(wěn)定,證明在食蟹猴中ADC和總抗體PK曲線的重疊(圖10)砰吻。
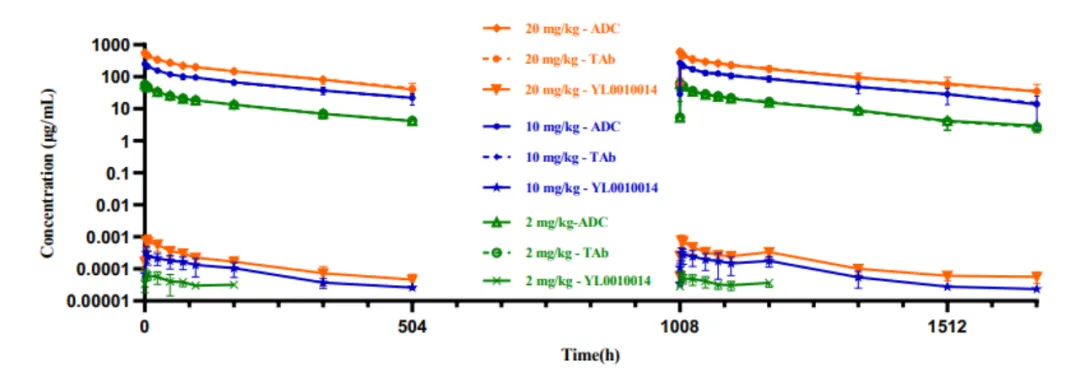
圖10. YL205在食蟹猴的PK性質祸榨。
這些結果表明,YL205具有良好的治療優(yōu)勢且险,并且具有解決表達NaPi2b的腫瘤患者未滿足的醫(yī)療需求的潛力垢雨。
2.4 YL211::出海羅氏,金額超10億美元
YL211 由由宜聯(lián)生物研發(fā)的靶向c-MET的ADC藥物敛旗,通過蛋白酶可裂解接頭將抗 cMET 人源化單克隆抗體與新型拓撲異構酶1抑制劑偶聯(lián)而得辐践,DAR為8,隨著有效載荷在腫瘤微環(huán)境中的細胞外釋放库说,在與腫瘤細胞表面的cMET結合后狂鞋,抗原-ADC復合物被內化到溶酶體囊泡中片择,隨后釋放毒性有效載荷。
今年AACR會議上骚揍,Xiao等人報道了YL211的臨床前活性字管,YL211可以驅動細胞周期停滯、細胞凋亡信不、PARP/半胱天冬酶 7 表達升高纤掸,以及細胞死亡和旁觀者效應(圖11)[6]。

在體內浑塞,YL211在引起腫瘤消退方面顯示出卓越的療效借跪,并且在細胞系和患者來源的異種移植物(CDX和PDX)小鼠模型中都顯示出良好的耐受性,具有低到高cMET表達水平(H358酌壕,CR5088等)掏愁。
猴子體內藥代動力學表明,YL211在循環(huán)中釋放的有效載荷小于0.1%(摩爾比)時高度穩(wěn)定卵牍。GLP安全性評估表明果港,在猴子中具有良好的安全性,并且沒有脫靶毒性陋锚。
這些臨床前數(shù)據(jù)表明潘谴,連接子在循環(huán)中的穩(wěn)定性以及有效釋放有效載荷在腫瘤中具有改善的治療窗口。綜上所述是菇,臨床前數(shù)據(jù)表明哆沽,YL211可能是一種有前途的cMET陽性癌癥患者治療策略。
2.5 YL212:全球權益授權再鼎
YL212 是由由宜聯(lián)生物研發(fā)的靶向DLL3 的ADC藥物枣肚,DLL3 是一種在小細胞肺癌 (SCLC) 和神經(jīng)內分泌腫瘤中過度表達的 Notch 配體抑制劑贬嚷。
2023年4月27日,宜聯(lián)生物與再鼎醫(yī)藥就YL212/ ZL-1310達成戰(zhàn)略合作和全球獨家許可協(xié)議丐鸽。
根據(jù)協(xié)議條款汇光,宜聯(lián)生物將有權獲得預付款和基于開發(fā)和銷售的里程碑付款,以及全球年度凈銷售額的分級特許權使用費和潛在的第三方許可分成郊男。再鼎醫(yī)藥將負責全球所有的開發(fā)和商業(yè)化活動旱谐。
今年1月,再鼎醫(yī)藥在美國啟動了ZL-1310一期臨床研究并完成了首例患者入組孵堪,隨后2月份撤防,再鼎醫(yī)藥宣布ZL-1310用于治療小細胞肺癌的全球一期臨床研究,已完成大中華區(qū)首例患者入組锯梁。
2.6 YL215:與和鉑醫(yī)藥子公司諾納生物一致同意授權給輝瑞
YL215(HBM9033)是由宜聯(lián)生物和和鉑醫(yī)藥共同開發(fā)的靶向MSLN的ADC藥物即碗,HBM9033中的全人源單克隆抗體(mAb)由和鉑醫(yī)藥的Harbour Mice平臺產生焰情,具有良好的特性陌凳,可保持與膜結合型MSLN的強結合和內化同時減少與游離型MSLN的結合,同時HBM9033采用了宜聯(lián)生物最新一代TMALIN平臺技術偶聯(lián)而得。
2023年12月15日合敦,宜聯(lián)生物和和鉑醫(yī)藥子公司諾納生物一致同意諾納生物有權就雙方共同開發(fā)的ADC產品HBM9033許可給被許可第三方輝瑞初橘,宜聯(lián)生物有權基于諾納生物與輝瑞合作獲得一定比例的分許可分成。
2023年8月28日宣布充岛,和鉑醫(yī)藥宣布在美國啟動HBM9033的臨床試驗保檐。
2.7 YL221和YL222:授權給復宏漢霖生物
2022年12月,宜聯(lián)生物與復宏漢霖生物達成合作授權協(xié)議崔梗。根據(jù)該協(xié)議約定夜只,復宏漢霖將獲得宜聯(lián)生物基于其自主知識產權的 ADC平臺技術針對兩個指定靶點(EGFR和PD-L1)的獨家、可分許可的權利蒜魄,以供復宏漢霖于許可區(qū)域內(即全球范圍)發(fā)現(xiàn)扔亥、研究、開發(fā)盯辅、生產摹跑、使用和商業(yè)化待開發(fā)ADC產品。宜聯(lián)生物將獲得預付款趴鹰、開發(fā)胚砰、注冊和銷售里程碑付款、分級特許權使用費纠沉,以及依據(jù)開發(fā)階段的第三方分許可分成敬魏。
2023年10月27日,復宏漢霖宣布岔雾,其與宜聯(lián)生物的合作開發(fā)的兩款ADC產品肠豺,包括靶向EGFR的新型ADC候選藥物注射用HLX42(YL221),及靶向PD-L1的新型ADC候選藥物注射用HLX43(YL222)扁钥,已經(jīng)同步獲得國家藥品監(jiān)督管理局(NMPA)臨床試驗批準俐粪,擬用于晚期/轉移性實體瘤的治療。
寫在最后
宜聯(lián)生物雖成立不久捐煤,但憑借其獨有的TMALIN技術平臺深受國內外藥企的青睞褪秀,包括再鼎醫(yī)藥、復宏漢霖薛训、BioNTech和羅氏等媒吗,共同合作開發(fā)多款產品。
目前其在研管線中乙埃,只有YL201和YL205還沒有授權出讓闸英,分別處于臨床2期和IND申報階段,都顯示出很好的活性介袜,此次宜聯(lián)生物與BioNTech達成的18億美元交易甫何,可能包括這兩款產品出吹。
參考文獻
1.https://cn.medilinkthera.com/technology#ny-nav
2.https://cn.medilinkthera.com/pipeline-details/3
3.Abstract 563: Preclinical development of YL202, a novel HER3-targeting antibody-drug conjugate (ADC) with novel DNA topoisomerase I inhibitor for treatment of solid tumors
4.YL202/BNT326, a HER3-targeted ADC, in patients with locally advanced or metastatic non-small cell lung cancer and breast cancer: Preliminary results from a first-in-human phase I trial.
5.Preclinical development of YL205, a novel NaPi2b-targeting antibody-drug conjugate (ADC) with novel topoisomerase I inhibitor-based linker-payload for treatment of solid tumors
6.Abstract 2615: Preclinical development of a next generation antibody drug conjugate (ADC) targeting cMET for treatment of solid tumors

 產業(yè)資訊
產業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 64
64

 產業(yè)資訊
產業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 66
66

 產業(yè)資訊
產業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 67
67