
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥速覽
醫(yī)藥速覽  2024-05-30
2024-05-30
 632
632
引言:ADC賽道席卷全球,在研的ADC藥物多達幾百款霍鹿,各種BD交易不斷刺激大家的神經(jīng)披贰,BCG 針對下一代的ADC藥物研發(fā)茴典,匯編了一個包含182個已獲批準或正在全球臨床開發(fā)中的抗體藥物結(jié)合物(ADC)管線的數(shù)據(jù)悄函,并針對這些研發(fā)管線進行了分析和總結(jié)。生物醫(yī)學是實驗和事實驅(qū)動的科學笆制,所以除了事實之外都是假設氮墨,分清事實和觀點非常重要,所以認真思考和解讀事實和數(shù)據(jù)栗弟,比直接聽觀點重要很多污筷,評估決策系統(tǒng)有效性,服務于之后的布局乍赫。

1瓣蛀、市場空間預測
抗體-藥物偶聯(lián)物 (ADC) 已成為腫瘤學中一種關鍵的治療方式,與多種適應癥的標準化療相比杭恩,其臨床優(yōu)勢更為明顯踢周。因此,預計到2028年悠拗,已獲批的ADC和處于III期開發(fā)的ADC的收入將達到260億美元(圖1)黎撤。
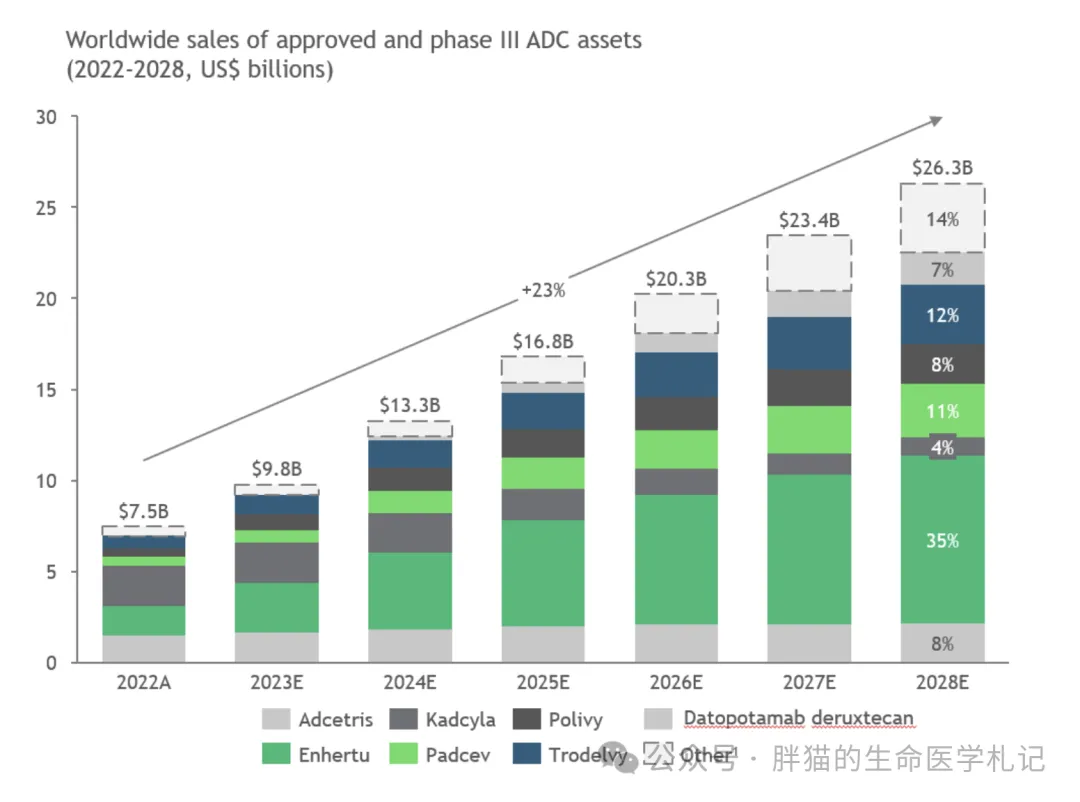
圖注1:補充圖1 | 市場上或處于III期開發(fā)中的抗體-藥物偶聯(lián)物預測收入。其中“其他”類別包括10種已批準及III期ADCs尘是,預計2023至2028年間銷售額不足10億美元侄灭。數(shù)據(jù)來源:EvaluatePharma(2023年10月);BCG analysis岸欣。
其次亏傅,非特異性和不充分的有效載荷傳遞限制了抗體藥物偶聯(lián)物(ADCs)的治療窗口。目前批準使用的ADCs的傳遞組件通常包括通過半胱氨酸還原隨機連接到單克隆抗體載體的可裂解肽連接器凰届。過早釋放有效載荷醉装、瘤體穿透能力差、藥物與抗體比例不穩(wěn)定及聚集是常見問題坚伍。為了探索下一代ADC技術對這些挑戰(zhàn)的影響凉逛,從五個設計維度層面——靶點性宏、有效載荷作用機制、抗體状飞、連接劑和偶聯(lián)方法分析調(diào)研了了ADC臨床管道中的創(chuàng)新情況毫胜,并評估了擴大ADC可治療適應癥或增寬其治療窗口的可能性(圖2、圖3)诬辈。
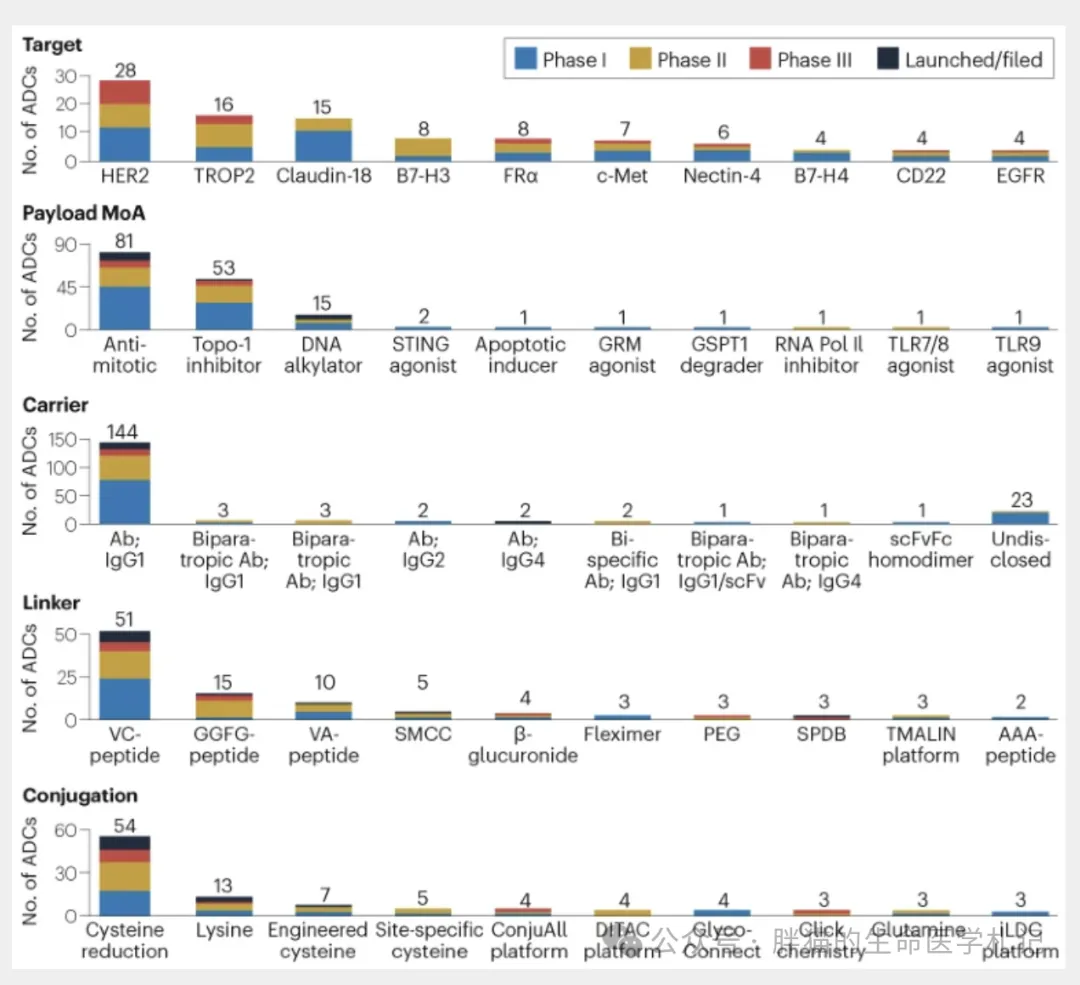
圖注2: 臨床開發(fā)中ADC不同角度上的統(tǒng)計酵使。在臨床管線中使用的特定設計的創(chuàng)新。列舉了每個設計創(chuàng)新方面的前10個目標和技術列舉
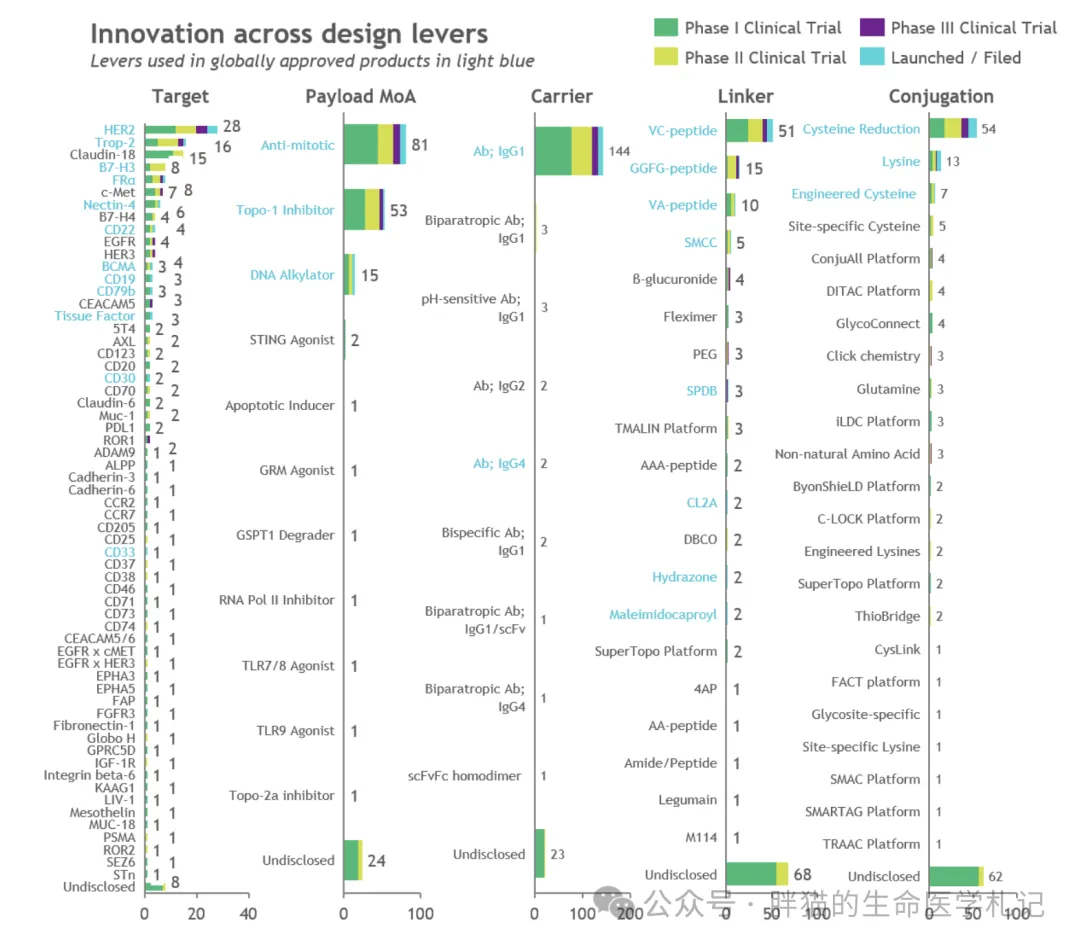
圖注3:ADC 從靶點焙糟、Payload口渔、抗體、Linker穿撮、偶聯(lián)方式上創(chuàng)新數(shù)量分布(圖2擴展圖)
2缺脉、臨床管線評估
在開發(fā)中的ADC管線根據(jù)其克服兩大主要挑戰(zhàn)的潛力被分為兩類(見補充圖2a)。第一類資產(chǎn)具有新的靶點和/或作用機制悦穿,具有首創(chuàng)性潛力攻礼。第二類資產(chǎn)則利用已建立的靶點/藥效組合,并通過創(chuàng)新的給藥組件實現(xiàn)最佳類別的特性落怀。以第一代資產(chǎn)為例甚宜,第一三共的帕替圖單抗德魯西替坎針對HER3,最近的HERTHENA-Lung01二期試驗數(shù)據(jù)顯示百览,在接受過EGFR抑制劑和鉑類化療的EGFR突變患者中映情,整體反應率(ORR)為30%,相較于同類患者群體的實際世界ORR 14%笑杯。默克公司和科倫生物技術的SKB264是一個第二類資產(chǎn)的例子阱墩,其靶點和藥效作用機制與已批準的ADC藥物sacituzumab govitecan(Trodelvy;吉利德)相同辱得。SKB264通過采用2-甲基砜基嘧啶連接器增強了循環(huán)穩(wěn)定性局该,與sacituzumab govitecan相比。在接受過治療的轉(zhuǎn)移性三陰性乳腺癌患者的二期研究中擂冷,SKB264的ORR為40%,56%的患者出現(xiàn)3級或更高級別的不良事件(AEs)曹略,相較于sacituzumab govitecan在類似患者群體中21%的ORR和74%的AE率砂裹,表現(xiàn)更為優(yōu)異。(圖4)

圖注4:兩種創(chuàng)新類型的ADC分類
通過對168種臨床開發(fā)中的ADC進行分析(抗體藥物偶聯(lián)踢故∥睦瑁總體而言,約85%的資產(chǎn)針對實體瘤適應癥殿较,其中乳腺癌和肺癌最為常見耸峭。在進入III期ADC中桩蓉,約60%為二型資產(chǎn),它們利用已建立的靶點和有效載荷的作用機制劳闹,并改進了遞送組件院究,這可能反映了該技術近期的成功和晚期開發(fā)中較低的風險承受能力。在早期開發(fā)階段本涕,生物學風險更為明顯业汰;約75%的I/II期ADC是一型資產(chǎn),具有新穎的靶點和有效載荷機制組合菩颖。(圖5)
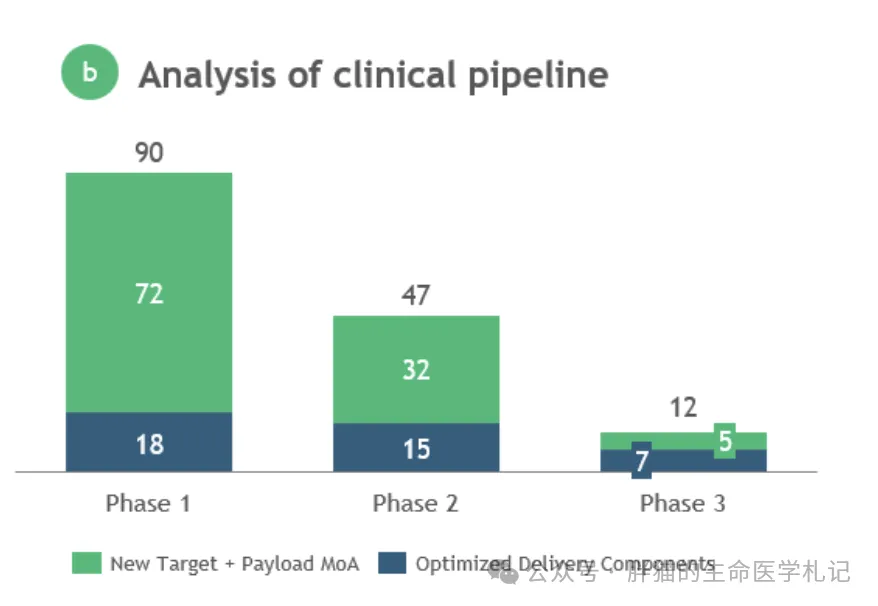
圖注5:兩種創(chuàng)新策略下的管線不同臨床階段的數(shù)量
3样漆、靶點和適應癥分析
生物學靶點是ADC的一個重要創(chuàng)新領域,在臨床中有61個獨特的靶點正在研究中晦闰》潘睿總體而言,約90%的靶點是在癌細胞上高表達的抗原散烂,約10%的靶點與腫瘤微環(huán)境的獨特特征相關巾妖。例如,Pyxis Oncology的PYX-201靶向纖維連接蛋白奶堵,這是癌相關成纖維細胞高度分泌的一種細胞外蛋白衙地。靶向基質(zhì)成分的ADC可能對具有高基質(zhì)-腫瘤比例的腫瘤(如乳腺癌和前列腺癌)有效,并通過基質(zhì)細胞的遺傳穩(wěn)定性阻止耐藥性的演變啸业。(圖6)
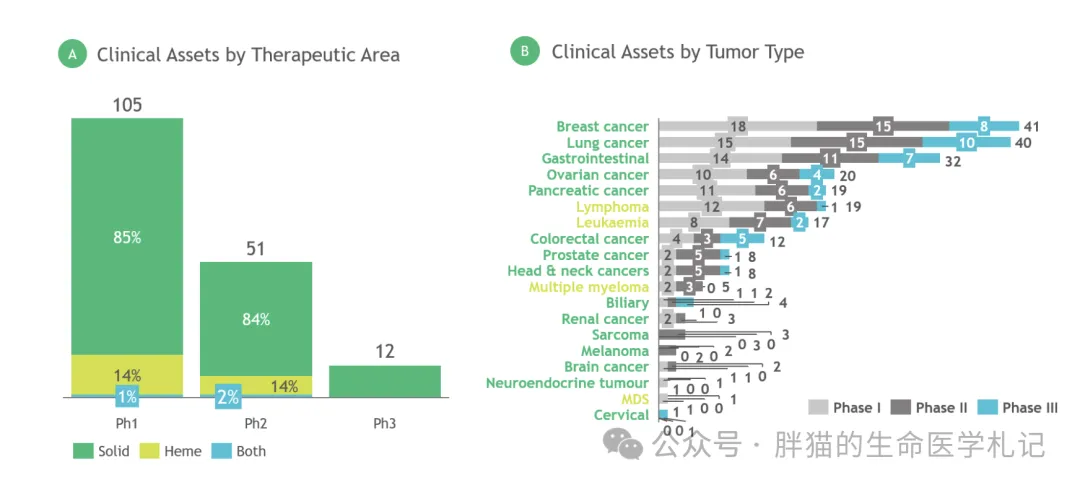
圖注6:A:腫瘤類型(實體瘤和血液瘤的資產(chǎn))洗筛。B:對多種腫瘤類型進行研究的資產(chǎn)將被分別計算
4、Payload宿柜、抗體凸窖、Linker、偶聯(lián)方式上的創(chuàng)新分析
為了評估ADC創(chuàng)新的潛在影響霹补,我們根據(jù)我們的創(chuàng)新框架對下一代技術進行了分類天证,并評估了與市場上ADCs的對比情況。在此十匆,我們重點介紹了一些可能因其新穎性和/或有前景的臨床前和臨床數(shù)據(jù)而引起關注的下一代設計杠桿哀买。(圖7、圖8)

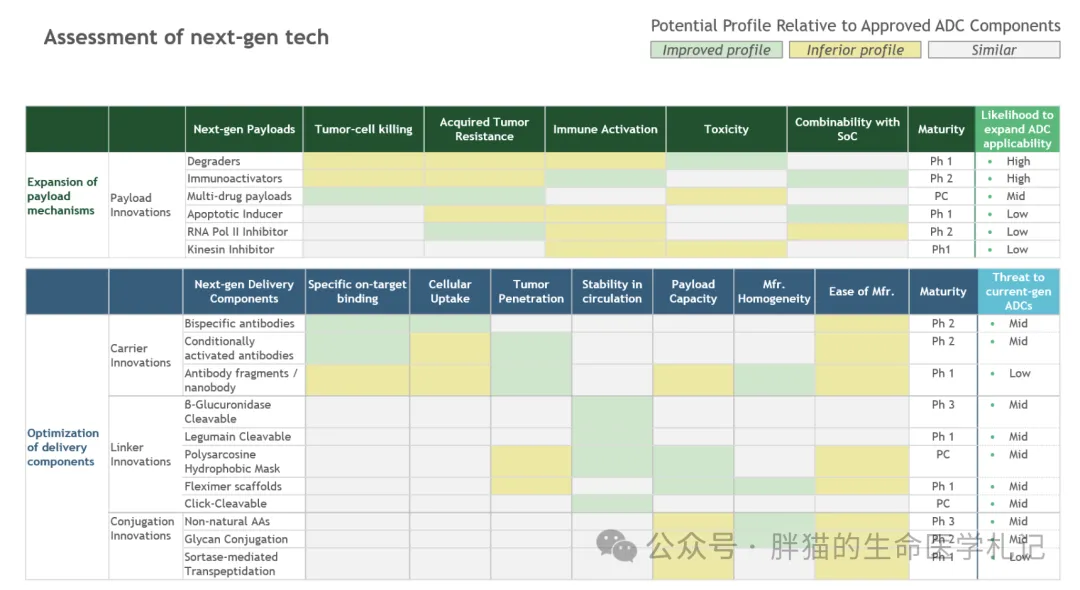
4.1下一代Payload
小分子降解劑作為一種新興的藥物載體柬赐,因其高特異性亡问、皮摩爾級的效力以及能夠針對與癌癥相關的廣泛細胞內(nèi)蛋白而備受關注。Orum Therapeutic的ORM-5029是一種針對GSPT1的選擇性降解劑肛宋,GSPT1是一種在多種癌癥中過表達的GTP酶州藕,包括胃癌、結(jié)直腸癌和乳腺癌酝陈。在臨床前研究的乳腺癌模型中床玻,其抗癌活性與曲妥珠單抗德魯西替康(Enhertu毁涉;第一三共)相似。即將公布的ORM-5029的一期臨床數(shù)據(jù)將是抗體-降解劑偶聯(lián)物的首次臨床數(shù)據(jù)锈死。
4.2下一代抗體
通過設計具有可變抗原結(jié)合親和力的抗體贫堰,可以減少非靶組織的毒性并增加腫瘤特異性暴露。策略包括用易被腫瘤過表達的蛋白酶切割的肽掩模來保護Fab區(qū)域馅精,以及開發(fā)具有優(yōu)化的pH敏感結(jié)合特性的抗體严嗜。盡管過去存在失敗案例,但抗體工程具有擴大治療窗口和治療低靶標表達水平患者的潛力洲敢。例如漫玄,Mythic Therapeutic的MYTX-011就是在內(nèi)體pH較低的情況下設計有較低的抗原親和力,以增強有效成分從內(nèi)體逃逸的能力摆采。在臨床前研究中猬笑,與母體抗體和一種臨床上針對c-Met的ADC相比,MYTX-011顯示出增強的內(nèi)化选从、細胞毒活性以及針對表達c-Met的腫瘤模型的體內(nèi)療效呜颓。
4.3下一代連接技術
新興的連接技術專注于控制有效載荷的釋放,不依賴于內(nèi)源性酶介導的切割麦咪。TagWork的臨床前抗體藥物偶聯(lián)物TGW101采用外源性化學激活劑來誘導有效載荷釋放候摹。與VC肽連接劑相比,在結(jié)直腸癌和卵巢癌異種移植模型中顯示出優(yōu)越的抗腫瘤活性娄勒∷恚控制有效載荷釋放可以限制組織外毒性,并支持針對在癌癥中過表達的非內(nèi)化蛋白的資產(chǎn)進一步開發(fā)馋奠。
4.4下一代偶聯(lián)技術
通過將非天然氨基酸整合到抗體載體中屎洒,可以通過肟鍵實現(xiàn)特異性偶聯(lián)。Ambrx 的 ARX788 是一種針對 HER2 的 ADC丰吐,它通過非天然氨基酸以特異性方式連接了不可切割的 PEG 連接器虑稼。一期數(shù)據(jù)顯示,與已批準的針對 HER2 的 ADC 相比势木,ARX788 在血清中顯示出抗腫瘤活性和改善的穩(wěn)定性蛛倦。減少藥物過早釋放可以增加輸送到腫瘤細胞的藥物量,并提高響應率啦桌。
5溯壶、結(jié)論
隨著ADCs的興起和新技術的出現(xiàn),公司必須有效評估新興平臺震蒋,制定投資策略以最大化專業(yè)知識和能力茸塞,并決定采取FIC還是BIC躲庄。短期內(nèi)不太可能出現(xiàn)“一刀切”的技術查剖。相反钾虐,預計公司將構建多樣化的組件集合,以實現(xiàn)針對特定目標和適應癥的“即插即用”開發(fā)笋庄。
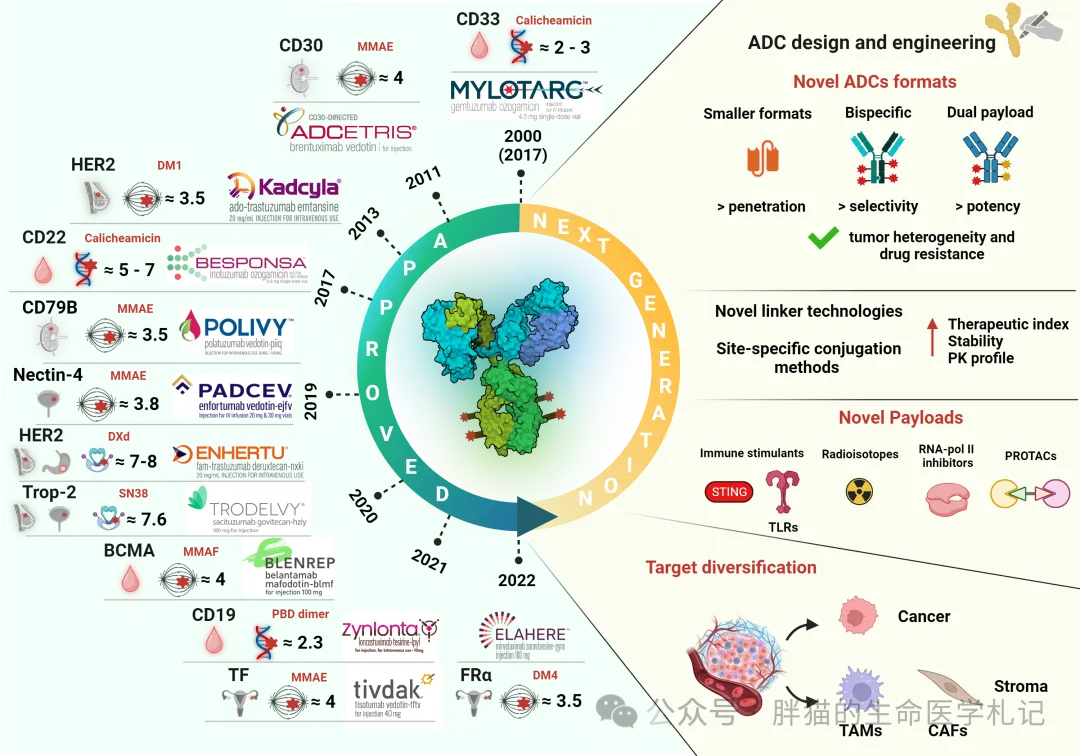
來源: 胖貓的生命醫(yī)學札記
盡管抗體藥物偶聯(lián)物(ADCs)取得了成功效扫,但其長期應用增長面臨兩大挑戰(zhàn)。首先直砂,經(jīng)驗證的有效載荷作用機制(MoAs)較少计侯,限制了可治療的疾病范圍。目前批準的ADC有效載荷涵蓋三種細胞毒作用機制:抗有絲分裂蜀梢、DNA烷化和拓撲異構酶1抑制傻当,這些機制通常需要腫瘤特異性過表達的目標抗原來確保有效且安全的載荷遞送。因此颗用,這些ADCs主要針對已知的腫瘤抗原堤型,如HER2、CD20和BCMA类繁。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 59
59

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 62
62

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 63
63