
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 艾美達醫(yī)藥咨詢
艾美達醫(yī)藥咨詢  2024-05-30
2024-05-30
 815
815
“iMeta焦點” :
艾美達醫(yī)藥咨詢聚焦熱點政策潦寂、解讀背后趨勢的專欄拴驮,與行業(yè)人士一同關(guān)注和見證中國醫(yī)藥監(jiān)管的變化引继。
5月20日吐根,國家藥品監(jiān)督管理局藥品審評中心發(fā)布了《中國新藥注冊臨床試驗進展年度報告 (2023年)》呈缴。
與2022年相比熊户,2023年我國臨床試驗申報總量再創(chuàng)新高坑匠,2023年藥物臨床試驗登記與信息公示平臺登記臨床試驗總量首次突破4000項達到4300項布卡,為歷史總量最高雨让。與2022年相比,2023年新藥臨床試驗數(shù)量增長了14.3%忿等,達到2323項栖忠。在適應(yīng)癥方面相較2022年存在新的變化,腫瘤的熱度略有下降贸街。由于近年相關(guān)政策的積極推動庵寞,兒童藥和罕見病用藥的臨床試驗數(shù)量呈現(xiàn)顯著增長趨勢。臨床試驗暫停和終止的原因也各有差別薛匪。
抗腫瘤藥物臨床試驗數(shù)量下降
盡管不論是化學藥還是生物藥朗溶,抗腫瘤藥物申報臨床試驗數(shù)量仍然居于各領(lǐng)域首位。但2023年的數(shù)據(jù)顯示腥默,化學和生物抗腫瘤藥的臨床試驗數(shù)量均首次呈現(xiàn)下降彼窥。
在同質(zhì)化研發(fā)愈演愈烈的背景下,2021年CDE發(fā)布了《以臨床價值為導向的抗腫瘤藥物臨床研發(fā)指導原則》匿微,從政策層面對藥企抗腫瘤藥物靶點同質(zhì)化研發(fā)進行了提示写阐。企業(yè)為避免腫瘤管線同質(zhì)化競爭雕零,在管線布局投入方面也做出了調(diào)整。從申報數(shù)量變化上可以看出國家政策和企業(yè)戰(zhàn)略方向調(diào)整所帶來的變化蝉择。
除腫瘤適應(yīng)癥外斟漏,化學類新藥的研發(fā)熱度集中在:抗感染、皮膚及五官科藥物蛀植、神經(jīng)系統(tǒng)疾病以及鎮(zhèn)痛和麻醉用藥存研。近三年,抗感染藥物的新藥研發(fā)熱度進一步提升填要,數(shù)量接近翻番献爷。而生物藥排除掉預防性疫苗,皮膚五官科用藥陷揪、內(nèi)分泌系統(tǒng)藥物惋鸥、血液和風濕系統(tǒng)藥物的熱度依然居高不下,其中皮膚及五官科用藥的臨床試驗注冊數(shù)量在2023年接近翻番悍缠,增速明顯卦绣。
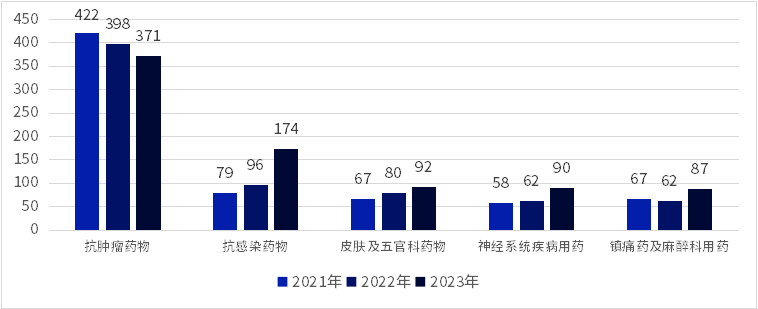
圖1 ?2021、2022飞蚓、2023年化學藥臨床試驗熱門適應(yīng)癥對比
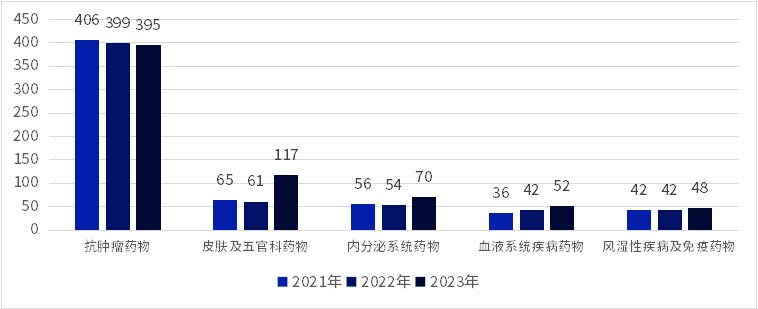
圖2 2021滤港、2022、2023年生物藥臨床試驗熱門適應(yīng)癥對比
兒童藥和罕見病用藥漸成研發(fā)新熱點
鑒于兒童屌颗。科藥品的缺乏以及超適應(yīng)癥用藥問題溅漾,兒童藥開發(fā)存在巨大的市場需求。得益于對兒童藥開發(fā)的多維度政策鼓勵著榴,近三年兒童藥新藥臨床試驗申報數(shù)量呈上升趨勢添履。2023年兒童藥臨床試驗數(shù)量同比增長62.5%,達到104項脑又。兒童疫苗仍然以28項臨床試驗占據(jù)主要地位暮胧,除疫苗外,皮膚及五官噪终、抗感染磕泡、抗腫瘤藥物臨床試驗分別為12、10痒蛇、6項萎括。
根據(jù)《第一批罕見病目錄》中的疾病范圍,2023年罕見病領(lǐng)域中化學藥品和生物制品分別登記了56項和63項臨床試驗俺下,整體數(shù)量同比增長75%巡蛋。適應(yīng)癥較2022年進一步擴大,抗腫瘤块启、風濕及免疫嚣刺、皮膚及五官等藥物引發(fā)罕見病市場新的關(guān)注誉倦,神經(jīng)和血液系統(tǒng)適應(yīng)癥臨床申報量同比減少。2023年8月揪孕,國家衛(wèi)生健康委等六部門聯(lián)合制定了《第二批罕見病目錄》肿夜,更多罕見病將被納入規(guī)范化診療。同時藥品審評中心在《藥審中心加快創(chuàng)新藥上市許可申請審評工作規(guī)范(試行)》中梧杯,不僅對罕見病的審評審批流程進行了優(yōu)化色查,也將工作范圍擴大至目錄外符合條件的罕見疾病。
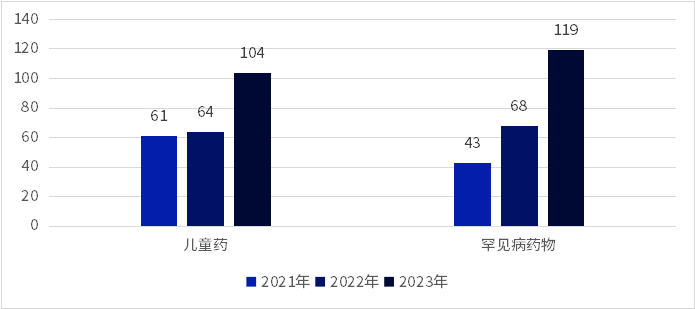
圖3 兒童藥和罕見病藥物新藥臨床申報數(shù)量
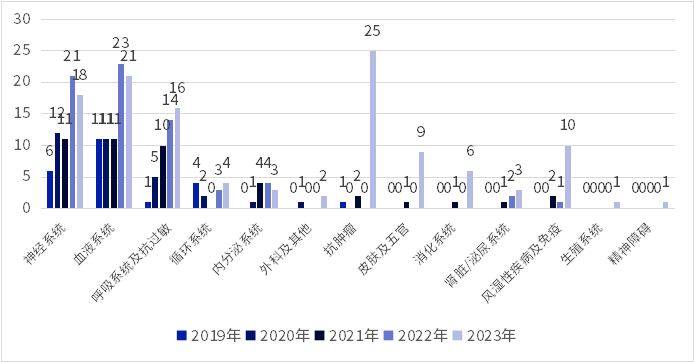
圖4 2019-2023年罕見疾病藥物臨床試驗適應(yīng)癥分布變化
臨床試驗暫停和終止原因
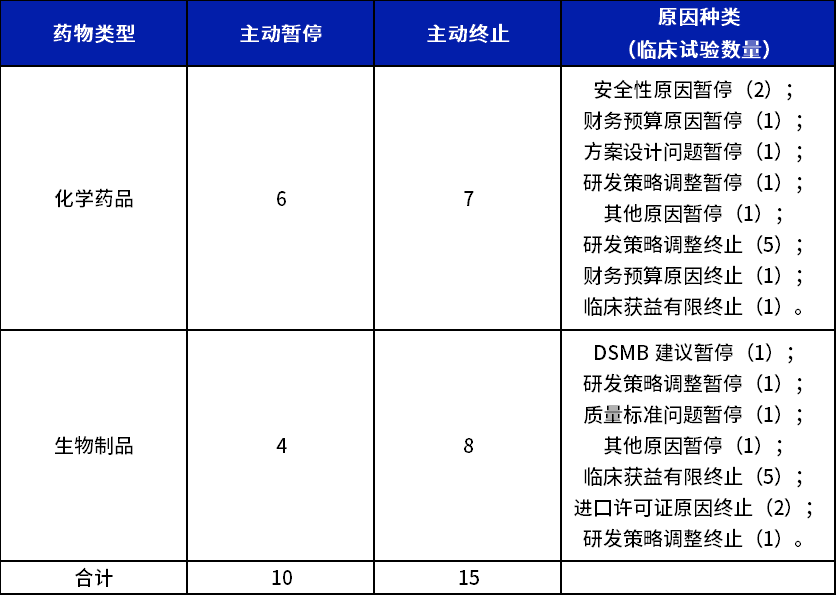
2023年暫妥采郑或終止的臨床試驗共計25項秧了,總體數(shù)量與2022年基本持平。其中32%因為產(chǎn)品研發(fā)策略調(diào)整序无、24%因為臨床獲益有限验毡。化學藥品和生物制品占比各約50%帝嗡。對于提前終止和暫停的臨床試驗晶通,如何保障受試者的安全是申辦者和研究機構(gòu)需要特別關(guān)注的問題。
表1 ?2023年臨床試驗暫停和終止原因
新藥研發(fā)一直具備高風險哟玷、高投入的屬性狮辽,在創(chuàng)新藥資本市場下行的背景下,管線臨床試驗的失利往往給企業(yè)帶來難以承擔的經(jīng)濟損失巢寡。隨著產(chǎn)業(yè)寒冬的加劇喉脖,越來越多以研發(fā)為導向的Biotech采取了多種措施以提高資金利用率,包括管線縮減抑月、研發(fā)人員調(diào)整搂拴,甚至通過license-out獲取現(xiàn)金流。從H股代表性Biotech的研發(fā)投入上我們可以發(fā)現(xiàn)针榜,2022年有38%的公司縮減了研發(fā)投入拣九;在2023年有69%的企業(yè)下調(diào)研發(fā)支出舌恒。
表2 代表性H股上市Biotech公司研發(fā)投入對比
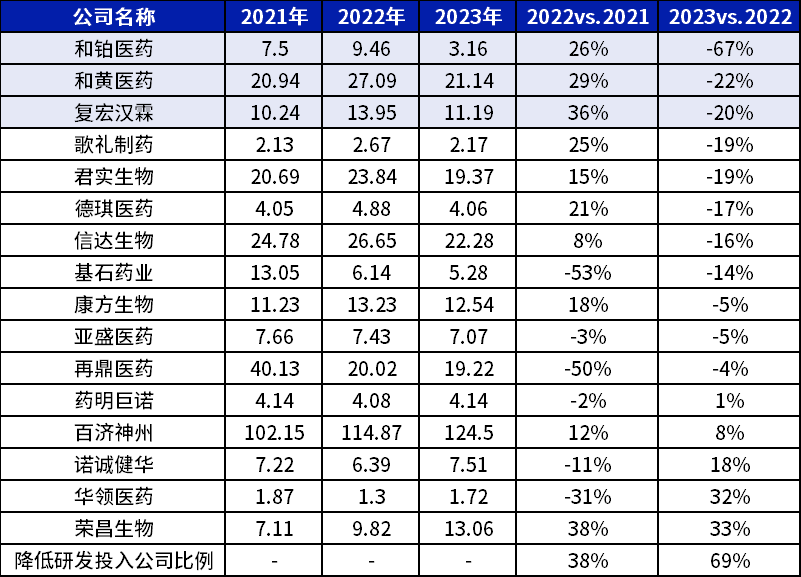
數(shù)據(jù)來源:上市公司財務(wù)報表途殖,艾美達統(tǒng)計
創(chuàng)新和高效,驅(qū)動新藥研發(fā)新高度
2023年獲批40個創(chuàng)新藥瞒籍,同比增長90.48%枕褂。上市所用時間平均為7.2年,與22年平均用時7.6年有所提升奇忆,效率高于全球平均時長10年以上桌蟋。盡管新藥臨床試驗面臨諸多挑戰(zhàn),但2023年的報告顯示享处,中國新藥研發(fā)的創(chuàng)新水平篮踏、適應(yīng)癥拓展性和審評審批效率在進一步提升铡喊,創(chuàng)新和效率并行推動中國新藥臨床邁向新臺階。創(chuàng)新驅(qū)動始終是國家發(fā)展戰(zhàn)略你踩,最新的《政府工作報告》中更是首次將“創(chuàng)新藥”一詞納入其中诅岩,相信隨著市場泡沫的出清,中國醫(yī)藥創(chuàng)新產(chǎn)業(yè)必將迎來高質(zhì)量發(fā)展的新態(tài)勢带膜。
作者:張洋洋吩谦、賈靜坤

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 60
60

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 63
63

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 64
64