
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥筆記
醫(yī)藥筆記  2024-05-31
2024-05-31
 555
555
2024年5月31日至6月4日掐股,2024年美國臨床腫瘤學會(ASCO)年會將在美國伊利諾伊州芝加哥市舉行,科倫博泰SKB264用于治療局部復發(fā)性或轉移性三陰乳腺癌三期臨床OptiTROP-Breast01的最新數(shù)據(jù)浪规,將于美國當?shù)貢r間6月2日上午09:45-11:45在“Clinical Science Symposium-Next Generation Antibody-Drug Conjugates估宏, Ther Revolution Continues” Session進行口頭報告蚀之,Session類型為clinical sicence Symposium答艘,為special session滤馍。日前贸典,該報告的摘要數(shù)據(jù)已經(jīng)公布拓劝。

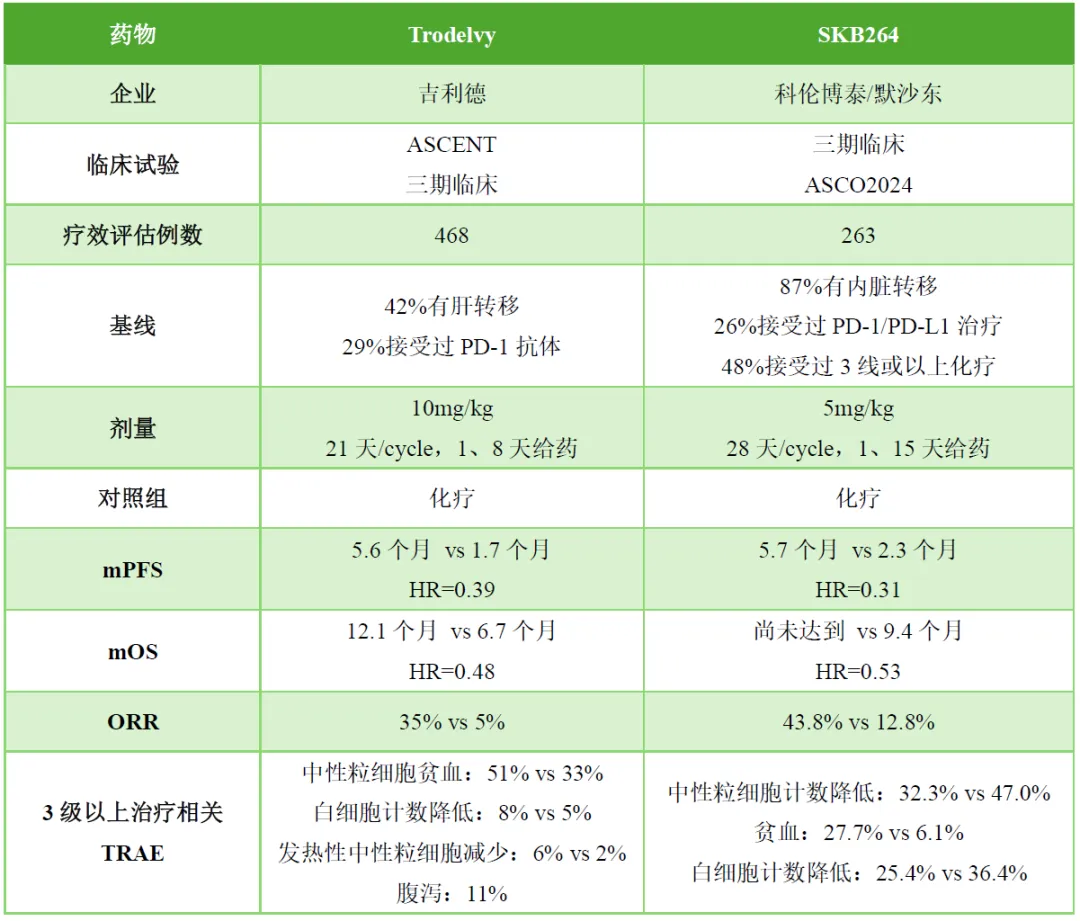
該三期臨床OptiTROP-Breast01入組263例患者雏逾,130例接受SKB264治療,133例接受化療治療郑临∑懿患者中位年齡為51歲价脾,87%存在內(nèi)臟轉移;26%既往接受過PD-1/PD-L1抑制劑治療笛匙;48%在晚期階段接受過三線或以上的化療侨把。根據(jù)期中分析(數(shù)據(jù)截止日期:2023年6月21日),已達到無進展生存期(PFS)主要終點妹孙,相比化療秋柄,不論Trop2表達水平如何,疾病進展或死亡的風險降低69%(HR-0.31)肢姜。
療效方面主渤,SKB264治療組mPFS為5.7個月,化療對照組mPFS為2.3個月驰闺,6個月PFS率分別為43.4%瘪叉、11.1%。對于OS首次期中分析(截至2023年11月30日)呕豪,SKB264治療組相比化療對照組死亡風險降低47%(HR=0.53)药扒,化療mOS為9.4個月,SKB264治療組的mOS尚未達到糯档。SKB264治療組和化療對照組的ORR分為43.8%隙殴、12.8%。
安全性方面蜡幼,SKB264治療組和化療對照組的主要3級及以上副作用包括中性粒細胞計數(shù)降低(32.3%掷栋、47.0%)、貧血(27.7%嗓万、6.1%)邦鲫、白細胞計數(shù)降低(25.4%、36.4%)神汹。
與目前的臨床標準治療方案庆捺,吉利德Trop2 ADC或化療相比,SKB264都表現(xiàn)出顯著的優(yōu)勢慎冤。OptiTROP-Breast01試驗直接與化療標準療法頭對頭對照疼燥,mPFS延長3.4個月沧卢,疾病進展或死亡風險降低69%蚁堤,死亡風險降低47%。從響應率來看但狭,SKB264治療組ORR達到43.8%披诗,而化療組的ORR僅為12.8%,SKB264的ORR接近化療組的4倍立磁,成為首款ORR突破40%的Trop2 ADC呈队。相比于吉利德的Trop2 ADC(非頭對頭)剥槐,SKB264的給藥劑量和頻率更低,疾病進展或死亡風險降低幅度69%宪摧,高于Trodelvy的57%助潭,ORR也更高。因此连欲,SKB264的療效全面超越主流的標準方案打且,徹底打破了三陰乳腺癌二線治療的天花板,預計未來將成為該臨床場景的新標準椅损。安全性方面帘战,SKB264的整體副作用可管理,沒有需要特別關注的毒性吉挎。
在2023年第46屆美國圣安東尼奧乳腺癌研討會(SABCS)將于美國中部時間(CST)上斑永,科倫博泰生物亦以POSTER SPOTLIGHT PRESENTATION形式公布了SKB264(MK-2870)用于治療局部晚期或轉移性三陰性乳腺癌(TNBC)患者II期拓展研究臨床結果。
入組59例經(jīng)治的局部晚期或轉移性三陰性乳腺癌(TNBC)患者接受SKB264單藥治療氨固,中位隨訪時間22.8個月蛀埂。89.8% (53名)患者既往接受過3種及以上治療方案,27.1%(16名)患者既往接受過免疫治療解瀑,約一半的患者有肺轉移妇乏,肝轉移約占1/3△薮撸客觀緩解率(ORR)為42.4%肺素,其中有3例患者完全緩解(CR),疾病控制率(DCR)為76.3% 宇驾,中位持續(xù)緩解時間(mDoR)為11.5個月倍靡,中位無進展生存期 (mPFS)為5.7個月,中位總體生存期(mOS)長達16.8個月课舍,12個月和24個月OS率分別為65%和39.5%塌西,近40%的患者可生存超過2年。在TROP2高表達(H-score>200筝尾,n=32)的患者亞組中捡需,ORR為53.1%,mDoR為11.1個月筹淫,mPFS為5.8個月站辉,mOS尚未達到,而12個月及24個月OS率分別為65.3%及57.3%损姜。
對于晚期的三陰乳腺癌來說饰剥,臨床上仍然缺少更多、更好的治療選擇。三陰乳腺癌在研藥物中寺癌,ADC扮演重要角色雌褥。SKB264在復發(fā)性三陰乳腺癌的三期臨床中已經(jīng)證明其卓越的臨床價值,并積極向前線拓展绅荒,包括合作伙伴默沙東已經(jīng)啟動的全球三期臨床MK-2870-012知祠,PD-1+SKB264聯(lián)合輔助治療既往經(jīng)PD-1+化療新輔助治療術后未達到pCR的三陰乳腺癌「窝颍科倫博泰則在推進主一項評估SKB2664在中國用于一線治療不可手術切除的局部晚期雕零、復發(fā)或轉移性PD-L1陰性TNBC患者的三期臨床。
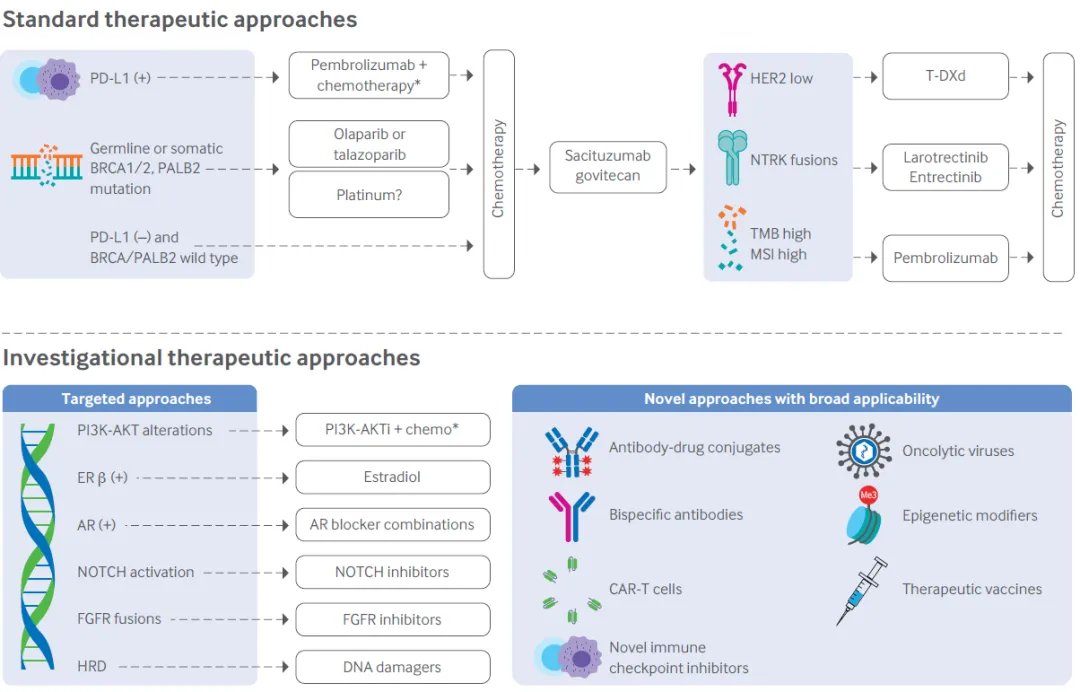
根據(jù)阿斯利康公布的流行病學和藥物應用趨勢分析數(shù)據(jù)蝉择,預計未來G7國家三陰乳腺癌使用ADC治療的峰值人數(shù)將接近50000例/年斟漏,包括近30000例前線治療和近20000例復發(fā)性的后線治療患者。

總結
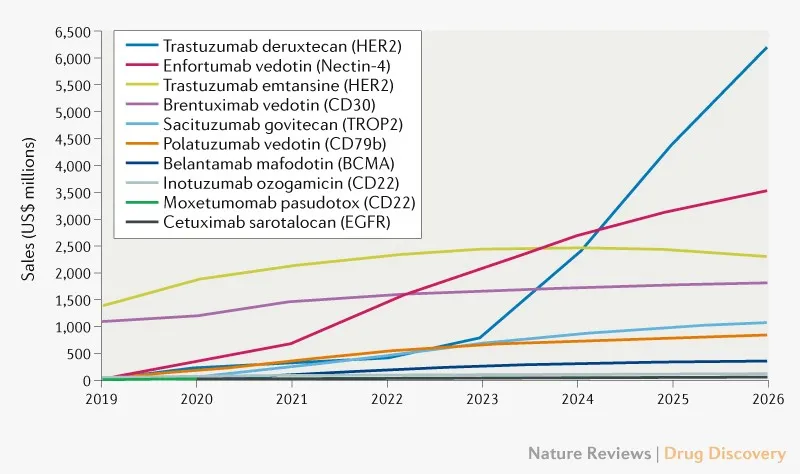
ADC藥物正在系統(tǒng)性地替代化療蛀植,應用場景日益廣闊存研。根據(jù)波士頓咨詢2021年在Nature Reviews Drug Discovery發(fā)表的分析文章,預計2026年ADC藥物市場規(guī)模將達到160億美元填要,現(xiàn)在看來這一預測明顯偏保守苦厅。2023年全球ADC藥物市場規(guī)模已經(jīng)達到106億美元,今年一季度32億美元关串。對于吉利德的Trop2 ADC拧廊,該文章預測2026年銷售額11億美元,實際上2023年即達到10.6億美元晋修,今年一季度銷售額3億美元吧碾,仍然保持高速增長。
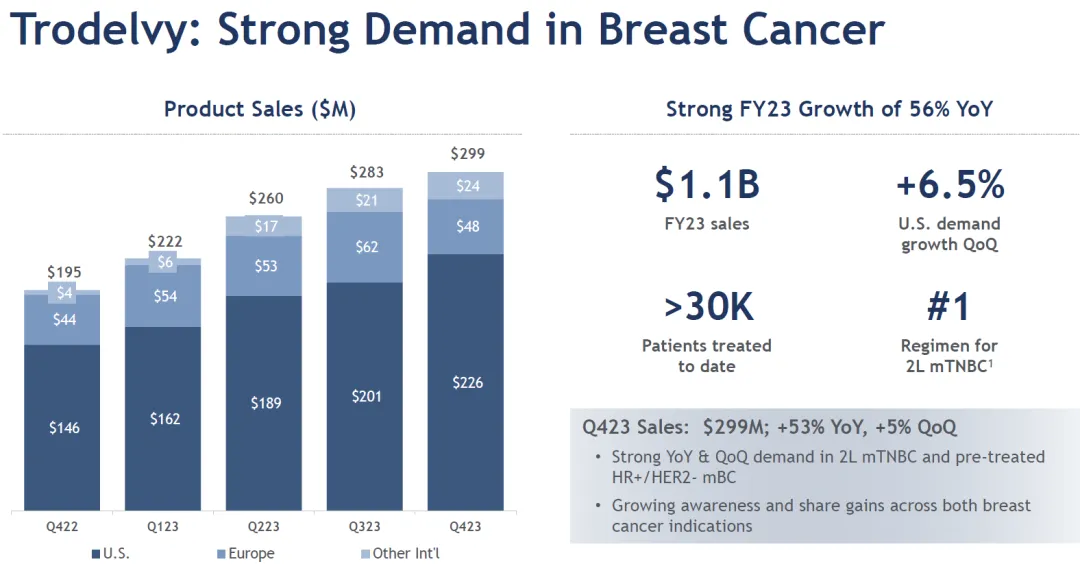
值得一提的是墓卦,Trodelvy超預期的銷售額還是在獲批適應癥比較有限的前提下實現(xiàn)的倦春,包括2020年4月獲批的三陰乳腺癌、2021年4月獲批的尿路上皮癌落剪、2023年2月獲批的HR+/HER2-乳腺癌睁本。Trodelvy目前在三陰乳腺癌二線治療占據(jù)主導地位,且處于快速增長階段(季度環(huán)比強勁增長)忠怖,換言之其在2023年的10.6億美元銷售額主要由三陰乳腺癌貢獻呢堰。
相比于Trodelvy,SKB264已經(jīng)在三期關鍵臨床中表現(xiàn)出更優(yōu)異的臨床療效凡泣,科倫博泰與默沙東同時積極向前線治療枉疼、更多瘤種快速拓展,預計將實現(xiàn)更大的商業(yè)價值噪终。默沙東從2023年10月開始磕泡,圍繞SKB264密集啟動9項全球三期臨床坑哥,覆蓋非小細胞肺癌痒蛇、子宮內(nèi)膜癌萎括、乳腺癌、胃癌等多個瘤種和不同臨床應用場景俺下⊙驳埃科倫博泰作為國內(nèi)ADC的標桿性企業(yè),在SKB264之后预铁,還有Nectin-4 ADC嚣赤、Claudin18.2 ADC等更多具有競爭力的ADC管線在積極推進中,期待其后續(xù)臨床進展簸翠。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 60
60

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 63
63

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 64
64