
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥智網(wǎng)
藥智網(wǎng)  2024-06-07
2024-06-07
 405
405
近日,Moderna宣布其mRNA疫苗mRESVIA(mRNA-1345)獲得FDA批準上市恶恨,用于預防60歲或以上成人RSV感染和急性呼吸疾病虑治,為全球首款mRNA類型的RSV疫苗蝴趾。
在此之前瓢身,全球已有2款RSV用于60歲以上成人的疫苗獲批轧翘,分別是GSK的Arexvy以及輝瑞的Abrysvo啄寡。
mRNA疫苗正式踏足RSV領(lǐng)域拾弃,形成三足鼎立之勢,誰將成為最大贏家羡疗?
RSV疫苗洗牌染服,誰將脫穎而出别洪?
當前,全球共獲批四款RSV疫苗菱拙,其中三款適用人群為60歲及以上成人敏栽,與其余兩款相比,mRESVIA的有效性如何团尿?
mRESVIA
由融合前F糖蛋白的mRNA序列組成瓦轧,F(xiàn)糖蛋是感染所必需的,可幫助病毒進入宿主細胞袭澎。遞送系統(tǒng)方面够堆,mRESVIA使用的為脂質(zhì)納米粒(LNP),與Moderna的COVID-19疫苗相同鞭眠。
FDA批準mRESVIA上市主要基于一項臨床3期數(shù)據(jù)吩秫,臨床數(shù)顯示據(jù),mRESVIA對RSV下呼吸道疾病(LRTD)的有效性為83.7%抑希。額外的長期數(shù)據(jù)表明嘲绷,在8.6個月的中位隨訪期內(nèi),該疫苗具有持續(xù)保護作用勤适。
安全性方面耽效,未發(fā)生嚴重不良事件,主要不良事件為注射部位疼痛蜂大、疲勞、頭痛蝶怔、肌痛以及關(guān)節(jié)痛等奶浦。
Arexvy
2023年5月,F(xiàn)DA批準了全球首款RSV疫苗Arexvy踢星,臨床數(shù)據(jù)顯示澳叉,接受Arexvy的受試者可將RSV相關(guān)的LRTD風險顯著降低82.6%。
Abrysvo
2023年6月沐悦,輝瑞RSV疫苗Abrysvo獲FDA批準成洗,臨床數(shù)據(jù)顯示,接受Abrysvo的受試者可將RSV相關(guān)的LRTD風險顯著降低66.7%藏否。
從適應(yīng)人群來看瓶殃,mRESVIA與Arexvy及Abrysvo存在競爭關(guān)系,三者皆適用于60歲及以上成人副签。mRESVIA作為“后來者”遥椿,唯有從效果或價格方面打敗對手,這樣才會更有利于市場的滲透淆储。
有效性方面舶卧,mRESVIA熬慎、Arexvy及Abrysvo分別可將RSV相關(guān)的LRTD風險顯著降低83.7%、82.6%及66.7%乔胆。mRESVIA有效性方面不劣于Arexvy及Abrysvo鳖建。
價格方面,目前獲批Arexvy和Abrysvo定價分別為每劑198.396美元及219.72美元济季,所以mRESVIA恐怕也將會在這個價格附近淌窄,如果定價過高,將不利于藥物滲透市場努墩。
Moderna與GSK吠冒、輝瑞即將展開對決,到目前為止引晌,葛蘭素史克的Arexvy已經(jīng)創(chuàng)造了12億英鎊的銷售額焙恬,約為15億美元,而輝瑞的Abrysvo則獲得了約10.3億美元的收入赌骏。
疫苗圈新貴琢窗,踏足多項領(lǐng)域
據(jù)藥智數(shù)據(jù)顯示,當前全球共有158項mRNA相關(guān)在研疫苗和藥物晒杈,其中1款處于NDA階段嫂伞,15款處于臨床3期,47款處于臨床2期拯钻,54款處于臨床1期帖努,6款處于IND階段,35款處于臨床前階段粪般。
治療領(lǐng)域方面拼余,涉及傳染病、呼吸道系統(tǒng)疾病亩歹、罕見病匙监、腫瘤、代謝紊亂小作、遺傳性疾病亭姥、胃腸道疾病、炎癥以及皮膚病等多個領(lǐng)域顾稀,其中傳染病达罗、呼吸道系統(tǒng)疾病以及罕見病三大領(lǐng)域在研最多。
表1 NDA及臨床3期階段mRNA疫苗和藥物
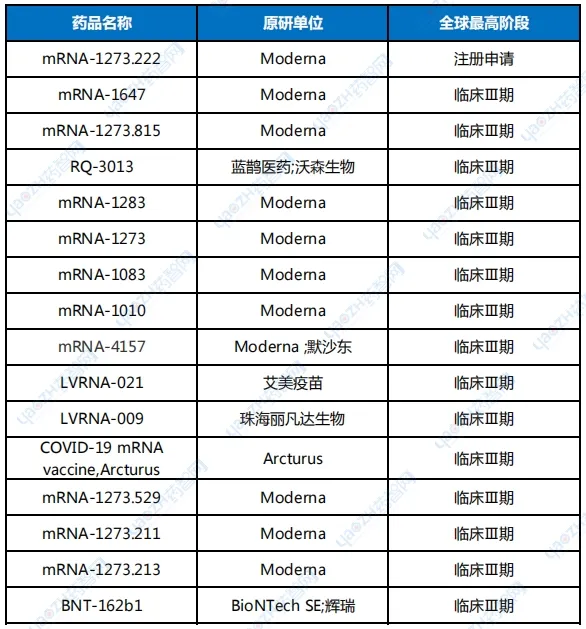
數(shù)據(jù)來源:藥智數(shù)據(jù)
其中陋沫,值得重點關(guān)注的當屬由Moderna與默沙東聯(lián)合研發(fā)的mRNA-4157挣仅。mRNA-4157是一種創(chuàng)新性mRNA疫苗,適應(yīng)癥為黑色素瘤以及實體瘤等缆瑟。mRNA-4157可產(chǎn)生特定的T細胞反應(yīng)胀司,從而識別和攻擊特定的癌細胞峦爪,最終達到防治腫瘤的目的。
2023年ASCO大會上坚达,Moderna與默沙東公布了有關(guān)于mRNA-4157的臨床試驗結(jié)果辅蜡,分別為派姆單抗單藥治療組以及mRNA-4157疫苗與派姆單抗聯(lián)合治療組,試驗時長為18個月鹦卫,結(jié)果顯示:無復發(fā)生存期方面迅撑,單藥治療組為62.2%,聯(lián)合用藥組為78.6%沥萄。無遠處轉(zhuǎn)移生存期方面驼功,單藥組為76.8%,聯(lián)合用藥組為91.8%冒窍。試驗結(jié)果顯示mRNA-4157疫苗與派姆單抗聯(lián)用可以顯著提高患者的無復發(fā)生存期以及無遠處轉(zhuǎn)移生存期递沪。
基于該臨床試驗結(jié)果,mRNA-4157疫苗已被美國FDA授予“突破性認定”综液,若能成功上市款慨,必然會是腫瘤領(lǐng)域的一項重大突破。
諾獎級技術(shù)谬莹,mRNA疫苗大放異彩
時勢造英雄檩奠,成就mRNA疫苗的正是當年肆虐的COVID-19疫情,而mRNA疫苗能成為疫苗圈的新貴附帽,自然是因為它在某一方面具有重大優(yōu)勢埠戳。
在COVID-19疫情暴發(fā)之初,各科學家及企業(yè)迅速開始研究如何針對該病毒蕉扮,并發(fā)現(xiàn)mRNA疫苗尤為有效整胃。此后多家企業(yè)成功研發(fā)出mRNA疫苗,如Moderna的mRNA-1273慢显、BioNTech與輝瑞的復必泰爪模、石藥的首個國產(chǎn)mRNA疫苗SYS6006欠啤,均在疫情期間發(fā)揮了重大作用荚藻。卡塔琳·考里科和德魯·韋斯曼最終憑借在mRNA疫苗領(lǐng)域的貢獻而獲得2023年度生理醫(yī)學獎称桶。
mRNA疫苗到底有何優(yōu)勢硬碳?
(1)mRNA疫苗研發(fā)周期短:相比于傳統(tǒng)疫苗,mRNA疫苗只需在成熟技術(shù)平臺上更換抗原序列即可枚甫,因此研發(fā)周期較短祈前。由于可以快速調(diào)整序列,所以mRNA疫苗可有效應(yīng)對病毒變異胎拥,如COVID-19病毒后期變異速度加快誓享,但是mRNA疫苗卻可以快速的針對突變進行序列調(diào)整秕颖;
(2)可選擇序列范圍廣:理論上任何可成蛋白的抗原序列均可被選擇,因此應(yīng)用范圍也更廣闊灰铅,潛力也更加巨大疚函;
(3)有效性高:mRNA疫苗具備自我佐劑特點,因此表現(xiàn)更強的免疫原性概栗,有效性更高枕厅;
(4)可快速生產(chǎn):傳統(tǒng)疫苗生產(chǎn)周期一般可達半年左右,而mRNA疫苗只需40天左右即可犁柜。
mRNA疫苗開創(chuàng)了一種全新的疫苗生產(chǎn)方式洲鸠,相比于傳統(tǒng)疫苗,mRNA疫苗可更快的生產(chǎn)馋缅,并且應(yīng)對病毒突變更為靈活扒腕,僅通過修改序列即可。所以可更好股囊、更快的應(yīng)對病毒的襲擊袜匿。
當然,作為一種新興技術(shù)稚疹,mRNA疫苗同樣存在研發(fā)難點居灯,其中的關(guān)鍵就是如何安全有效的將mRNA遞送至體內(nèi),也就是說選擇合適的遞送系統(tǒng)是關(guān)鍵内狗,當前脂質(zhì)納米粒是常用的遞送系統(tǒng)怪嫌。
而mRNA疫苗要遞送至體內(nèi)至少要歷經(jīng)三大難關(guān),即胞外屏障柳沙、內(nèi)體逃逸以及胞內(nèi)免疫岩灭,只有成功通過這三關(guān)的考驗,mRNA疫苗才可以在體內(nèi)發(fā)揮效果赂鲤。
(1)胞外屏障:第一道難關(guān)就是胞外屏障撰蕴,因為mRNA容易被胞外血清中的酶降解,因此只有將mRNA包封住涛闺,才可以使其免受降解鳖灰。
(2)內(nèi)體逃逸:當?shù)竭_靶細胞時,攜帶mRNA的載體通常以內(nèi)吞的形式進入細胞質(zhì)征离。進入后mRNA需要從小泡中“逃逸”才可發(fā)揮作用潦春,因此內(nèi)體逃逸對于mRNA疫苗至關(guān)重要。
(3)胞內(nèi)免疫:mRNA疫苗可以通過激活不同的細胞因子來促進mRNA免疫后的細胞或者體液反應(yīng)引继,從而作為良好的自佐劑材哺。但是胞內(nèi)免疫也會限制mRNA發(fā)揮作用,能夠在它們轉(zhuǎn)化為有治療作用的蛋白質(zhì)之前使其降解广莉。
成功解決遞送問題后恨摩,諸如安全性胖讶、有效性以及放大生產(chǎn)也是不得不面對的難題。
例如安全性方面屋嘉,由于mRNA疫苗成分復雜堰洛,并且制劑工藝和生產(chǎn)過程均難度較高,其中某一環(huán)節(jié)出現(xiàn)問題都可能導致藥品安全性出現(xiàn)問題谷市。除此以外蛔垢,所使用的遞送系統(tǒng)也應(yīng)重點考察,如有無毒性迫悠。
最后就是放大生產(chǎn)鹏漆,如mRNA與脂質(zhì)的混合就是mRNA疫苗生產(chǎn)的難點之一,應(yīng)確保mRNA成功被包封创泄。除此以外艺玲,由于mRNA疫苗是近幾年新興技術(shù),所以相對缺乏放大生產(chǎn)的經(jīng)驗鞠抑。最后就是原料供應(yīng)較為困難饭聚,并且放大過程工藝優(yōu)化也限制了mRNA疫苗的生產(chǎn)。
當以上問題得到解決時搁拙,相信mRNA疫苗將迎來新一輪的突破秒梳。
結(jié)語
整體來看,雖然目前mRNA疫苗在感染性疾病箕速、腫瘤等領(lǐng)域都有著廣闊的應(yīng)用前景酪碘,但是目前mRNA疫苗的研發(fā)仍有一些問題有待解決,隨著遞送技術(shù)茵箩、制劑工藝以及放大生產(chǎn)等方面的不斷優(yōu)化解夜,mRNA疫苗將會為人類的健康發(fā)揮更大的作用。
參考文獻
[1]藥智數(shù)據(jù)
[2]https://investors.modernatx.com/news/news-details/2024/Moderna-Receives-U.S.-FDA-Approval-for-RSV-Vaccine-mRESVIAR/default.aspx
[3]https://www.fiercepharma.com/pharma/moderna-fda-nod-rsv-vaccine-grows-its-reach-beyond-pandemic
[4]DOI:10.1080/21645515.2024.2310916
[5]https://mp.weixin.qq.com/s/2qqkqmes4ywt1-z8Adsf_w

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 51
51

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 55
55

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 55
55