 投資大會
投資大會
 中國醫(yī)藥創(chuàng)新與投資大會
中國醫(yī)藥創(chuàng)新與投資大會  2024-08-05
2024-08-05
 407
407

路演項(xiàng)目報(bào)名須知
路演報(bào)名請進(jìn)入官網(wǎng):http://cbiic.phirda.com/差按,點(diǎn)擊右上角【路演報(bào)名】,進(jìn)入路演報(bào)名注冊頁面喳逛。
由于文件上傳限制邮偎,請務(wù)必在PC端報(bào)名管跺。
普通參會將于8月中旬開放注冊,目前僅接受路演報(bào)名禾进。
路演項(xiàng)目類型
創(chuàng)新藥(含罕見病治療藥物)豁跑,如:全新分子實(shí)體;新機(jī)制、新靶點(diǎn)或按照藥品管理的全新相關(guān)療法;具有明顯臨床價(jià)值優(yōu)勢的改良型新藥(已有活性成份改構(gòu)或前體藥物命迈、新組合藥物以及新劑型贩绕、新用途和新給藥途徑藥物);
已經(jīng)獲批臨床、較同類產(chǎn)品具有顯著優(yōu)勢的第二類壶愤、第三類醫(yī)療器械或診斷試劑;
AI-生物醫(yī)藥項(xiàng)目;大數(shù)據(jù)-智慧醫(yī)療項(xiàng)目;醫(yī)藥數(shù)字化項(xiàng)目;
前沿技術(shù)領(lǐng)域:細(xì)胞與基因治療、核酸藥物等馏鹤;
企業(yè)/機(jī)構(gòu)宣講項(xiàng)目涮饱。
注:臨床數(shù)據(jù)全球首發(fā)專場原則上只接受上述第1類項(xiàng)目申報(bào)。
需要準(zhǔn)備材料
宣講題目(中英文);
路演項(xiàng)目簡介(中英文牵蠢,中文200~300字符常择,英文800~1200字符),項(xiàng)目審核通過后將體現(xiàn)在會議手冊中仓疯,請務(wù)必填寫準(zhǔn)確笆赤,并符合字?jǐn)?shù)要求;
項(xiàng)目情況詳細(xì)介紹:請?jiān)谧韵到y(tǒng)內(nèi)下載路演項(xiàng)目申報(bào)書模板,完整填報(bào)項(xiàng)目信息后上傳至注冊系統(tǒng)魂欺,信息僅用于專家審核粮唯,不公開,必須上傳;
路演現(xiàn)場演示文稿PPT虏绑,16:9模式(審核通過后需在11月20日00:00前上傳浇找,逾期系統(tǒng)關(guān)閉將無法提交,未上傳PPT將視為放棄路演)
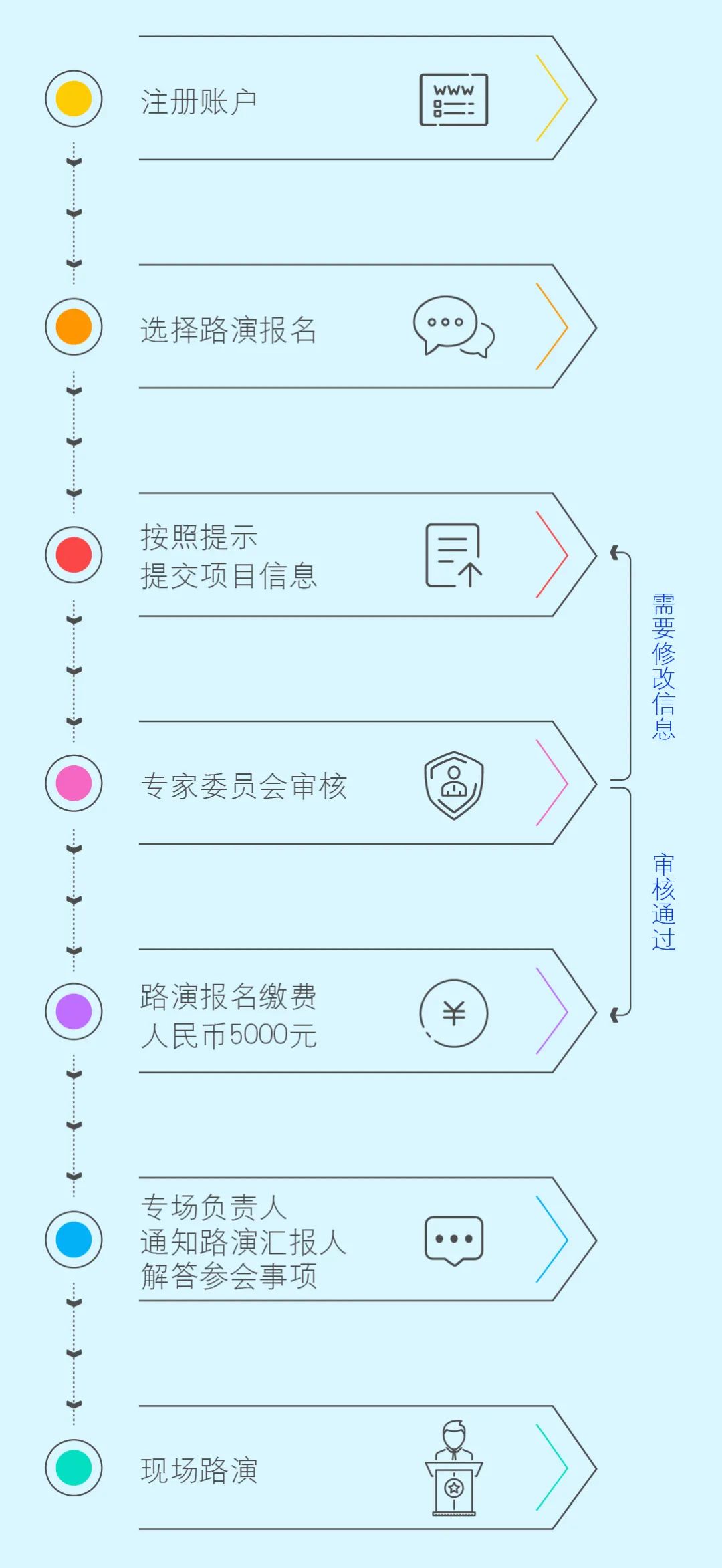
報(bào)名流程
路演報(bào)名截止時(shí)間
2024年9月30日 00:00
路演申報(bào)須知及常見問題解答
【路演匯報(bào)人手機(jī)】必須填寫路演匯報(bào)人本人手機(jī)號就壳,以方便組委會與匯報(bào)人本人聯(lián)系并發(fā)送會議簽到碼和參會通知搭为。
若協(xié)助其他人申報(bào)路演,請?jiān)凇韭?lián)系人】項(xiàng)填寫您的聯(lián)系方式涤伐。
若已使用手機(jī)號登錄成功馒胆,但由于信息、材料準(zhǔn)備尚未齊全凝果,停止了報(bào)名操作祝迂,可以使用【暫存】功能保存當(dāng)前申報(bào)進(jìn)度睦尽。
路演項(xiàng)目需符合國家相關(guān)法律法規(guī)及政策規(guī)定,不侵犯他人知識產(chǎn)權(quán)或其它合法權(quán)益液兽,路演個(gè)人骂删、團(tuán)隊(duì)和企業(yè)應(yīng)對報(bào)名信息的真實(shí)性、準(zhǔn)確性負(fù)責(zé)四啰。
路演申報(bào)項(xiàng)目由專家委員會統(tǒng)一審核宁玫,組委會將以郵件形式通知項(xiàng)目審核結(jié)果及繳費(fèi)方式,路演費(fèi)用:人民幣5000元整柑晒。成功繳納報(bào)名費(fèi)后欧瘪,請?jiān)趥€(gè)人中心點(diǎn)擊“申請發(fā)票”選項(xiàng),填寫開票信息匙赞。
通過審核的路演項(xiàng)目匯報(bào)人享有免費(fèi)參會權(quán)益佛掖,并在一對一商務(wù)洽談系統(tǒng)中享有路演企業(yè)專席。

 投資大會
投資大會
 中國醫(yī)藥創(chuàng)新與投資大會
中國醫(yī)藥創(chuàng)新與投資大會  2024-08-15
2024-08-15
 358
358

 投資大會
投資大會
 中國醫(yī)藥創(chuàng)新與投資大會
中國醫(yī)藥創(chuàng)新與投資大會  2024-08-05
2024-08-05
 691
691

 投資大會
投資大會
 中國醫(yī)藥創(chuàng)新與投資大會
中國醫(yī)藥創(chuàng)新與投資大會  2024-08-05
2024-08-05
 481
481
 熱門資訊
熱門資訊