
 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 246
246
11月13日,PTC Therapeutics宣布,美國FDA加速批準基因療法Kebilidi(eladocagene exuparvovec)用于治療芳香族L-氨基酸脫羧酶缺乏癥(AADCD)的兒童和成人患者,無論他們的疾病嚴重程度為何铜乱。據(jù)新聞稿思恐,這是FDA批準的首個直接注射到大腦的基因療法酝豪。
此前驱还,這款基因治療以Upstaza?于2022年11月獲得歐盟委員會批準上市嗜暴,成為直接注入大腦的首款獲批基因療法,也是改變AADCD疾病進程的首款獲批療法议蟆。
AADCD是一種致病率極高且會縮短壽命的罕見遺傳性疾病闷沥。患者由于編碼AADC酶的DDC基因出現(xiàn)變異咐容,導(dǎo)致AADC酶功能缺失舆逃,因此患者無法合成多巴胺,而多巴胺是運動功能所必需的神經(jīng)遞質(zhì)戳粒。
該基因療法將以KEBILIDI?(eladocagene exoparvovec tneq)的品牌在美國上市路狮,適用于治療AADC缺乏癥的兒童和成人,包括各種疾病嚴重程度恼芙。
商業(yè)化上市準備工作正在順利進行中结晒,已經(jīng)確定了卓越中心,外科醫(yī)生接受了基因治療程序的培訓(xùn)仪丛。Kebilidi是一種基于腺相關(guān)病毒2(AAV2)載體的基因療法汤史,旨在通過一次性治療软殿,將功能正常的DDC基因直接遞送到大腦的殼核中卒粮,提高AADC酶的水平并恢復(fù)多巴胺的生產(chǎn)。
該療法通過立體定向神經(jīng)外科手術(shù)直接施用于大腦殼核骨惫。臨床試驗結(jié)果表明钱挺,患者在接受該基因治療后,多巴胺會從頭合成蜀勃,隨后逐漸獲得運動發(fā)育里程碑辣沧。該療法的療效和安全性特征在多個臨床試驗和同情用藥項目中得到驗證,首例患者在2010年接受治療驼鳞。
臨床試驗的結(jié)果已經(jīng)在《細胞》旗下的Molecular Therapy上發(fā)表哀铡。

在臨床研究中,無法達到預(yù)期運動發(fā)育里程碑的患者早在接受治療3個月后就能觀察到具有臨床意義的運動功能改善臼婆,這一轉(zhuǎn)變持續(xù)到接受治療后5年以上抒痒。此外,所有接受治療患者的認知能力得到改善颁褂。
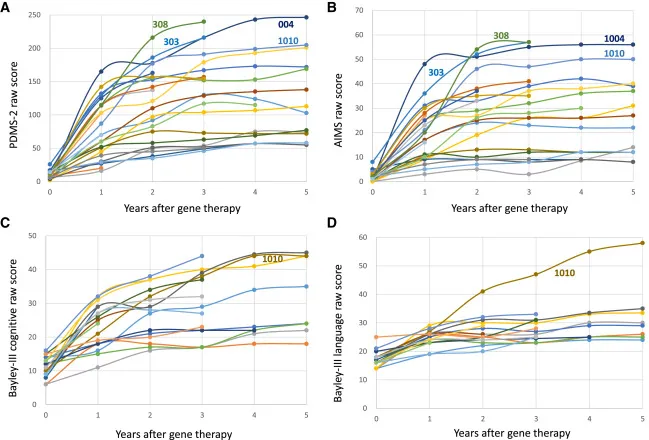
基因治療后發(fā)育里程碑的改善

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 246
246

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 225
225

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 56
56