 會員動態(tài)
會員動態(tài)
 Insight數(shù)據(jù)庫
Insight數(shù)據(jù)庫  2023-08-16
2023-08-16
 1418
1418
8 月 14 日帮廉,恒瑞醫(yī)藥發(fā)布公告稱其與美國 One Bio, Inc. 達(dá)成協(xié)議,將具有自主知識產(chǎn)權(quán)的 1 類新藥 SHR-1905 注射液項(xiàng)目有償許可給 One Bio。

來自:恒瑞
根據(jù)協(xié)議條款,One Bio 將獲得 SHR-1905 項(xiàng)目在除大中華區(qū)以外的全球范圍內(nèi)開發(fā)袱蜡、生產(chǎn)和商業(yè)化 SHR-1905 的獨(dú)家權(quán)利陈莽。
恒瑞則將獲得首付款和近期里程碑付款首付款和近期里程碑總計(jì) 2,500 萬美元底挫,其中包括 2,150 萬美元的首付款和為 SHR-1905 的首個(gè)海外臨床 Ⅱ 期試驗(yàn)提供一定數(shù)量的樣品后獲得的 350 萬美元的近期里程碑付款汗捡。在研發(fā)及銷售里程碑付款方面淑际,基于 SHR-1905 在美國、日本和約定的歐洲國家分別首次獲批上市及實(shí)際年凈銷售額情況扇住,One Bio 將向恒瑞支付累計(jì)不超過 10.25 億美元的研發(fā)及銷售里程碑款春缕。此外,One Bio 將向恒瑞支付達(dá)到實(shí)際年凈銷售額兩位數(shù)比例的銷售提成艘蹋。
SHR-1905 為恒瑞自主研發(fā)且具有知識產(chǎn)權(quán)的胸腺基質(zhì)淋巴細(xì)胞生成素 (TSLP)單克隆抗體锄贼,可以阻斷炎癥細(xì)胞因子的釋放,抑制下游炎癥信號的傳導(dǎo)女阀, 最終改善炎癥狀態(tài)并控制疾病進(jìn)展宅荤。由于 TSLP 作用于炎癥級聯(lián)反應(yīng)的早期上游,SHR-1905 有潛力適用于廣泛的重度哮喘浸策,不受表型(嗜酸性或過敏等)以及生物標(biāo)志物的限制冯键,因此相較其他靶點(diǎn)藥物具有更大的市場潛力。
此外庸汗,基于差異化的分子設(shè)計(jì)惫确,SHR-1905 有望成為同類最佳(Best-in-class)。SHR-1905 于 2021 年 5 月獲得國家藥品監(jiān)督管理局批準(zhǔn)開展用于哮喘的臨床試驗(yàn)也隧,2023 年 5 月獲批開展慢性鼻竇炎伴鼻息肉適應(yīng)癥的臨床試驗(yàn)流沦,目前均處于臨床Ⅱ期。截至目前絮商, SHR-1905 相關(guān)項(xiàng)目累計(jì)已投入研發(fā)費(fèi)用約 5,705 萬元邢窜。
SHR-1905 全球項(xiàng)目開發(fā)進(jìn)度甘特圖
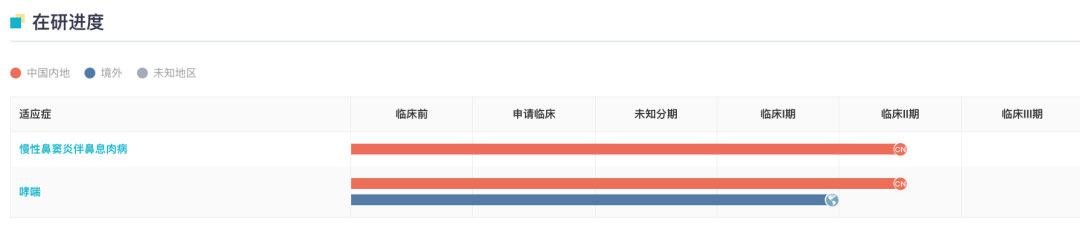
來自:Insight 數(shù)據(jù)庫網(wǎng)頁版
同類產(chǎn)品中,全球范圍內(nèi)铆韭,僅有 1 款產(chǎn)品獲批上市丘隙,即阿斯利康與安進(jìn)共同開發(fā)的 Tezspire(tezepelumab)于 2021 年在美國獲批上市,2022 年在日本和歐盟獲批上市盅力。
2022 年 Tezspire 全球銷售額合計(jì)約為 1.74 億美元;2023 年第一季度 Tezspire 全球銷售額合計(jì)約為 1.07 億美元舆焕。其他同類產(chǎn)品在國內(nèi)外尚處于臨床試驗(yàn)階段按任,適應(yīng)癥以哮喘為主。

 會員動態(tài)
會員動態(tài)
 信達(dá)生物
信達(dá)生物  2024-09-04
2024-09-04
 39
39

 會員動態(tài)
會員動態(tài)
 中國醫(yī)藥創(chuàng)新促進(jìn)會
中國醫(yī)藥創(chuàng)新促進(jìn)會  2024-08-30
2024-08-30
 92
92

 會員動態(tài)
會員動態(tài)
 中國醫(yī)藥創(chuàng)新促進(jìn)會
中國醫(yī)藥創(chuàng)新促進(jìn)會  2024-08-23
2024-08-23
 97
97
 熱門資訊
熱門資訊