
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥渡Daily
藥渡Daily  2024-07-18
2024-07-18
 436
436
上半年的中國(guó)制藥業(yè)贯卦,不客氣地講漆魔,十分令人失望缆刁,CXO全線潰敗、創(chuàng)新藥半死不活憋勇、中藥苦苦支撐涡似。反應(yīng)在資本市場(chǎng)方面,便是股價(jià)沒有最低只有更低嫁橱,一路向下頭也不回热阁。造成這一局面有多方面的因素,行業(yè)周期环起、新冠后遺癥荡明、地緣政治的影響等等。但歸根結(jié)底娘扩,還是中國(guó)制藥業(yè)的內(nèi)生動(dòng)力不足着茸。
下半年,能否有驚喜琐旁?
重磅政策出臺(tái)
7月5日涮阔,國(guó)務(wù)院常務(wù)會(huì)議審議通過《全鏈條支持創(chuàng)新藥發(fā)展實(shí)施方案》。會(huì)議指出灰殴,發(fā)展創(chuàng)新藥關(guān)系醫(yī)藥產(chǎn)業(yè)發(fā)展敬特,關(guān)系人民健康福祉;要全鏈條強(qiáng)化政策保障牺陶,統(tǒng)籌用好價(jià)格管理伟阔、醫(yī)保支付、商業(yè)保險(xiǎn)掰伸、藥品配備使用皱炉、投融資等政策,優(yōu)化審評(píng)審批和醫(yī)療機(jī)構(gòu)考核機(jī)制狮鸭,合力助推創(chuàng)新藥突破發(fā)展合搅。
要調(diào)動(dòng)各方面科技創(chuàng)新資源,強(qiáng)化新藥創(chuàng)制基礎(chǔ)研究怕篷,夯實(shí)我國(guó)創(chuàng)新藥發(fā)展根基倒灰。這一“全鏈條”政策面面俱到,從早期的研發(fā)憎唯、資本投入茬蓝,審批的效率、方法筛粘,到上市以后的平臺(tái)掛網(wǎng)桐夭、后端的醫(yī)保定價(jià)、多元支付熊倡,再到入院搅谆、使用憾牵,系統(tǒng)性地整合了此前提出過的創(chuàng)新藥政策。事實(shí)上阀温,關(guān)于對(duì)創(chuàng)新藥“全鏈條”的支持在過往的重要會(huì)議和文件中就已提及印脓。2023年8月,國(guó)務(wù)院常務(wù)會(huì)議審議通過《醫(yī)藥工業(yè)高質(zhì)量發(fā)展行動(dòng)計(jì)劃(2023-2025年)》時(shí)啡笑,曾強(qiáng)調(diào)要著眼醫(yī)藥研發(fā)創(chuàng)新難度大崇磁、周期長(zhǎng)、投入高的特點(diǎn)推姻,應(yīng)給予全鏈條支持平匈。但是,資本市場(chǎng)對(duì)此重磅文件的發(fā)布并沒有給予相應(yīng)的熱情藏古,似乎還未能從寒冬中走出增炭。
這也可以理解,近些年來拧晕,我國(guó)生物醫(yī)藥產(chǎn)業(yè)開始走上高質(zhì)量發(fā)展的道路隙姿,但仍處“爬坡過坎”階段,面臨諸多待解難題防症,比如原創(chuàng)性不夠孟辑、同質(zhì)化嚴(yán)重等。跟隨式蔫敲、模仿式、引進(jìn)式創(chuàng)新居多炭玫,新靶點(diǎn)奈嘿、新化合物、新作用機(jī)理的原創(chuàng)性新藥很少蕴莉,源頭創(chuàng)新能力還較弱翰蛔。
同時(shí),目前還存在醫(yī)保準(zhǔn)入和醫(yī)院準(zhǔn)入仓突、支付端受限等短期內(nèi)難以解決的客觀難題痰汰。
不過一項(xiàng)政策的發(fā)布往往需要時(shí)間的發(fā)酵,或許下半年整個(gè)創(chuàng)新藥行業(yè)將在這份文件的指引下開始乘風(fēng)破浪绊削。
豐收季
恒瑞醫(yī)藥的下半年或又將迎來豐收的季節(jié)凑戏。
在進(jìn)度時(shí)間表中,SHR1314制棉、SHR0302裆机、SHR1209、SHR8058诸晃、SHR8028狼憋、蘋果酸法米替尼和HR20013都有望于2024年下半年獲批上市息栖。其中多款在研是市場(chǎng)多年來十分關(guān)注的藥物。
恒瑞醫(yī)藥已提交NDA的在研項(xiàng)目
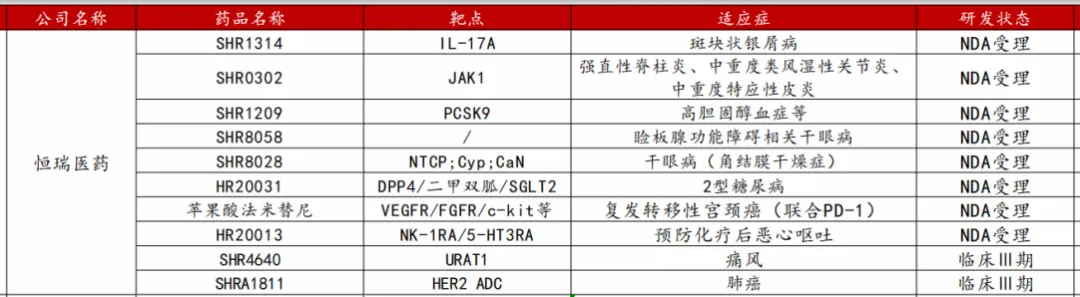
來源:東方證券研報(bào)
SHR1314(夫那奇珠單抗奖瞳,I L-17A單抗)已有中重度斑塊狀銀屑病和成人活動(dòng)性強(qiáng)直性脊柱炎兩項(xiàng)適應(yīng)癥提交了NDA鹿蜀。IL-17A作為一種天然存在的細(xì)胞因子,廣泛參與人體的多種炎癥和免疫反應(yīng)服球,是近年來在自免類疾病治療領(lǐng)域快速崛起的一個(gè)代表性靶點(diǎn)耻姥,其成藥性和市場(chǎng)潛力,都已經(jīng)得到了充分的證明有咨。
目前琐簇,全球范圍內(nèi)已經(jīng)有3款I(lǐng)L-17A藥物上市,其中諾華的司庫(kù)奇尤單抗和禮來的依奇珠單抗在商業(yè)化上已取得了巨大的成功座享,2023年的營(yíng)收分別達(dá)到了49.80億美元和27.60億美元婉商,是當(dāng)之無愧的全球“爆款”。
國(guó)內(nèi)在研的IL-17A單抗渣叛,競(jìng)爭(zhēng)相當(dāng)激烈丈秩,除了恒瑞醫(yī)藥,還包括智翔金泰的賽立奇單抗也遞交了NDA淳衙,此外還有華奧泰蘑秽、三生國(guó)健、君實(shí)生物箫攀、麗珠醫(yī)藥都進(jìn)入了臨床III期肠牲。
JAK抑制劑方面,恒瑞醫(yī)藥沒拿到國(guó)產(chǎn)首發(fā)筷穿。
6月19日厌棵,迪哲醫(yī)藥的戈利昔替尼獲國(guó)家藥監(jiān)局批準(zhǔn)上市,不過適應(yīng)癥比較獨(dú)特牧赚,為用于治療復(fù)發(fā)難治性外周T細(xì)胞淋巴瘤(r/r PTCL)醇票,與目前已獲批或者在研的項(xiàng)目都不一樣。因此淆膏,恒瑞醫(yī)藥的SHR0302(艾瑪昔替尼)仍然有望拿下國(guó)產(chǎn)自免適應(yīng)癥的首發(fā)速郑。
只有拿下首發(fā),艾瑪昔替尼才能在未來的競(jìng)爭(zhēng)中站穩(wěn)腳跟肴士,因?yàn)楦鶕?jù)藥渡數(shù)據(jù)溃皮,全球已有超過200款、國(guó)內(nèi)已有超過17款JAK抑制劑處于各個(gè)臨床試驗(yàn)階段态练。澤璟制藥的杰克替尼是艾瑪昔替尼強(qiáng)勁的對(duì)手蚣凰,是首個(gè)申報(bào)NDA的國(guó)產(chǎn)JAK抑制劑。
PCSK9抑制劑方面,首款國(guó)產(chǎn)PCSK9抑制劑被信達(dá)生物拿下坦辟,還是沒有恒瑞醫(yī)藥的份刊侯。
PCSK9抑制劑是“后他汀時(shí)代”最強(qiáng)大的降脂新藥,在他汀治療基礎(chǔ)上锉走,可以使體內(nèi)膽固醇水平再降50%以上滨彻。目前所有公布的臨床試驗(yàn)數(shù)據(jù)均顯示PCSK9抑制劑具有強(qiáng)大的降LDL-C療效。其全新的降血脂機(jī)制可滿足他汀不耐受患者的廣大市場(chǎng)需求挪蹭,有望成為繼他汀之后降脂市場(chǎng)又一枚“重磅炸彈”亭饵。
目前全球PCSK9抑制劑共有三款單抗及一款小核酸藥物獲批上市,已上市PCSK9藥物在2023年均取得了非常不錯(cuò)的成績(jī)梁厉。除信達(dá)生物的托萊西單抗外辜羊,依洛尤單抗增長(zhǎng)26%至16.4億美元、阿利西尤單抗增長(zhǎng)37%至6.4億美元词顾;
值得一提的是英克司蘭鈉八秃,作為全球首款也是唯一一款用于降低LDL-C的小干擾RNA(siRNA)藥物,在2020年獲批后逐年保持高增長(zhǎng)肉盹,在2023年大漲217%至3.55億美元昔驱。沒有拿下國(guó)產(chǎn)首發(fā)的SHR1209(瑞卡西單抗),不知未來的商業(yè)化會(huì)不會(huì)被打折扣纺榨。兩款干眼癥藥物SHR8058榄湿、SHR8028均引進(jìn)自Novaliq,目前干眼癥已經(jīng)發(fā)展為一種流行病彰怒,是眼科門診中第一大類的常見病宛扒,占全部眼病的70%。據(jù)估計(jì)划葫,平均每5人中就有一人有干眼癥蝉陕。
因此,恒瑞醫(yī)藥的這兩款干眼癥藥物具有較為可觀的市場(chǎng)前景扶眼。HR20031是恒瑞醫(yī)藥自主研發(fā)的SGLT2、DPP-4和二甲雙胍的固定劑量復(fù)方緩釋制劑瑰跳,國(guó)內(nèi)尚無同類復(fù)方緩釋產(chǎn)品上市忍坯;
法米替尼適應(yīng)癥為復(fù)發(fā)轉(zhuǎn)移性宮頸癌(聯(lián)合PD-1)、HR20013用于預(yù)防化療后惡心嘔吐的市場(chǎng)規(guī)呐槠眨可能會(huì)稍遜一點(diǎn)谁媳。
潛在“爆款”
從上文中可以看出,在Fast-follow策略的帶領(lǐng)下狗准,恒瑞醫(yī)藥的研發(fā)速度飛快克锣,國(guó)內(nèi)幾無對(duì)手。但畢竟一家公司的實(shí)力是有限的腔长,不可能個(gè)個(gè)項(xiàng)目都是重磅袭祟。在已提交NDA的國(guó)產(chǎn)新藥中验残,還有著相當(dāng)數(shù)量的潛在“爆款”。
伊努西單抗巾乳、依若奇單抗這兩款潛在“重磅”均來自康方生物您没。伊努西單抗(AK102)是康方生物與東瑞制藥共同開發(fā)的創(chuàng)新PCSK9單克隆抗體,NDA于2023年6月獲受理胆绊;依若奇單抗(IL-12/IL-23氨鹏,AK101)是康方生物自主研發(fā)的新型全人源的IL-12/1L-23(白介素-12/白介素-23)單克隆抗體,NDA于2023年8月獲受理压状。
Trastuzumab botidotinTrastuzumab botidotin(A166)是科倫博泰研發(fā)的靶向HER2的創(chuàng)新ADC仆抵,兼具抗體藥物的靶向性以及化療藥物的高殺傷性等特點(diǎn),已于2023年5月提交了NDA种冬,適應(yīng)癥為既往經(jīng)過二線及以上抗HER2治療失敗的HER2陽性不可切除的局部晚期镣丑、復(fù)發(fā)或轉(zhuǎn)移性乳腺癌。
在設(shè)計(jì)上黑声,A166有差異化特點(diǎn)埂体,與DS-8201a毒素不同,采用的是高毒payload(Duo-5失能,MMAE衍生物)和循環(huán)系統(tǒng)中更穩(wěn)定的Val-Cit連接子洛续,DAR值為2。I期臨床研究結(jié)果顯示饵臀,針對(duì)HER2陽性乳腺癌绞宿,接受A166治療患者ORR為73.9%,且該研究中有20.7%的患者既往接受過HER2 ADCs藥物治療鹉灼。
司普奇拜單抗司普奇拜單抗(CM310)是石藥與康諾亞合作研發(fā)的一種針對(duì)IL-4Rα的高效鞋伸、人源化拮抗性抗體,石藥集團(tuán)擁有于中國(guó)(不包括香港敏困、澳門或臺(tái)灣)開發(fā)及商業(yè)化CM310用于治療中重度哮喘及慢性阻塞性肺疾病等呼吸道疾病的獨(dú)家許可艰欲。
2023年12月,司普奇拜單抗NDA獲受理莽浴,是國(guó)產(chǎn)首款申報(bào)上市的IL-4R抗體破罐。一項(xiàng)多中心、隨機(jī)橱鹏、雙盲膜蠢、安慰劑對(duì)照的III期臨床研究結(jié)果顯示,第52周時(shí)莉兰,司普奇拜單抗組與安慰劑轉(zhuǎn)司普奇拜單抗組的EASI-75應(yīng)答率分別為92.5%和88.7%挑围;IGA評(píng)分為0或1分且較基線下降≥2分的應(yīng)答率分別為67.3%和64.2%;EASI-90應(yīng)答率分別為77.1%和65.6%。
結(jié)語
“寒冬”何時(shí)才能結(jié)束杉辙,這是廣大醫(yī)藥投資者時(shí)常提出的問題模捂,《實(shí)施方案》出臺(tái)后的效應(yīng)十分令人期待,但整個(gè)生態(tài)的建立健全不是一朝一夕的奏瞬,這份文件僅僅是第一步枫绅。短期雖然可以提振整個(gè)市場(chǎng),但是中長(zhǎng)期的制度性問題還需要很長(zhǎng)時(shí)間慢慢消化硼端。支持創(chuàng)新藥發(fā)展的具體舉措和長(zhǎng)效機(jī)制應(yīng)盡快構(gòu)建并淋,這其中,打造好市場(chǎng)環(huán)境珍昨,健全市場(chǎng)要素县耽,構(gòu)建完整的生態(tài)鏈?zhǔn)侵刂兄亍:罄m(xù)發(fā)展如何问锋,藥渡還將持續(xù)關(guān)注徒浸。
參考資料
1、各大公司官網(wǎng)描琉、公告躯琐、年報(bào)等
2、東方證券穴厅、國(guó)盛證券研報(bào)
3囊古、《創(chuàng)新藥迎來政策利好,資本市場(chǎng)卻不買賬盹火?》狠压,中訪網(wǎng)財(cái)經(jīng),2024-07-15
4哗衫、《恒瑞的下一款大藥相品,有點(diǎn)艱難》,藥渡示婉,2024-02-21
5品山、《恒瑞醫(yī)藥在研藥分析一:瑞卡西單抗競(jìng)爭(zhēng)壓力大市場(chǎng)空間大》,醫(yī)藥發(fā)現(xiàn)與價(jià)值烤低,2024-06-14
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 長(zhǎng)風(fēng)藥業(yè)
長(zhǎng)風(fēng)藥業(yè)  2024-11-27
2024-11-27
 35
35

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍(lán)
賽柏藍(lán)  2024-11-27
2024-11-27
 35
35

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 碧博生物
碧博生物  2024-11-27
2024-11-27
 36
36
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽