
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Insight數(shù)據(jù)庫
Insight數(shù)據(jù)庫  2024-07-19
2024-07-19
 456
456
7 月 19 日遏治,據(jù) CDE 官網(wǎng)顯示,豪森藥業(yè)阿美替尼第三項適應(yīng)癥上市申請獲受理梆砸,推測的適應(yīng)癥可能為:表皮生長因子受體(EGFR)敏感突變非小細胞肺癌(NSCLC)的輔助治療(受理號:CXHS2400060)哺哼。
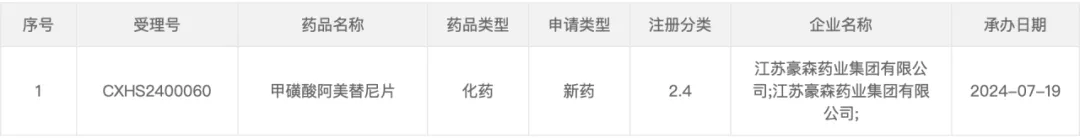
截圖來自:CDE官網(wǎng)
在此之前佩抹,阿美替尼已在 2020 年 3 月獲批,適用于既往經(jīng) EGFR 酪氨酸激酶抑制劑(TKI)治療時或治療后出現(xiàn)疾病進展虽柜,并且經(jīng)檢測確認存在 EGFR T790M 突變陽性的局部晚期或轉(zhuǎn)移性 NSCLC 成人患者飒晴。2021 年 12 月,阿美替尼再次獲批财偶,從二線推進到一線拙位,用于具有 EGFR 外顯子 19 缺失或外顯子 21(L858R)置換突變陽性的局部晚期或轉(zhuǎn)移性 NSCLC 成人患者的一線治療。本次新適應(yīng)癥的受理课枉,讓阿美替尼適應(yīng)癥拓展到圍手術(shù)期属胖,進一步拓展了阿美替尼在 NSCLC 領(lǐng)域的商業(yè)潛力。
在 NSCLC 患者中,EGFR 基因突變是最常見的變異類型莲疤。針對這些突變恃定,EGFR-TKI 被公認為最有效的治療手段。目前砍机,國內(nèi)已上市三代 EGFR-TKI 藥物寞殿。在臨床應(yīng)用中,第三代 EGFR-TKI 在前兩代的基礎(chǔ)上取得了顯著的療效提升铭莱。阿美替尼作為首個國產(chǎn)原創(chuàng)的第三代 EGFR 靶向藥物骡尽,彌補了國產(chǎn)藥物在這一領(lǐng)域的歷史空白。
2020 年 12 月擅编,豪森藥業(yè)正式啟動了一項隨機攀细、對照、雙盲沙咏、III 期辨图、多中心臨床研究,旨在評估阿美替尼相較于安慰劑在 EGFR 敏感突變陽性的 II-IIIB 期 NSCLC 輔助治療中的有效性和安全性(NCT04687241/CTR20202460)肢藐。該研究的主要終點為獨立評審委員會(IRC)評估的無病生存期(DFS)故河,預(yù)計該臨床試驗將于 2029 年 1 月完成,期待數(shù)據(jù)發(fā)布吆豹。
NCT04687241/CTR20202460歷史時光軸
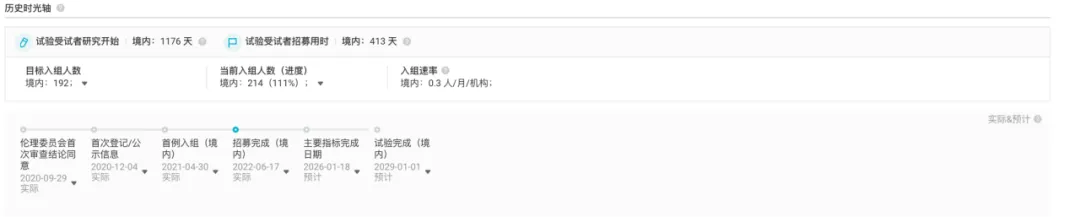
截圖來自:Insight 數(shù)據(jù)庫官網(wǎng)
除了在國內(nèi)大放異彩外鱼的,豪森藥業(yè)針對阿美替尼在國際市場上也展開了積極的戰(zhàn)略布局。2022 年 12 月痘煤,EMA 正式受理了阿美替尼的上市許可申請凑阶。該申請涉及兩項適應(yīng)癥:一是用于一線治療具有 EGFR 敏感突變的局部晚期或轉(zhuǎn)移性 NSCLC 成人患者,二是用于治療存在 EGFR T790M 突變陽性的局部晚期或轉(zhuǎn)移性 NSCLC 成人患者衷快。這一重要舉措標(biāo)志著豪森藥業(yè)在全球抗癌藥物市場中的進一步拓展宙橱,彰顯了其在抗腫瘤領(lǐng)域的研發(fā)實力和國際化發(fā)展戰(zhàn)略。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 長風(fēng)藥業(yè)
長風(fēng)藥業(yè)  2024-11-27
2024-11-27
 32
32

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍
賽柏藍  2024-11-27
2024-11-27
 32
32

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 碧博生物
碧博生物  2024-11-27
2024-11-27
 33
33