
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識林
識林  2024-07-26
2024-07-26
 404
404
美國 FDA 于 7 月 17 日發(fā)布了《2023 財(cái)年廠房設(shè)施檢查年報(bào)》,為我們了解 FDA 的檢查情況提供了一個全景圖乞哀。
從報(bào)告中初橘,我們可以了解到撕擂,2023 財(cái)年蘑拯,在 FDA 注冊的中國藥品(包括原料藥)和醫(yī)療器械設(shè)施有 6,897 家枯怖,F(xiàn)DA 對這些中國設(shè)施進(jìn)行了 53 次 GMP 檢查猾瘸,74 次批準(zhǔn)前/許可前檢查勉盅,41 次監(jiān)督檢查,12 次有因檢查牺氨。
相比之下狡耻,在 FDA 注冊的印度設(shè)施有 1,245 家,F(xiàn)DA 對這些印度設(shè)施進(jìn)行了 155 次 GMP 檢查猴凹,113 次批準(zhǔn)前/許可前檢查夷狰,110 次監(jiān)督檢查,45 次有因檢查郊霎。
根據(jù) FDA 6 月份發(fā)布的另一份年報(bào) —《2023 財(cái)年藥品質(zhì)量狀況報(bào)告》沼头,F(xiàn)DA 對于印度檢查覆蓋率較高,而中國檢查覆蓋率較低的解釋是由于旅行限制導(dǎo)致檢查延遲书劝。
首先來介紹一下 FDA 發(fā)布這份廠房設(shè)施檢查年報(bào)的背景进倍。根據(jù) 2012年《FDA 安全與創(chuàng)新法》(FDASIA)要求 FDA 每年在網(wǎng)站上公布依據(jù)《聯(lián)邦食品、藥品和化妝品法》(FDCA)第 510 條注冊的廠房設(shè)施的檢查報(bào)告购对。此后猾昆,《21 世紀(jì)醫(yī)藥法》和 2017 年《FDA 重授權(quán)法》(FDARA)對這一要求進(jìn)行了小幅修訂。2022 年 12 月的《食品藥品綜合改革法》(FDORA)對報(bào)告要求進(jìn)行了大幅修訂协包。
根據(jù)修訂后的法律要求帅珍,F(xiàn)DA 應(yīng)不遲于每年的 5 月 1 日在其網(wǎng)站上發(fā)布廠房設(shè)施檢查年報(bào),內(nèi)容應(yīng)包括:
上一財(cái)年根據(jù) FDCA 第 510 條注冊的美國本土和海外的廠房設(shè)施數(shù)量
各關(guān)注地區(qū)此類注冊設(shè)施的數(shù)量幔憋;
上一財(cái)年度檢查的本土設(shè)施數(shù)量和海外設(shè)施數(shù)量司报,包括各關(guān)注地區(qū)設(shè)施數(shù)量;
上一財(cái)年度執(zhí)行的檢查次數(shù);
上一財(cái)年度執(zhí)行的例行監(jiān)督檢查次數(shù)偎洋,包括各關(guān)注地區(qū)滚尼;
上一財(cái)年度執(zhí)行的有因檢查次數(shù),包括每各關(guān)注地區(qū)睁奶;
達(dá)成的協(xié)議認(rèn)可或其它方式認(rèn)可的檢查次數(shù)栽寄,包括各關(guān)注地區(qū);
原料藥(API)或成品制劑(FDF)每類廠房設(shè)施的數(shù)量拆聋;
FDA 預(yù)算中用于上述檢查的百分比;
FDA 擴(kuò)大對外國監(jiān)管機(jī)構(gòu)認(rèn)可的檢查的情況姊呐,包括擴(kuò)大此類認(rèn)可范圍方面存在的障礙懒披。
這里的關(guān)注地區(qū)(Region of Interest)法律定義是指包括中國、印度剖张、歐盟切诀、英國以及 FDA 認(rèn)為有必要對該地區(qū)進(jìn)行特定檢查的外國國家或地理區(qū)域。
下面我們具體來看看一些數(shù)據(jù):
表1 美國本土和海外藥品和器械注冊廠房設(shè)施數(shù)量
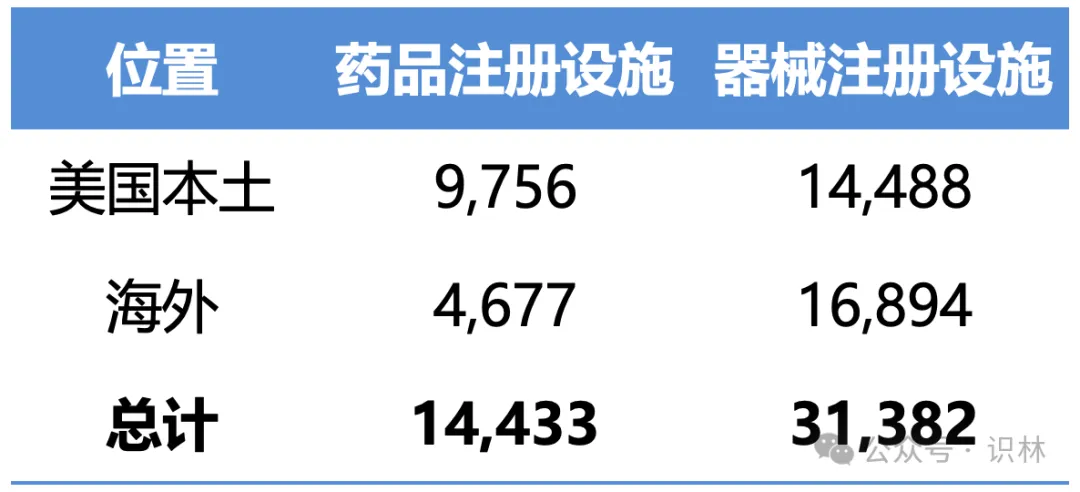
表2 關(guān)注地區(qū)注冊廠房設(shè)施數(shù)量(編者注:這里的廠房設(shè)施包括藥品和器械設(shè)施)

表3 注冊藥品設(shè)施類型
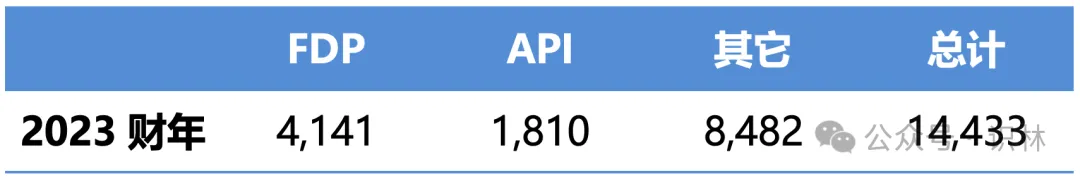
表4 美國本土和海外設(shè)施檢查數(shù)量(GMP檢查)

表5 支持申請行動的廠房設(shè)施檢查數(shù)量(批準(zhǔn)前/許可前檢查)

表6 例行監(jiān)督檢查和有因檢查數(shù)量
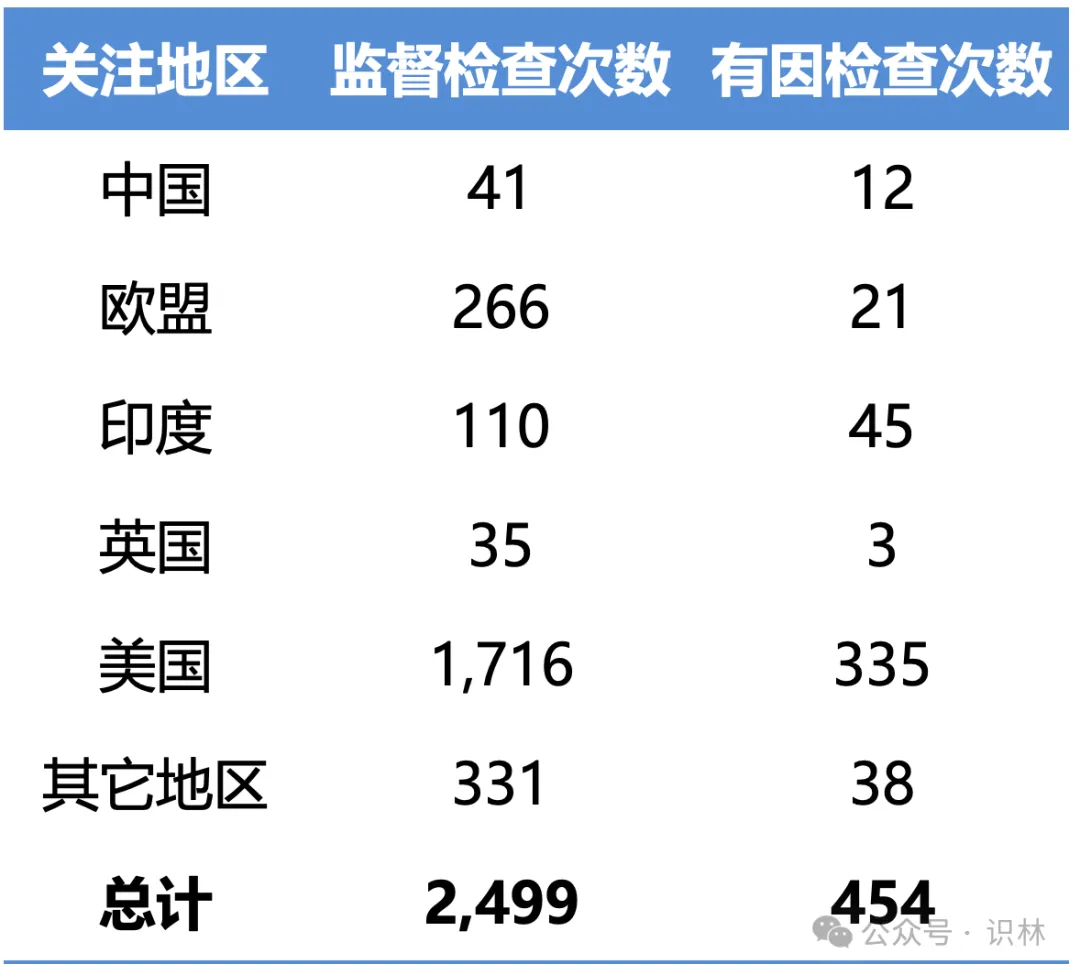
表7 通過互認(rèn)協(xié)議(Mutual Recognition Agreement搔弄,MRA)由外國監(jiān)管機(jī)構(gòu)執(zhí)行的例行監(jiān)督檢查和有因檢查數(shù)量
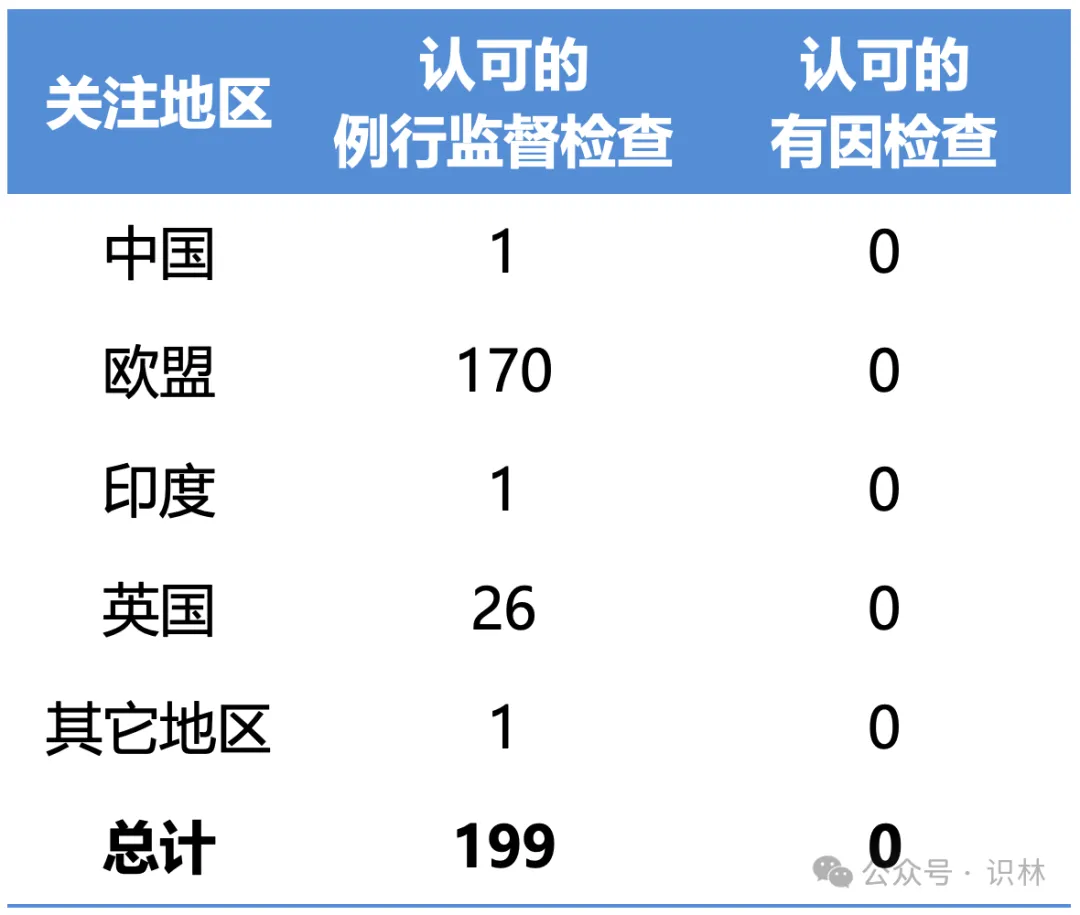
FDA 在報(bào)告中表示擴(kuò)大了與歐盟的互認(rèn)協(xié)議范圍幅虑,以包括獸藥,并與瑞士簽署并生效了互認(rèn)協(xié)議顾犹。此外倒庵,F(xiàn)DA 最近實(shí)施了第三國檢查,以擴(kuò)大 MRA 影響范圍炫刷。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 長風(fēng)藥業(yè)
長風(fēng)藥業(yè)  2024-11-27
2024-11-27
 24
24

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍(lán)
賽柏藍(lán)  2024-11-27
2024-11-27
 25
25

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 碧博生物
碧博生物  2024-11-27
2024-11-27
 26
26
 熱門資訊
熱門資訊