
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-08-02
2024-08-02
 420
420
2024年8月1日泞叉,宜明昂科-B(01541)發(fā)布公告稱督近,與Instil Bio, Inc (NASDAQ: TIL)全資子公司SynBioTx Inc.達(dá)成獨(dú)家對外授權(quán)協(xié)議:宜明昂科將其兩款在研創(chuàng)新管線產(chǎn)品IMM2510(VEGFxPD-L1 mAb-Trap)和IMM27M(CTLA-4, ADCC加強(qiáng)型)大中華區(qū)以外的開發(fā)及商業(yè)化權(quán)利授權(quán)SynBioTx Inc.,同時(shí)保留兩款產(chǎn)品在大中華區(qū)的權(quán)利曼散。宜明昂科將獲得5000萬美金的首付款及近期付款茁升,以及超過20億美金的后續(xù)開發(fā)嫂前、注冊、商業(yè)化里程碑付款鹰泡,及單位數(shù)至低雙位數(shù)的大中華區(qū)以外的銷售提成萝渐。
IMM2510由宜明昂科自主研發(fā),是一款靶向VEGF及PD-L1的雙特異性分子叛冠,采用單克隆抗體-受體重組蛋白(mAb-Trap)結(jié)構(gòu)磨慷。IMM2510能夠通過阻斷VEGF/VEGFR信號通路,抑制腫瘤血管生成從而抑制腫瘤的生長和轉(zhuǎn)移把奢,并使腫瘤細(xì)胞對免疫反應(yīng)更敏感薇痛,同時(shí)通過阻斷PD-L1/PD-1相互作用及誘導(dǎo)Fc介導(dǎo)的抗體依賴的細(xì)胞毒性作用(ADCC)和抗體依賴的細(xì)胞吞噬作用(ADCP)活性激活T細(xì)胞、自然殺傷細(xì)胞及巨噬細(xì)胞什湘,從而發(fā)揮抗腫瘤免疫治療作用凳忙。
同時(shí)靶向 PD-(L)1 和 VEGF的雙特異性分子在治療惡性實(shí)體瘤方面有著巨大的市場前景。今年5月禽炬,康方生物披露了依沃西單抗(PD-1/VEGF雙特異性抗體)單藥頭對頭K藥一線治療PD-L1陽性的NSCLC III期臨床數(shù)據(jù)取得陽性結(jié)果涧卵,點(diǎn)燃了業(yè)界對于其未來在該適應(yīng)癥上替代K藥等PD-1單抗的期待。普米斯生物的PM8002(PD-L1/VEGF雙特異性抗體)也在三陰性乳腺癌中取得亮眼的臨床數(shù)據(jù)腹尖。而在2022和2023年柳恐,康方和普米斯分別與Summit Therapeutics和BioNTech達(dá)成了金額可觀的授權(quán)合作。
作為國內(nèi)臨床開發(fā)進(jìn)度處于第一梯隊(duì)的VEGF/PD-L1雙特異性分子热幔,宜明昂科的IMM2510多個(gè)項(xiàng)目已經(jīng)進(jìn)入臨床phase Ib/II 階段乐设,包括單藥和聯(lián)合治療項(xiàng)目。2024 ASCO年會上公布的I期劑量遞增結(jié)果顯示绎巨,IMM2510總體耐受性良好并在實(shí)體瘤中展示出積極的療效信號:在不同劑量下近尚,2例既往免疫治療失敗的非小細(xì)胞肺鱗癌患者及1例胸腺鱗癌患者取得了部分緩解(PR),在7例疾病穩(wěn)定(SD)的實(shí)體瘤患者中场勤, 4例取得腫瘤縮小15%以上的SD(其中兩例為非小細(xì)胞肺癌)戈锻。
此次交易中的另一個(gè)產(chǎn)品IMM27M是新一代CTLA-4抗體,具有增強(qiáng)的ADCC活性首潮。其可誘導(dǎo)靶向CTLA-4過度表達(dá)彬膘、具有免疫抑制作用的調(diào)節(jié)性T細(xì)胞的強(qiáng)效免疫反應(yīng),促進(jìn)調(diào)節(jié)性T細(xì)胞從腫瘤微環(huán)境(TME)中清除剑学,從而增強(qiáng)T細(xì)胞的抗腫瘤反應(yīng)绝皇。
IMM27M已完成I期劑量遞增的患者招募工作, 2023年ASCO年會上公布的數(shù)據(jù)顯示IMM27M總體耐受性良好:在較廣的劑量范圍里膨溃,所有受試者均沒有出現(xiàn)劑量限制性毒性(DLT)呐猴。在兩例經(jīng)過多線治療后的激素受體陽性(HR+)的晚期乳腺癌患者中觀察到積極的療效(兩例均獲得PR);一例晚期復(fù)發(fā)的實(shí)體瘤患者中觀察到腫瘤縮小超過20%的SD肠祭。乳腺癌是女性發(fā)病率最高的惡性腫瘤常废,根據(jù)WHO數(shù)據(jù)铝儒,2022年全球有230萬女性被診斷患乳腺癌,激素受體陽性乳腺癌占總體乳腺癌的約70%极棵。
IMM2510和IMM27M在肺癌抬邑、乳腺癌及其他實(shí)體瘤方面積極的療效表現(xiàn),為這兩個(gè)產(chǎn)品在市場潛力巨大的實(shí)體瘤領(lǐng)域的后續(xù)開發(fā)打下了良好的開端嗤详。加上合作方和美國資本市場的加持个扰,有望未來快速推進(jìn)國際臨床進(jìn)展。
差異化優(yōu)勢的CD47
宜明昂科從成立伊始葱色,就一直被標(biāo)簽為CD47靶點(diǎn)研發(fā)的biotech递宅。其核心產(chǎn)品替達(dá)派西普 (IMM01) 已有三個(gè)適應(yīng)癥獲批III期注冊臨床,其中IMM01聯(lián)合替雷利珠單抗針對PD-(L)1單抗難治性經(jīng)典霍奇金淋巴瘤(cHL)Ⅲ期注冊臨床試驗(yàn)于7月初完成首例患者入組給藥苍狰。
作為一個(gè)關(guān)鍵的巨噬細(xì)胞檢查點(diǎn)办龄,在多種腫瘤細(xì)胞表面都有表達(dá),CD47曾被認(rèn)為是繼PD-1/PD-L1之后潛力巨大的腫瘤免疫靶點(diǎn)淋昭。然而在過去兩年里俐填,相關(guān)藥物的研發(fā)屢屢碰壁。
面對市場的擔(dān)憂和疑慮翔忽,宜明昂科創(chuàng)始人田文志博士曾對IMM01的差異化優(yōu)勢進(jìn)行了介紹:“IMM01是SIRPα-Fc融合蛋白英融。為解決CD47分子的安全性問題,IMM01與CD47結(jié)合區(qū)域采用了一個(gè)工程化的人類SIRPα結(jié)構(gòu)域歇式,在體外研究中驶悟,該結(jié)構(gòu)域顯示不與人體紅細(xì)胞結(jié)合,具有很強(qiáng)的安全性優(yōu)勢材失。另外找塌,公司還對該結(jié)構(gòu)域采取了去糖基化的修飾,降低了分子的免疫原性困煤。IMM01通過雙重作用機(jī)制充分激活巨噬細(xì)胞鸥萌,即干擾CD47/SIRPα相互作用阻斷“別吃我”信號,并通過激活巨噬細(xì)胞的Fcγ受體傳遞“吃我”信號前忿。橫向?qū)Ρ瓤垂卑矗琁MM01的親和力KD為~3nM,約為Magrolimab的千分之一扁奢,適中的親和力使得IMM01的外周血受體占位維持在10-15%的水平,(而Magrolimab用藥后14天為90%以上)匹憎,從而避免了CD47抗體藥物常見的抗原沉默效應(yīng)逻袭。IMM001的Ⅱ期推薦劑量僅為2.0mg/kg,CD47抗體劑量通常在20至45mg/kg之間业满≈恚”
替達(dá)派西普的優(yōu)勢也在臨床數(shù)據(jù)中得到了印證克矿,兩項(xiàng)II期臨床研究數(shù)據(jù)—IMM01聯(lián)合阿扎胞苷(AZA)治療初治較高風(fēng)險(xiǎn)的骨髓增生異常綜合征(HR-MDS)和IMM01聯(lián)合替雷利珠單抗治療既往PD-1抗體治療失敗后的經(jīng)典霍奇金淋巴瘤(cHL)入選2024 ASCO口頭報(bào)告,以其優(yōu)秀的療效和安全性數(shù)據(jù)贏得了現(xiàn)場的熱烈反響憎兽。其中IMM01聯(lián)合替雷利珠單抗治療既往PD-1抗體治療失敗后cHL的口頭報(bào)告被2024年中國臨床腫瘤學(xué)年度進(jìn)展研討會(BOC)評選為Best of ASCO in China? 冷离。
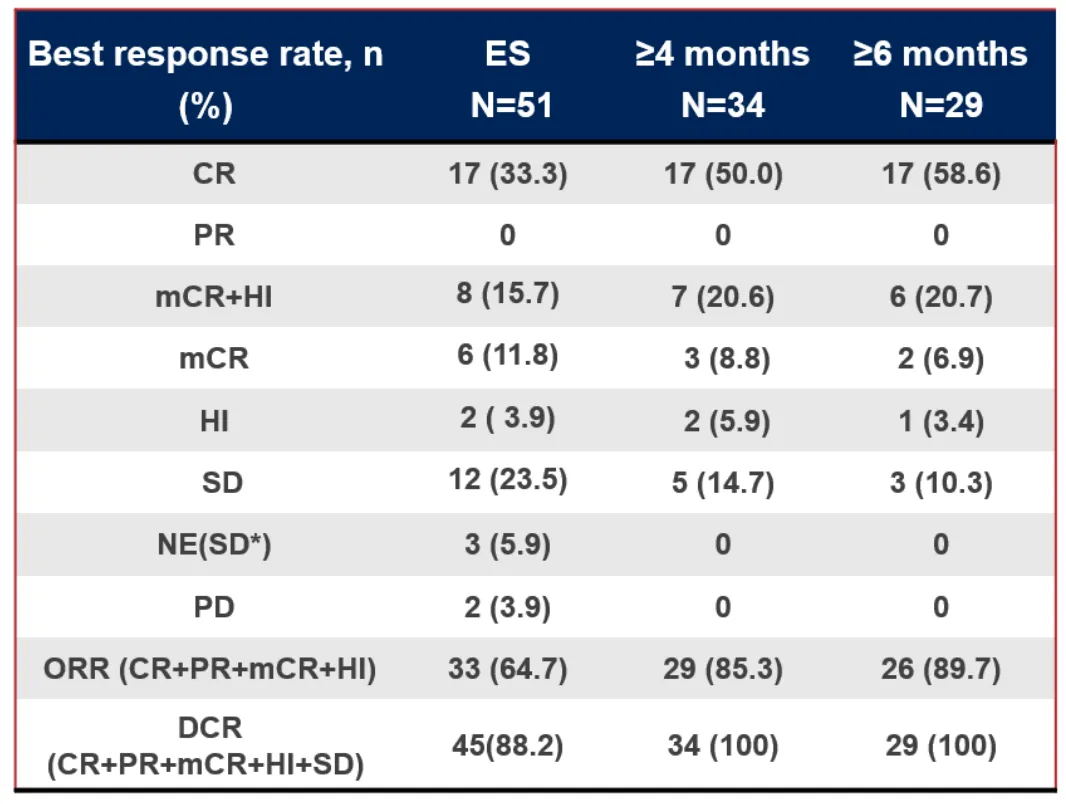
根據(jù)ASCO數(shù)據(jù),IMM01聯(lián)合阿扎胞苷治療初治HR-MDS適應(yīng)癥方面纯命,在整體51個(gè)可評估患者中西剥,完全緩解率(CR)達(dá)到33.3%,總體反應(yīng)率達(dá)到64.7%亿汞;在治療超過4個(gè)月的34名患者中瞭空,CR達(dá)到50.0%, ORR達(dá)到85.3%疗我;而在治療超過6個(gè)月的29名患者中咆畏,CR達(dá)到58.6%, ORR達(dá)到89.7%吴裤;反應(yīng)隨著治療時(shí)間的延長旧找,療效持續(xù)提升。中位觀察時(shí)間為15.9個(gè)月麦牺,中位無進(jìn)展生存期(mPFS)和中位總生存期(mOS)未達(dá)到钦讳,12個(gè)月OS為71.1%。同時(shí)還觀察到IMM01+AZA聯(lián)合治療后整體血紅蛋白(HGB)和血小板(PLT)明顯恢復(fù)枕面,血紅蛋白或血小板輸注顯著減少栖挣。IMM01聯(lián)合AZA做為一線治療成人較高風(fēng)險(xiǎn)MDS患者耐受性良好,療效顯著贮祥。
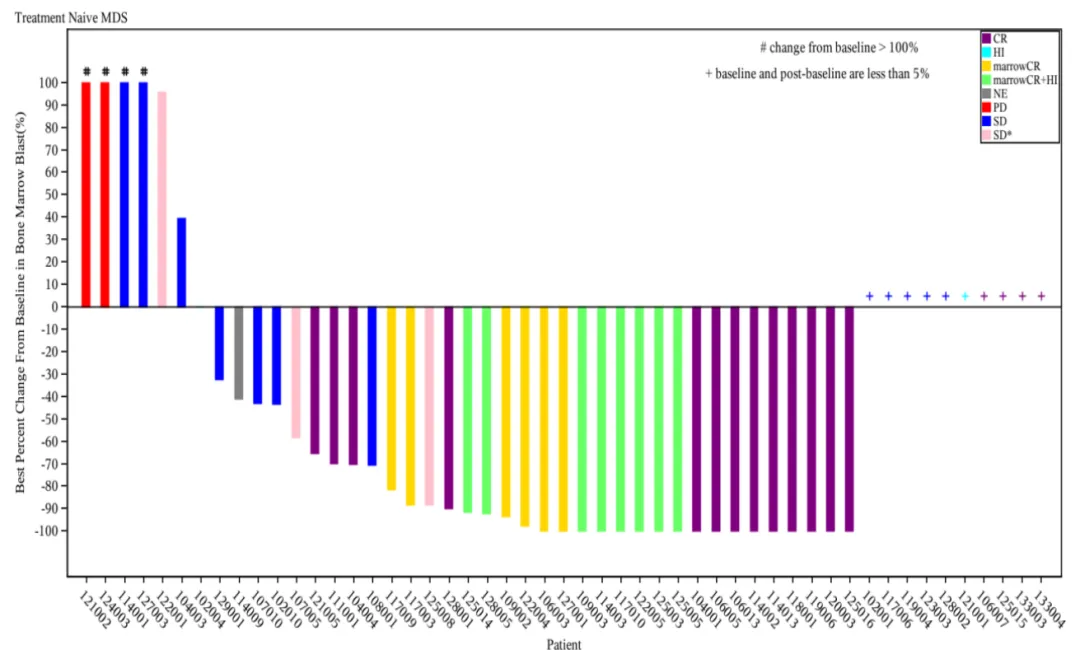
(骨髓原始細(xì)胞較基線的最佳百分比變化)
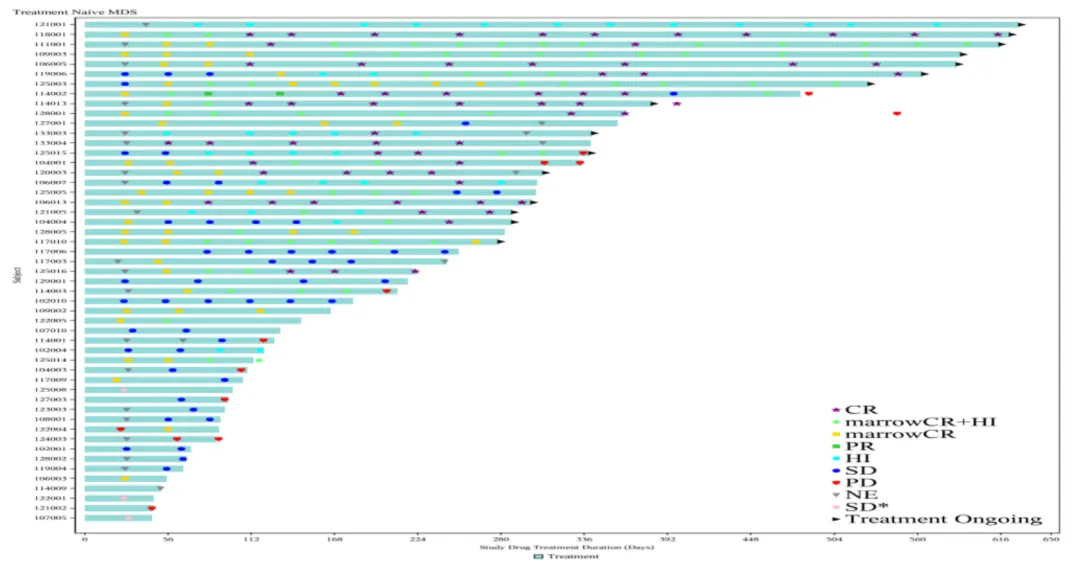
(治療持續(xù)時(shí)間及反應(yīng))
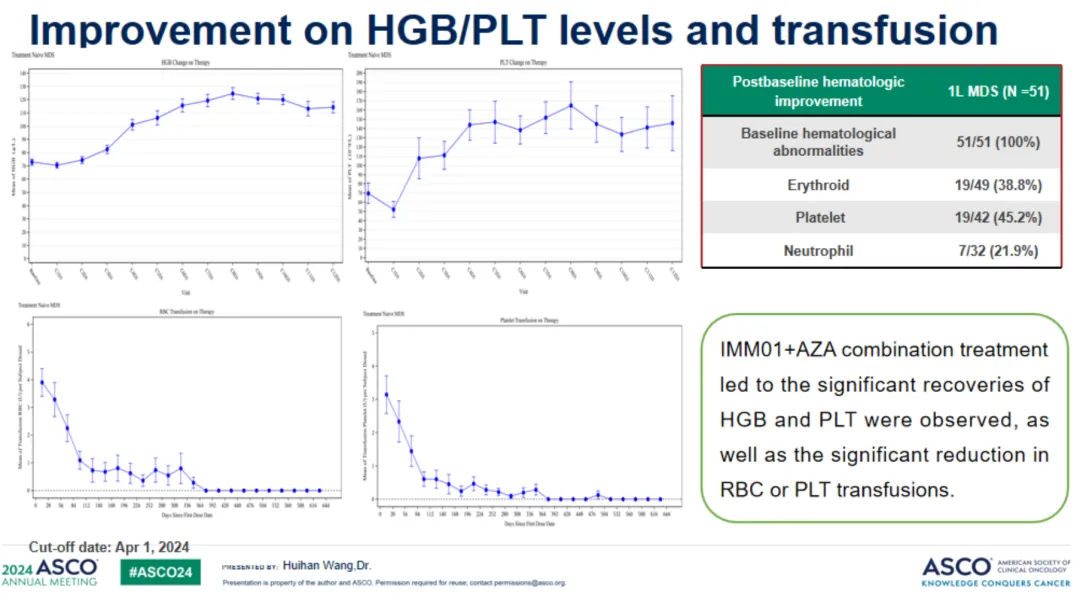
(在51例可評估患者中經(jīng)過治療后血紅蛋白和血小板明顯恢復(fù)夫次,血紅蛋白或血小板輸注顯著減少)
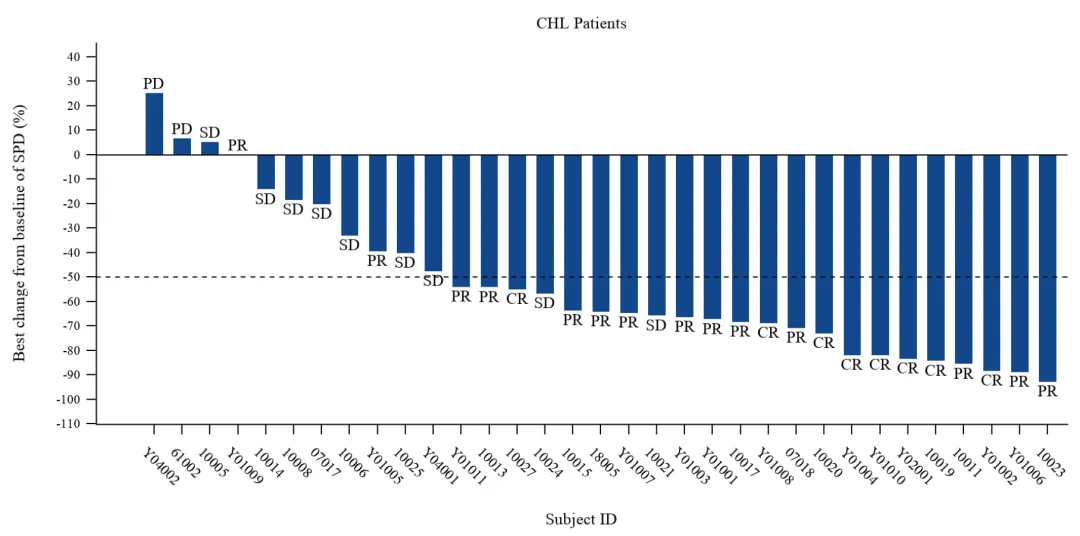
IMM01聯(lián)合替雷利珠單抗治療既往PD-1抗體治療失敗后的cHL II期試驗(yàn)數(shù)據(jù)顯示,在33例可評估患者中(此前接受的平均治療線數(shù)為4線)程昨,ORR達(dá)到66.7%, CR 率達(dá)到 24.2%搔冈。在29例(87.9%)患者中觀察到靶病灶大小的減小。中位觀察時(shí)間為6.87個(gè)月咖亏,中位至緩解時(shí)間為1.6個(gè)月肩菲,中位無進(jìn)展生存期和中位持續(xù)緩解時(shí)間未達(dá)到∫烟疲總體安全性耐受性良好犹佣,未觀察到溶血的發(fā)生。
不只是CD47
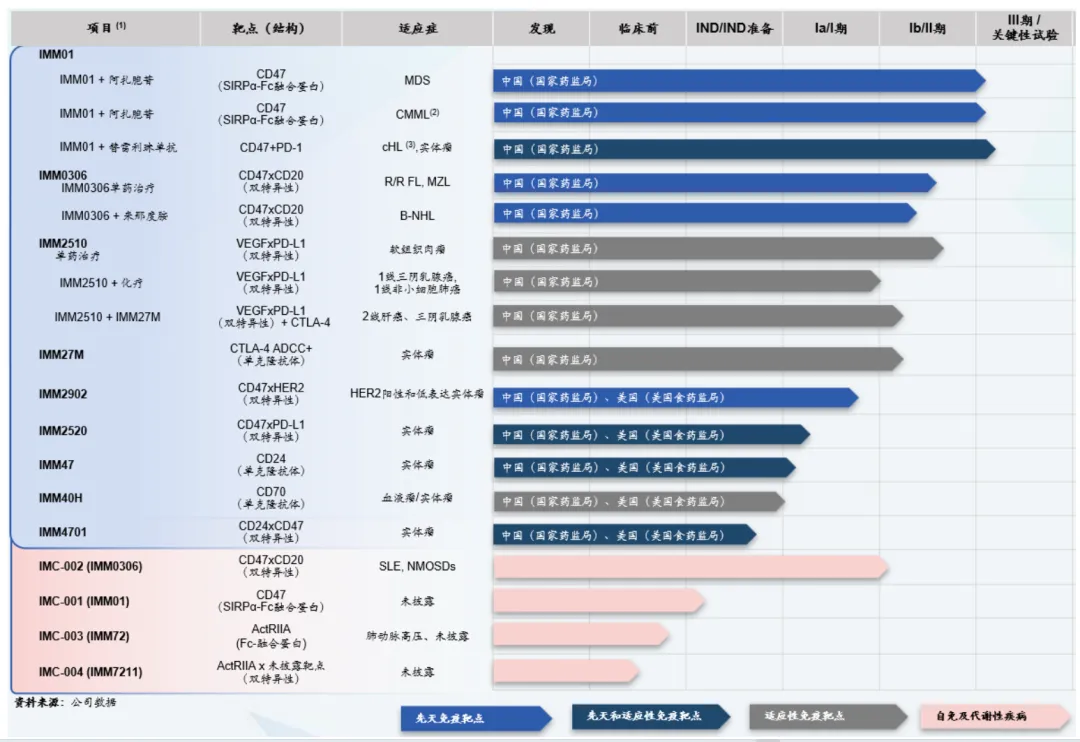
作為一家全自研的創(chuàng)新藥研發(fā)平臺型公司绞芽,縱觀宜明昂科產(chǎn)品線皱辞,除了CD47和本次對外授權(quán)的VEGF x PD-L1和CTLA-4 ADCC+, 亦有布局靶向CD24, CD70等創(chuàng)新分子,以及代謝領(lǐng)域大有可為的ActRIIA和此靶點(diǎn)相關(guān)的雙抗。而在競爭格局相對良好且市場空間巨大的自免領(lǐng)域股冗,宜明昂科的Amulirafusp alfa (IMM0306, CD47x CD20 mAb-Trap)已獲得兩個(gè)適應(yīng)癥IND批件霹陡。
宜明昂科此次授權(quán)合作方Instil Bio為一家專注創(chuàng)新腫瘤治療的臨床階段biotech公司。根據(jù)該公司官網(wǎng)資料止状,其CEO Bronson Crouch是一位生物醫(yī)藥行業(yè)資深創(chuàng)業(yè)者和投資人烹棉,他曾投資的Peloton Therapeutics于2019年被Merk以11億美金首付款收購,核心產(chǎn)品Belzutifan(PT2977)于2023年獲FDA批準(zhǔn)上市怯疤,治療晚期腎細(xì)胞癌浆洗;另一家腫瘤免疫公司CoStim Pharmaceuticals, Inc.于2014年被諾華收購,成交金額未披露旅薄。
此次BD合作辅髓,除了給宜明昂科帶來可觀的現(xiàn)金流外,也將助力宜明昂科在市場空間更大的實(shí)體瘤板塊加速推進(jìn)少梁。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 長風(fēng)藥業(yè)
長風(fēng)藥業(yè)  2024-11-27
2024-11-27
 12
12

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍(lán)
賽柏藍(lán)  2024-11-27
2024-11-27
 12
12

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 碧博生物
碧博生物  2024-11-27
2024-11-27
 14
14
 熱門資訊
熱門資訊