
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥筆記
醫(yī)藥筆記  2024-08-07
2024-08-07
 331
331
2024年8月5日,樂普生物發(fā)布公告射赛,在研EGFR ADC新藥MRG003獲得FDA的突破療法認(rèn)證店溢,用于治療復(fù)發(fā)性或轉(zhuǎn)移性非角質(zhì)化鼻咽癌(NPC)成人患者属提。


突破療法為FDA加快新藥審評的4種方式之一漱办,資格認(rèn)定要求非常嚴(yán)格,適用于嚴(yán)重和危及生命的適應(yīng)癥区蛹,并在重要臨床終點已經(jīng)表現(xiàn)出相比于現(xiàn)有療法有重大臨床改善的藥物业满。獲得突破療法認(rèn)證的藥物,可以獲得所有快速通道的審評待遇姊宗,開發(fā)過程中可以盡早的獲得密集指導(dǎo)等歹朵。
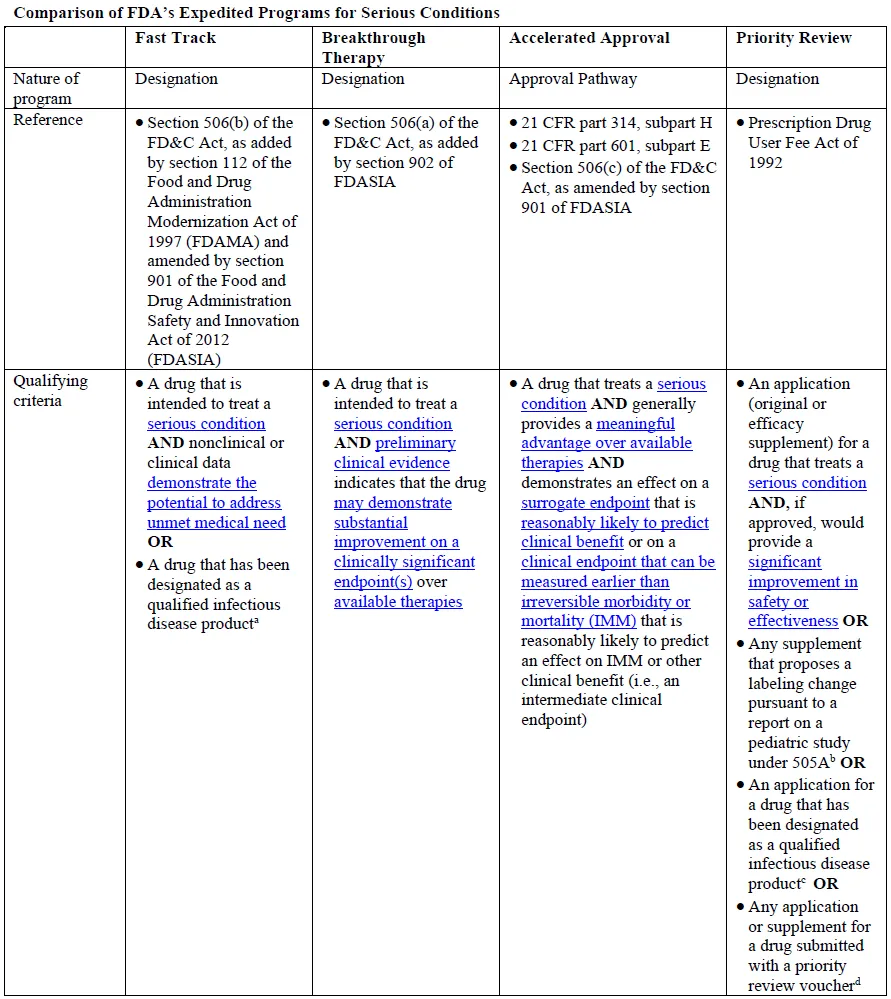
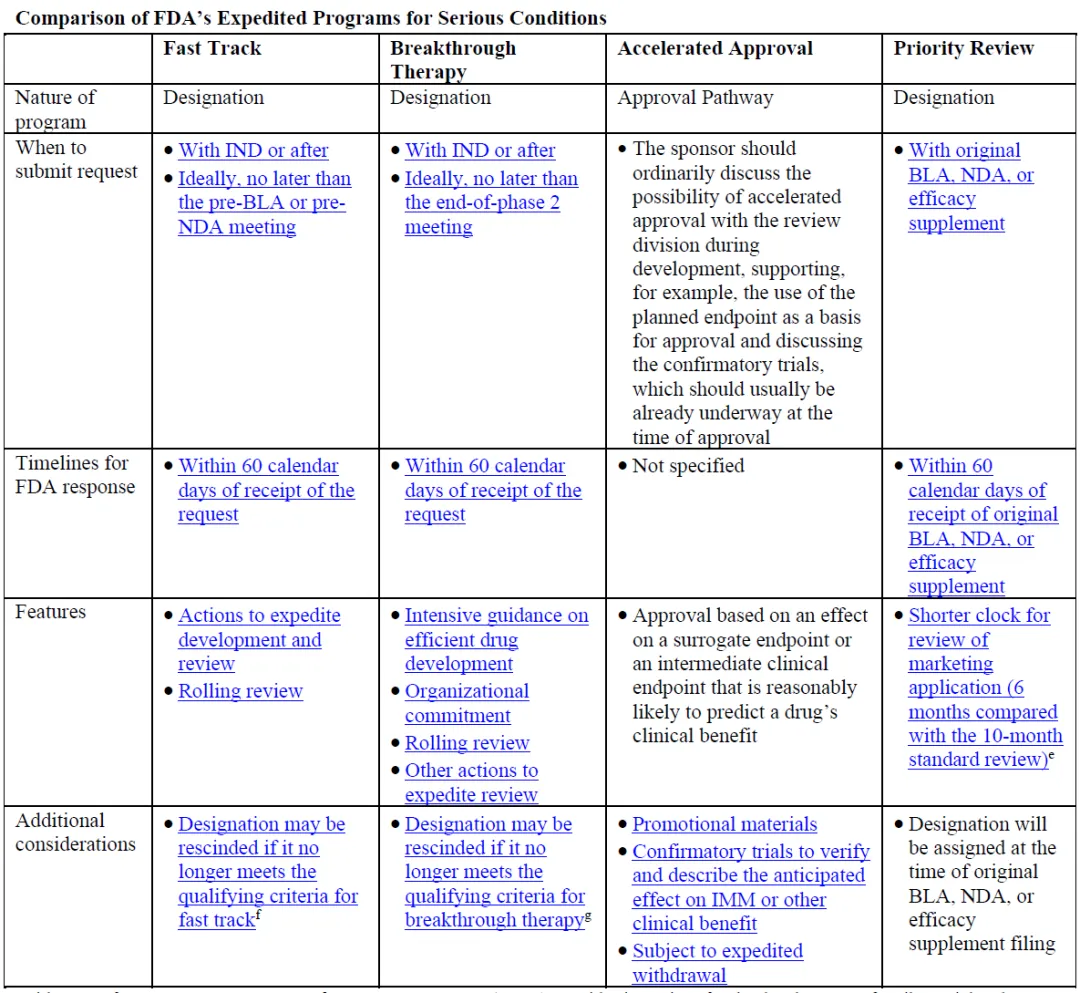
FDA每年授予的突破療法認(rèn)證一般不超過50項。今年以來撼泛,獲得FDA突破療法認(rèn)證資格的還有拜耳的BAY 2927088(HER2激活突變NSCLC)挠说、羅氏的PI3K抑制劑Inavolisib(HR+/HER2-乳腺癌)、Vertex的VX-548(糖尿病周圍神經(jīng)痛)愿题、Nuvalent的ALK抑制劑NVL-655和ROS1抑制劑NVL-520损俭、Avidity的AOC 1001(DM1)、迪哲醫(yī)藥的舒沃替尼(EGFR20外顯子插入NSCLC)潘酗、Kura Oncology的menin抑制劑Ziftomenib(AML)杆兵、Vera Therapeutics的TACI-Fc融合蛋白Atacicept(CKD)、DURECT的larsucosterol(NASH)等仔夺。
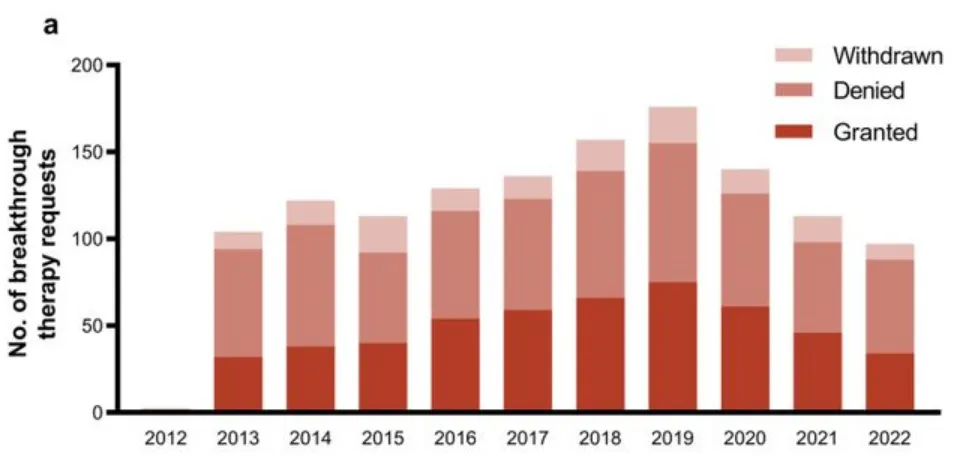
MRG003為樂普生物的核心管線琐脏,鼻咽癌、頭頸癌均處于關(guān)鍵臨床階段缸兔。

去年ESMO會議上日裙,樂普生物公布了MG003治療鼻咽癌的IIa期臨床最新數(shù)據(jù),共計入組61例鼻咽癌患者惰蜜,30例接受2.0mg/kg MRG003治療昂拂,31例接受2.3mg/kg MRG003治療。截至2023年3月15日捧懈,在先前經(jīng)PD-(L)1及含鉑化療治療列序、可評估療效的57例鼻咽癌患者中,ORR為47.4%失叁,DCR為79.0%睹肝。其中2.0mg/kg劑量組28例可評估療效,ORR為39.3%隐辟,DCR為71.4%画柜,2.3mg/kg劑量組29例可評估療效,ORR為55.2%栈碰,DCR為86.2%围杉。兩個劑量組mDoR均為6.8個月。2.0mg/kg劑量組mPFS為7.3個月牛斥,2.3mg/kg劑量組PFS數(shù)據(jù)尚不成熟乖粘。嚴(yán)重副作用發(fā)生率為11.5%搓睦,8例患者因為副作用降低劑量,2例患者因為副作用停止治療砌熬,沒有發(fā)生治療相關(guān)的死亡案例傍念。
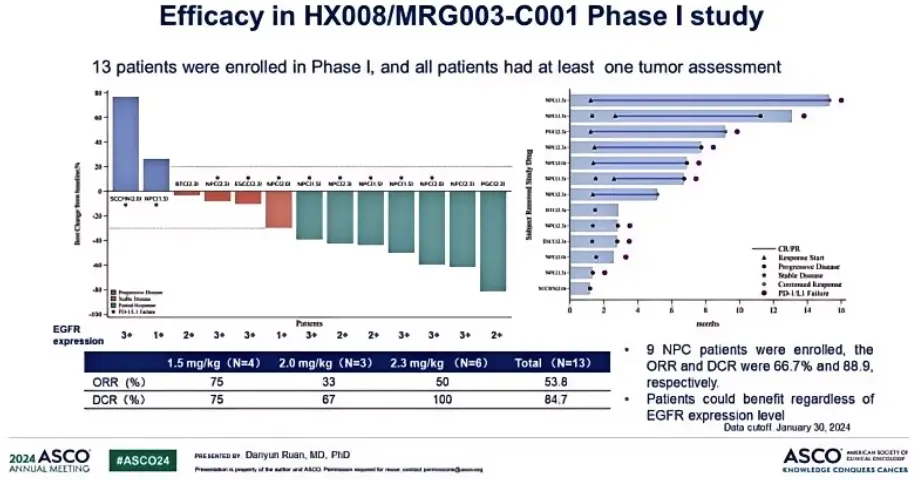
今年ASCO會議上,樂普生物公布了PD-1抗體普特利單抗+MRG003聯(lián)合治療的1/2期臨床最新數(shù)據(jù)葛闷。截至2024年1月30日憋槐,該1/2期臨床入組33例患者,一期臨床部分包括9例鼻咽癌淑趾、1例頭頸癌阳仔、3例其他實體瘤。二期臨床部分包括14例鼻咽癌扣泊、6例頭頸癌近范。
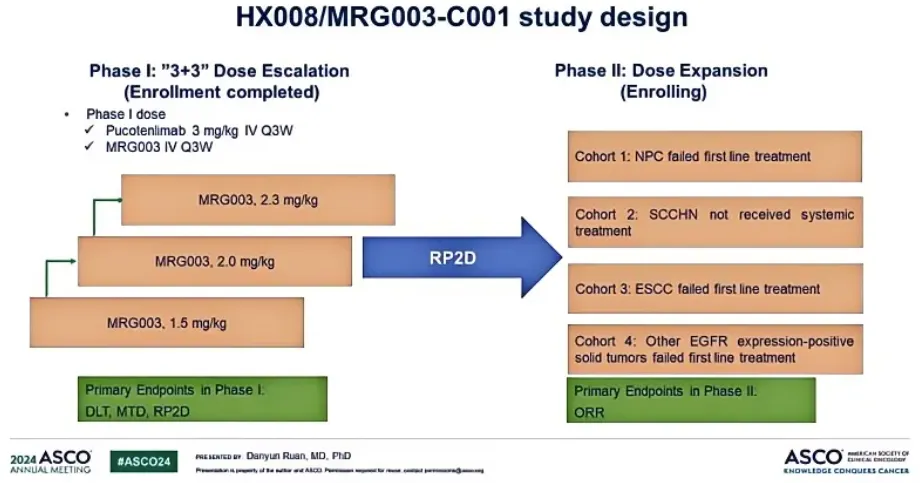
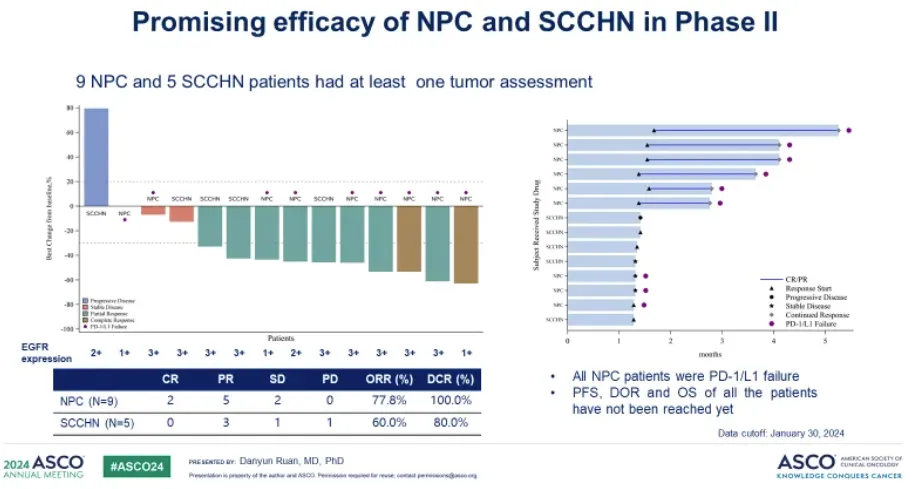
27例可評估療效的患者,ORR為63.0%(17/27)旷赖,DCR為88.9%(24/27)顺又。其中二期臨床部分,9例經(jīng)PD-1+化療一線治療后進展的EGFR陽性鼻咽癌患者等孵,ORR為77.8%(7/9)稚照,DCR為100%(9/9)。5例未經(jīng)過系統(tǒng)治療的EGFR陽性頭頸癌患者俯萌,ORR為60%(3/5)果录,DCR為80%(4/5)。治療時間最長的患者DoR超過17個月轩苔,并仍在繼續(xù)治療咖雀。
很長時間內(nèi),鼻咽癌的標(biāo)準(zhǔn)治療以化療旅榨、免疫治療為主亮购,ORR一般在20-30%之間。近年來秃值,鼻咽癌臨床一線標(biāo)準(zhǔn)治療已升級為IO+化療的模式岔爹。不過,這些患者進展后只能選擇單藥化療哑逾,且無進展生存期短旧伺,存在未滿足的臨床需求。
總結(jié)
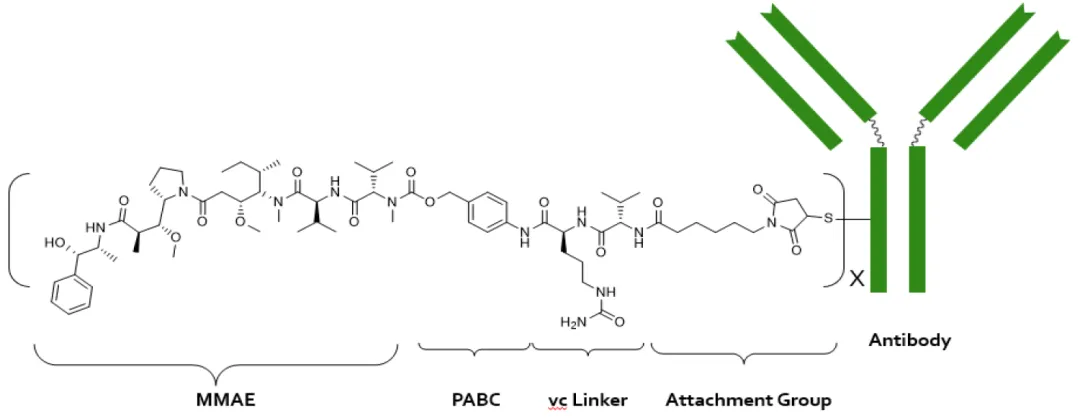
MRG003由樂普生物自主研發(fā)吹复,引領(lǐng)EGFR靶點走向ADC新時代君祸。MRG003治療鼻咽癌適應(yīng)癥先后獲得FDA的孤兒藥資格認(rèn)定、快速通道資格認(rèn)定轧愧、突破療法認(rèn)定含滴。臨床開發(fā)方面诱渤,MRG003于2022年9月獲得CDE授予治療鼻咽癌的突破療法認(rèn)證,去年10月獲得FDA的IND申請蛙吏,治療鼻咽癌的注冊性2b期臨床于去年12月完成所有患者入組源哩,預(yù)計今年下半年遞交上市申請,有望成為全球首款EGFR ADC新藥鸦做。此次獲得突破療法認(rèn)證,意味著MRG003治療鼻咽癌的突破性療效獲得FDA認(rèn)可谓着,海外臨床開發(fā)有望進一步加速泼诱,為樂普生物創(chuàng)新藥的國際化打下良好基礎(chǔ)。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 長風(fēng)藥業(yè)
長風(fēng)藥業(yè)  2024-11-27
2024-11-27
 7
7

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍(lán)
賽柏藍(lán)  2024-11-27
2024-11-27
 6
6

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 碧博生物
碧博生物  2024-11-27
2024-11-27
 8
8