
 政策法規(guī)
政策法規(guī)
 2017-06-02
2017-06-02
 4037
4037
根據(jù)總局《關(guān)于解決藥品注冊(cè)申請(qǐng)積壓實(shí)行優(yōu)先審評(píng)審批的意見》(食藥監(jiān)藥化管[2016]19號(hào))嘴父,我中心組織專家對(duì)申請(qǐng)優(yōu)先審評(píng)的藥品注冊(cè)申請(qǐng)進(jìn)行了審核論證例氓,現(xiàn)將擬優(yōu)先審評(píng)的藥品注冊(cè)申請(qǐng)及其申請(qǐng)人予以公示,公示期5日煎殷。公示期間如有異議蔼卡,請(qǐng)?jiān)谖抑行木W(wǎng)站“信息公開-->優(yōu)先審評(píng)公示-->擬優(yōu)先審評(píng)品種公示”欄目下提出異議喊崖。
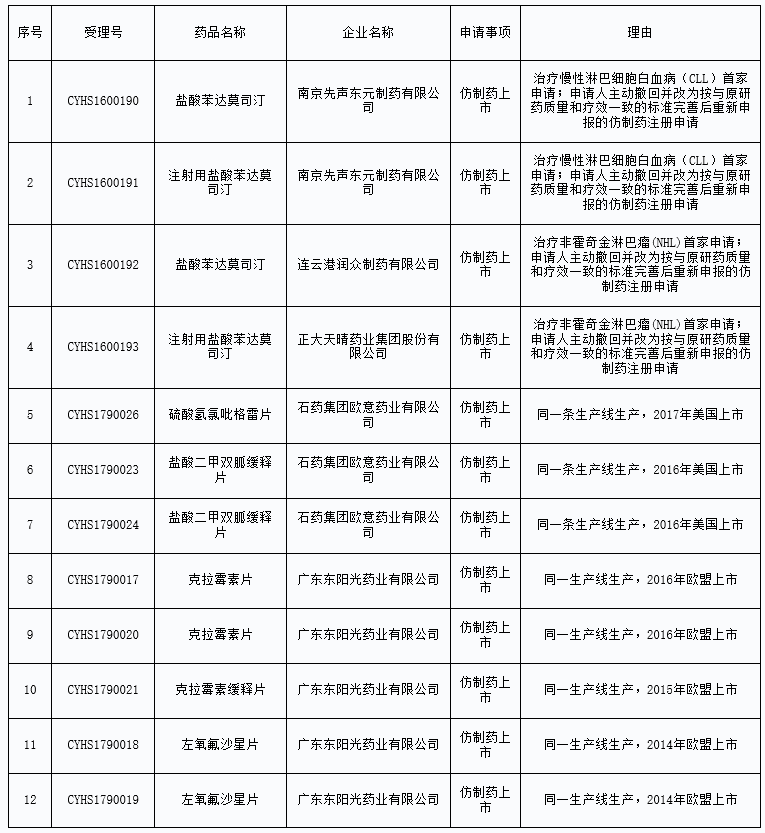
第十八批擬納入優(yōu)先審評(píng)程序藥品注冊(cè)申請(qǐng)公示名單如下:

 政策法規(guī)
政策法規(guī)
 CDE
CDE  2024-11-21
2024-11-21
 160
160

 政策法規(guī)
政策法規(guī)
 國家藥監(jiān)局
國家藥監(jiān)局  2024-10-24
2024-10-24
 211
211

 政策法規(guī)
政策法規(guī)
 廣東省人民政府
廣東省人民政府  2024-10-09
2024-10-09
 291
291
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽