
 產業(yè)資訊
產業(yè)資訊
 醫(yī)藥經濟報
醫(yī)藥經濟報  2024-08-08
2024-08-08
 342
342
CAR-T產品市場的潛力與價值,正在吸引越來越多的國內醫(yī)藥巨頭入場爱蚣!
日前,華東醫(yī)藥發(fā)布公告炊健,宣布其全資子公司華東醫(yī)藥(杭州)有限公司(以下簡稱“華東醫(yī)藥”)與北京藝妙神州醫(yī)藥科技有限公司(以下簡稱“藝妙神州”)正式簽訂了產品獨家商業(yè)化合作協議揽仔。

根據協議內容,華東醫(yī)藥將獲得藝妙神州研發(fā)的靶向CD19的自體CAR-T候選產品——IM19嵌合抗原受體T細胞注射液(簡稱“IM19注射液”)在中國大陸地區(qū)的獨家商業(yè)化權益挨狡。為此斯泥,華東醫(yī)藥將向藝妙神州支付1.25億元人民幣作為首付款,并承諾在達到注冊及銷售里程碑時支付最高不超過9.5億元人民幣的額外款項迫赞。
事實上啼阵,華東醫(yī)藥在此前已經將科濟藥業(yè)BCMA CAR-T產品賽愷澤(澤沃基奧侖賽注射液)收入囊中,本次出手CD19 CAR-T產品扑轮,價值導向非常明確:在市場推廣方面撤奸,將IM19 CAR-T細胞注射液與其現有的重點品種如賽愷澤等進行深度整合,共享專家網絡喊括、研究及臨床資源胧瓜。隨著國內大藥企陸續(xù)進場布局CAR-T,在復星郑什、藥明府喳、信達、華東等國內藥企聚集的賽道上蘑拯,誰將成為“卷王”钝满?
華東全面布局CAR-T
兩次出手機會幾何?
CAR-T療法通過從患者體內提取T細胞申窘,并在實驗室中進行基因編輯弯蚜,使其表達能特異性識別并攻擊腫瘤細胞表面抗原(例如CD19)的嵌合抗原受體(CAR)。經過改造的CAR-T細胞被重新注入患者體內后剃法,能夠精準識別并摧毀表達CD19的腫瘤細胞碎捺,實現治療目的。
作為藝妙神州的核心產品贷洲,IM19注射液針對在多種B細胞惡性腫瘤中廣泛表達的CD19抗原掖猬,布局了復發(fā)難治彌漫大B細胞淋巴瘤(r/r-DLBCL)、急性B淋巴細胞白血簿鞔巍(B-ALL)和套細胞淋巴瘤(MCL)三大適應癥凌宫。這些疾病因復發(fā)率高、預后差死辫,傳統(tǒng)治療手段往往難以達到理想效果麻坯,因此CAR-T療法的出現為這些患者提供了新的治療希望。
目前檬舀,IM19注射液的臨床研究已取得顯著進展毙帚。該產品已在中國開展針對上述三種適應癥的臨床試驗脓脸,其中針對彌漫大B細胞淋巴瘤末線治療的研究即將完成II期臨床試驗。初步數據顯示熔布,IM19注射液在治療復發(fā)或難治性彌漫大B細胞淋巴瘤患者中展現出良好的療效和安全性辐椎。
據悉,在已完成至少一次療效評估的59例患者中默徘,細胞因子釋放綜合征(CRS)和神經毒性(NT)的發(fā)生率分別為42%和7%恰岳,且未出現3-4級CRS或NT事件。在可評估有效性的患者中建芙,IM19注射液的最佳客觀緩解率達到了76%没隘。預計將于2024年四季度提交藥品上市許可申請。
此外禁荸,IM19注射液在急性B淋巴細胞白血病和套細胞淋巴瘤的研究也已進入關鍵階段右蒲。I期臨床試驗已順利完成所有受試者回輸,即將進入II期臨床試驗赶熟。特別值得一提的是瑰妄,B-ALL適應癥的前期非注冊臨床研究顯示,IM19單次回輸治療復發(fā)難治的B-ALL患者完全緩解率達到97.5%映砖,且安全性良好间坐。
此次華東醫(yī)藥與藝妙神州的合作,無疑具有深遠的意義邑退。華東醫(yī)藥將獲得IM19注射液在中國大陸地區(qū)的獨家商業(yè)化權益竹宋,這一合作將進一步豐富其在血液腫瘤領域的產品管線,并顯著提升市場競爭力瓜饥。
同時,藝妙神州將借助華東醫(yī)藥豐富的商業(yè)化經驗和市場覆蓋能力浴骂,加速IM19注射液的商業(yè)化進程快混,以滿足國內B細胞血液腫瘤患者的迫切需求。雙方的合作不僅將推動國產CAR-T細胞治療藥物的發(fā)展能航,還將為腫瘤患者提供更多穿互、更好的治療選擇。
值得一提的是挚蟹,華東醫(yī)藥在CAR-T市場的布局早有動作峡徽。去年年初,華東醫(yī)藥以“2億元首付款+最高不超過10.25億元人民幣的注冊及銷售里程碑付款”成功引進科濟藥業(yè)BCMA CAR-T產品澤沃基奧侖賽注射液的中國大陸獨家商業(yè)化權益木影。該產品已于今年3月獲批绣首,用于治療復發(fā)或難治性多發(fā)性骨髓瘤成人患者。
作為國產第二款上市的BCMA CAR-T產品璃淤,澤沃基奧侖賽注射液的上市不僅豐富了華東醫(yī)藥的產品線施旱,也進一步鞏固了公司在血液腫瘤治療領域的地位唬辛。上市后,市場反應熱烈乌迎,患者與醫(yī)療專業(yè)人士均對其療效寄予厚望泉扛。
行業(yè)內普遍認為,華東醫(yī)藥通過引進外部優(yōu)質CAR-T產品区转,并結合自身強大的商業(yè)化能力苔巨,迅速切入CAR-T市場。作為國內較早布局CAR-T市場的企業(yè)之一废离,華東醫(yī)藥憑借澤沃基奧侖賽注射液和IM19 CAR-T細胞注射液的成功引進和商業(yè)化侄泽,已經在國內CAR-T市場占據了一席之地。
多款產品競相上市
國內市場“開卷”
隨著人口老齡化厅缺、飲食環(huán)境變化等多重因素的影響蔬顾,癌癥發(fā)病率持續(xù)攀升,對更為有效的治療方案需求日益迫切湘捎。在此背景下诀豁,CAR-T細胞療法作為一種新興的治療手段,盡管尚未實現大面積推廣和應用窥妇,但其顯著的療效和個體化定制的優(yōu)勢已預示著巨大的市場增長潛力舷胜。
據統(tǒng)計,截至目前活翩,全球范圍內共有11款CAR-T產品獲批上市烹骨,其中中國占據5席,具體包括三款CD19 CAR-T產品和兩款BCMA CAR-T產品矩袖。
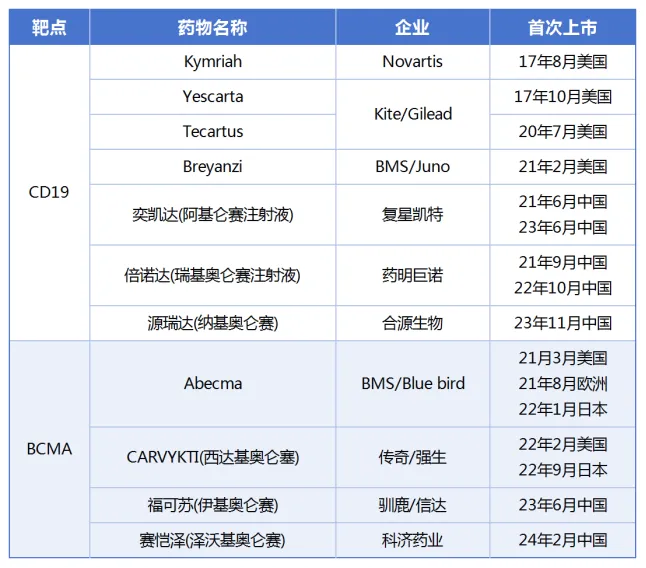
CD19作為表達于B淋巴細胞及濾泡樹突狀細胞表面的重要蛋白陵阁,是免疫球蛋白(Ig)超家族的一員。它通過B細胞受體(BCR)依賴和非依賴方式拖牢,在B細胞的發(fā)育锹鹉、增殖和分化過程中發(fā)揮關鍵的調節(jié)作用。目前浦忠,臨床上針對CD19為靶點的治療惡性腫瘤的主要手段包括嵌合抗原受體T細胞(CAR-T)療法和抗體偶聯藥物(ADCs)塑满。
在CD19 CAR-T產品方面,中國已取得了顯著進展韩记。去年年底硫联,合源生物自主研發(fā)的納基奧侖賽注射液成功在中國獲批上市,這款產品不僅是中國首款具有全自主知識產權的CD19 CAR-T細胞治療產品喂交,同時也是中國首款獲批上市的治療白血病的CAR-T產品援仍。其獨特的CD19 scFv(HI19a)結構和國際領先的生產制造工藝,在成人r/r B-ALL注冊臨床研究中展現出了100%的生產成功率察夕。
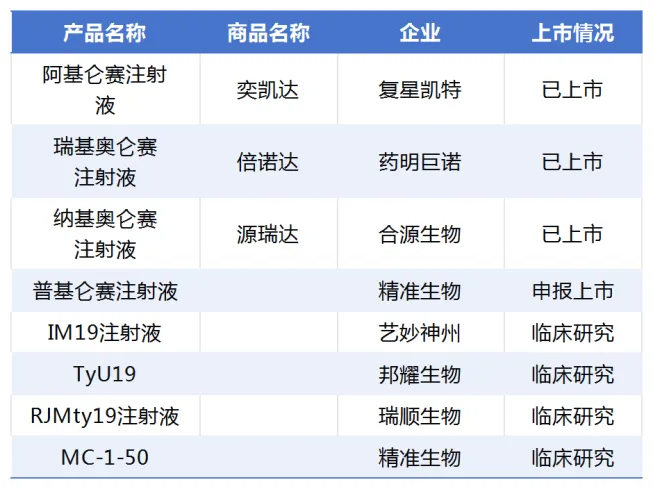
目前亿永,中國市場上已有三款CD19 CAR-T產品掠廓,分別是復星凱特的阿基侖賽注射液、藥明巨諾的瑞基奧侖賽注射液以及合源生物的納基奧侖賽注射液甩恼。
前不久蟀瞧,重慶精準生物CD19 CAR-T療法普基侖賽注射液的上市申請獲得NMPA受理。公開資料顯示条摸,普基侖賽注射液由精準生物自主研發(fā)悦污,是針對CD19陽性B細胞起源的惡性血液系統(tǒng)疾病而開發(fā)的CAR-T細胞免疫治療產品。該產品對CAR結構進行了優(yōu)化钉蒲,同時采用更為安全的基因轉導載體系統(tǒng)切端,從而使其具有潛在更好的有效性和安全性。
普基侖賽注射液用于兒童顷啼、青少年B細胞急性淋巴細胞白血蔡ぴ妗(B-ALL)適應癥于2019年在中國獲批開展注冊臨床研究。根據早前公布的1期注冊臨床數據钙蒙,入組的9例患者均獲得完全緩解(CR)茵瀑,總體緩解率達100%,且首次達到完全緩解(CR)的患者微小殘留病變也均為陰性躬厌,且總體安全性和耐受性良好煤蔚。除了白血病,普基侖賽注射液也在開展用于治療彌漫大B細胞淋巴瘤坠狈、濾泡性淋巴瘤谦枢、套細胞淋巴瘤的研究。
此外墙冻,據不完全統(tǒng)計怕茉,還有多款CD19 CAR-T產品正在中國進行臨床研究,包括藝妙神州的IM19奏尽、邦耀生物開發(fā)的靶向CD19抗原的異體通用型CAR-T細胞治療產品TyU19榨豹、廣東瑞順生物技術有限公司的RJMty19注射液、重慶精準生物技術有限公司的MC-1-50細胞制劑原承。
與此同時碳环,多發(fā)性骨髓瘤作為一種難治性的惡性漿細胞疾病矮蘑,其患病人數在中國將持續(xù)增加废奖。據Frost & Sullivan估計,2023年中國多發(fā)性骨髓瘤的患病人數約為15.3萬人置塘,新發(fā)病例數為2.32萬人内地。預計到2030年,中國多發(fā)性骨髓瘤的患病人數將增長至26.63萬人赋除。而B細胞成熟抗原(BCMA)作為CAR-T治療多發(fā)性骨髓瘤(MM)使用最廣泛阱缓、最成熟的靶點非凌,正受到廣泛關注。
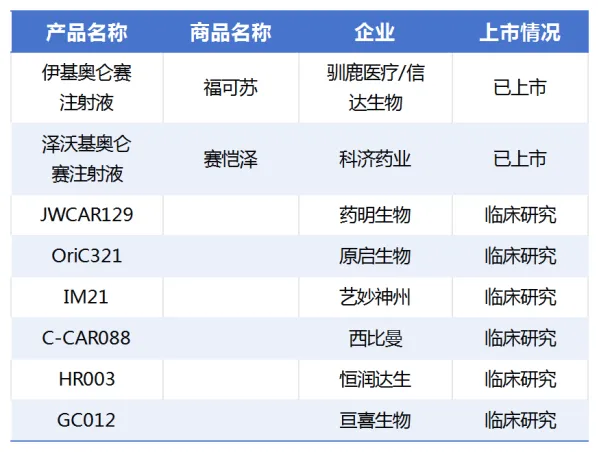
2023年6月荆针,馴鹿生物與信達生物合作開發(fā)的伊基侖賽注射液獲批上市敞嗡,成為首款在中國獲批的BCMA靶點CAR-T療法,用于治療復發(fā)/難治性多發(fā)性骨髓瘤(R/R MM)航背。
隨后喉悴,科濟藥業(yè)的澤沃基奧侖賽注射液也獲得了NMPA的新藥上市批準,這是一款用于治療復發(fā)/難治多發(fā)性骨髓瘤的自體BCMA靶向CAR-T細胞產品玖媚。其不俗的療效數據吸引了華東醫(yī)藥的目光箕肃,后者以2億人民幣的首付款及最高不超過10.25億元的注冊及銷售里程碑付款,獲得了澤沃基奧侖賽在中國大陸的獨家商業(yè)化權益今魔。
在全球范圍內勺像,BCMA作為多發(fā)性骨髓瘤的重要靶點,正成為CAR-T領域的競爭焦點错森。除了馴鹿生物的伊基侖賽注射液外痛但,BMS/藍鳥生物的Abecma和強生/傳奇生物的Carvykti也已被美國FDA批準用于治療既往接受過多種療法的R/R MM成人患者。值得一提的是翎女,Carvykti由傳奇生物自主研發(fā)攘宝,是首個國內自主研發(fā)并在海外獲批上市的細胞療法。
在國內酸飞,仍有多款在研BCMA靶向CAR-T療法處于臨床推進開發(fā)中下驴,如亙喜生物的GC012、恒潤達生的HR003等央封。由此可見赛臀,CAR-T作為一種革命性的細胞治療方法,在腫瘤治療領域展現出了巨大的市場潛力徐渗。
近年來丰扁,CAR-T療法的市場規(guī)模迅速增長。據市場研究報告顯示店麻,全球CAR-T市場規(guī)模已從2017年的0.1億美元增長至2023年的數十億美元纽哭,并預計在未來幾年內保持高速增長態(tài)勢。中國作為全球癌癥高發(fā)國家之一坐求,對CAR-T技術的需求尤為迫切蚕泽,市場增長潛力巨大。據預測桥嗤,到2030年须妻,中國CAR-T市場規(guī)模有望達到數百億元人民幣。
當前泛领,國內CAR-T市場的商業(yè)化合作正處于快速發(fā)展階段荒吏×簿跨國藥企通過引進海外成熟產品并在中國進行本地化生產,快速占領市場绰更;而本土企業(yè)則通過自主研發(fā)和臨床試驗推動國產CAR-T產品的上市進程瞧挤。
此外,國內企業(yè)之間以及企業(yè)與科研機構儡湾、醫(yī)療機構之間的合作也日益頻繁皿伺,共同推動CAR-T技術的產業(yè)化發(fā)展。如復星凱特盒粮、藥明巨諾鸵鸥、傳奇生物等,均通過自主研發(fā)和臨床試驗推動國產CAR-T產品的上市進程嘶在。同時护忠,還有眾多處于研發(fā)階段的初創(chuàng)企業(yè)也在積極參與這一領域。
行業(yè)內人士指出扎趋,國內CAR-T市場參與者眾多前茧,包括大型跨國藥企如諾華、吉利德等莲态,以及眾多本土創(chuàng)新企業(yè)丰浙。這些企業(yè)紛紛加大研發(fā)投入,推動CAR-T產品的研發(fā)和商業(yè)化進程秤凡。然而袄映,隨著市場參與者的增加,競爭也日益激烈丘登,內卷現象逐漸顯現泽姨。

 產業(yè)資訊
產業(yè)資訊
 凱萊英藥聞
凱萊英藥聞  2024-11-22
2024-11-22
 109
109

 產業(yè)資訊
產業(yè)資訊
 動脈網
動脈網  2024-11-22
2024-11-22
 105
105

 產業(yè)資訊
產業(yè)資訊
 藥明康德
藥明康德  2024-11-22
2024-11-22
 119
119