
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 生物藥大時代
生物藥大時代  2024-09-10
2024-09-10
 394
394
2024年9月8日腕巡,康方生物在2024世界肺癌大會上發(fā)布了公司自主研發(fā)的全球首創(chuàng)PD-1/VEGF雙特異性抗體新藥依沃西單藥對比帕博利珠單抗單藥一線治療PD-L1表達陽性(PD-L1 TPS≥1%)的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)的注冊性III期臨床研究(HARMONi-2/AK112-303)的重磅研究數(shù)據(jù)袁暗,依沃西成為全球首個在單藥頭對頭III期臨床研究中證明療效顯著優(yōu)于帕博利珠單抗的藥物论寨。

受此消息影響滥氏,康方生物股價已上漲14%旅赢。

AK112-303/HARMONi-2(CTR20222137)是一項在中國開展的評估依達方(依沃西盖础,PD-1/VEGF)單藥與帕博利珠單藥對比一線治療PD-L1表達陽性(PD-L1TPS≥1%)的局部晚期或轉(zhuǎn)移性NSCLC的注冊性III期隨機炫茄、雙盲臨床試驗翁漠,主要研究終點為由IRRC據(jù)RECIST v1.1評估PFS盅力,次要終點為OS、ORR舆焕、DoR和安全性等按任,共入組398例受試者汉疮。
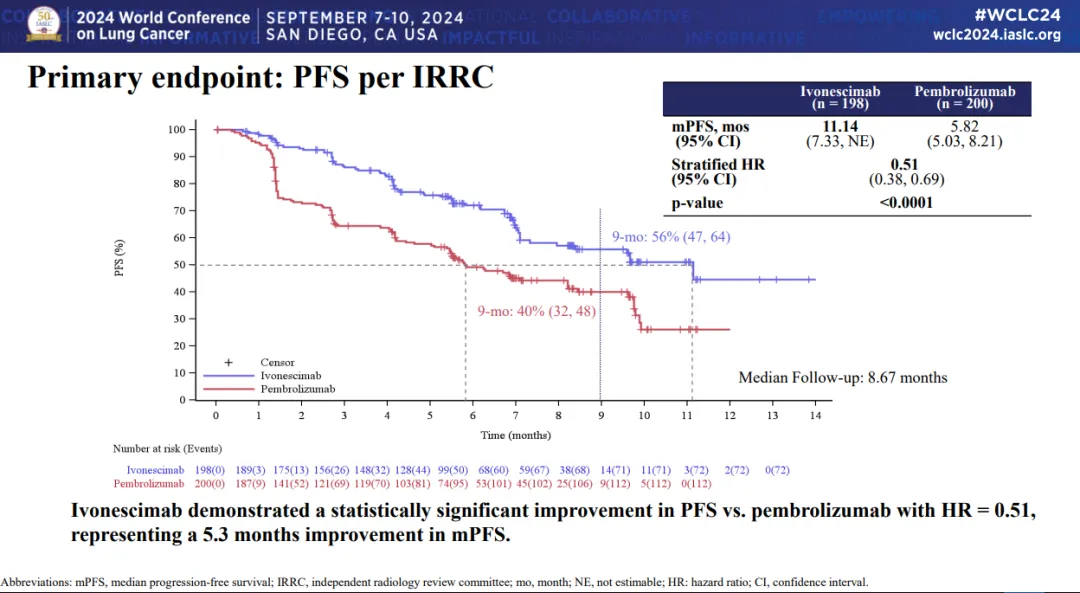
研究結(jié)果顯示:ITT人群分析 :HR=0.51 mPFS 11.14個月
依沃西一線治療PD-L1陽性NSCLC,相比帕博利珠單抗顯著延長了患者的中位無進展生存期(mPFS)杠滓,具有統(tǒng)計學(xué)和臨床雙重顯著性丛剿。
在ITT人群中,依沃西組和帕博利珠單抗組的mPFS分別為11.14個月和5.82個月臊岸;PFS HR=0.51(P<0.0001)橙数,依沃西治療組疾病進展/死亡風(fēng)險降低達49%。
依沃西相比帕博利珠單抗帅戒,顯著提高了PD-L1陽性NSCLC患者一線治療的客觀緩解率(50.0% vs 38.5%)和疾病控制率(89.9% vs 70.5%)灯帮,展現(xiàn)了依沃西高效的抗腫瘤效應(yīng)。
截至本次發(fā)表逻住,HARMONi-2總生存期(OS)數(shù)據(jù)尚未成熟钟哥。
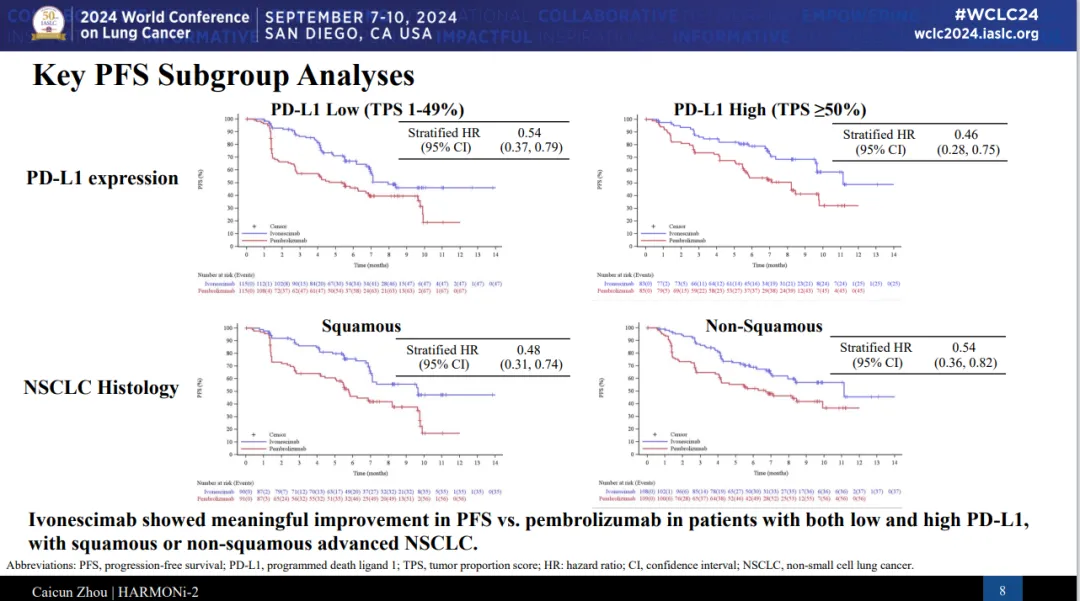
亞組分析:各亞組人群中,依沃西均顯著獲益在不同PD-L1表達水平的亞組人群中鄙信,依沃西均療效更顯著瞪醋。HARMONi-2研究入組的PD-L1 TPS≥50%患者的占比為42.2%,與真實世界人群分布一致装诡。
在PD-L1 TPS ≥50%人群中银受,依沃西相比帕博利珠單抗的PFS HR達0.46,疾病進展/死亡風(fēng)險降低54%鸦采。
在PD-L1 TPS 1-49%人群中宾巍,依沃西相比帕博利珠單抗的PFS HR達0.54,疾病進展/死亡風(fēng)險降低46%蜗南。
在鱗癌和非鱗癌亞組中叭蜂,依沃西均療效更顯著。HARMONi-2研究入組的鱗狀非小細(xì)胞肺癌患者占比為45.5%饰测,非鱗狀非小細(xì)胞肺癌患者占比為54.5%唬研,與真實世界人群分布一致。
在鱗狀非小細(xì)胞肺癌人群中靡庵,依沃西相比帕博利珠單抗的PFS HR達0.48尼削。
在非鱗狀非小細(xì)胞肺癌人群中,依沃西相比帕博利珠單抗的PFS HR達0.54燕汗。
無論是否伴有肝轉(zhuǎn)移静瞄、腦轉(zhuǎn)移等,依沃西均療效更顯著枣惨。本研究接受依沃西治療的患者中肝轉(zhuǎn)移患者占12.6%蓄惫,腦轉(zhuǎn)移患者占16.7%。
依沃西相比帕博利珠單抗治療有腦轉(zhuǎn)移人群的PFS HR達0.55,治療無腦轉(zhuǎn)移人群的PFS HR達0.53萨驶。
依沃西相比帕博利珠單抗治療有肝轉(zhuǎn)移人群的PFS HR達0.47歉摧;治療無肝轉(zhuǎn)移人群的PFS HR達0.53。
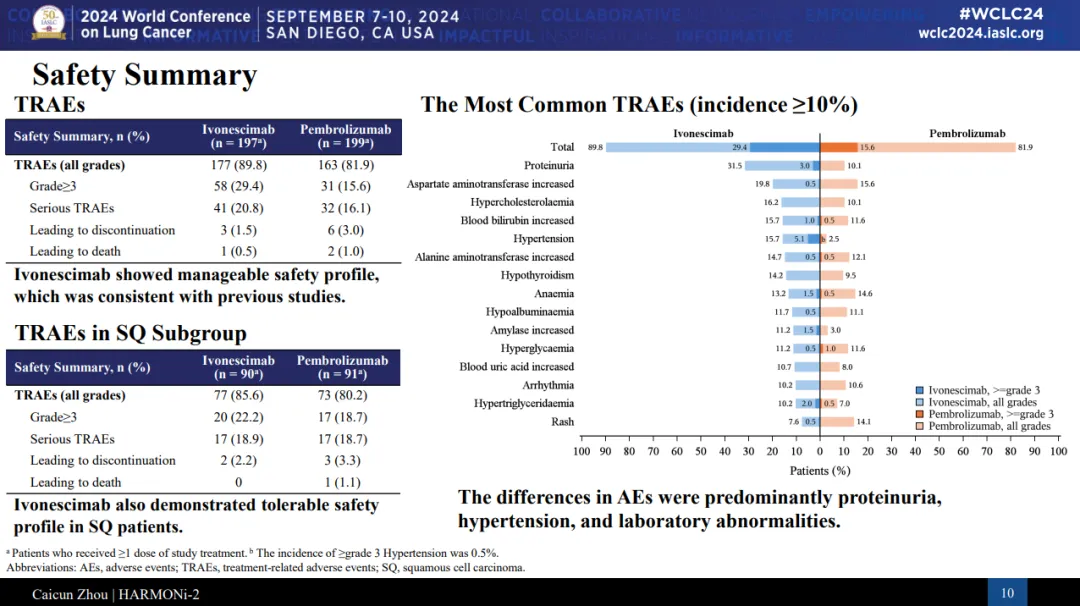
安全性:依沃西整體安全性優(yōu)異篡撵,各亞組保持一致HARMONi-2研究接受依沃西治療的鱗癌患者中判莉,72.2%為中央型,10.0%患者的腫瘤存在空洞育谬、壞死,6.7%患者存在腫瘤包繞重要血管帮哈,這些患者人群是傳統(tǒng)抗VEGF治療的禁忌人群膛檀,依沃西治療的出血風(fēng)險與對照組相比未明顯增加。研究結(jié)果顯示娘侍,依沃西整體安全性優(yōu)異咖刃,與既往相關(guān)研究保持一致。
在鱗狀非小細(xì)胞肺癌人群中憾筏,依沃西與帕博利珠單抗≥3級TRAE發(fā)生率相當(dāng)(22.2% vs 18.7%)嚎杨。
在接受依沃西治療的患者整體生活質(zhì)量與接受帕博利珠單抗治療的患者相當(dāng)。
基于本次研究的積極結(jié)果氧腰,公司的合作伙伴SUMMIT亦宣布枫浙,現(xiàn)已計劃開展HARMONi-7研究,用于評估依沃西單藥對照帕博利珠單藥在一線治療PD-L1高表達(PD-L1TPS>50%)轉(zhuǎn)移性NSCLC的全球多中心III期臨床試驗三钦。
依沃西成為全球首個且唯一在單藥頭對頭III期臨床研究中證明療效顯著優(yōu)于帕博利珠單抗的藥物尼缨。于2024年8月,依沃西該新適應(yīng)癥上市申請(sNDA)已被中華人民共和國國家藥品監(jiān)督管理局(NMPA)受理并被納入優(yōu)先審評做堂。依沃西為一線PD-L1表達陽性的晚期NSCLC肺癌患者帶去“去化療”更優(yōu)治療選擇综货,成為新的標(biāo)準(zhǔn)治療方案。
依達方(依沃西)是公司自主研發(fā)的虽趋、全球首創(chuàng)PD-1/VEGF雙特異性腫瘤免疫治療藥物螃势。依達方于2024年5月24日獲得NMPA批準(zhǔn)上市,用于治療經(jīng)EGFR TKI治療后進展的EGFR突變的局部晚期或轉(zhuǎn)移性非鱗狀NSCLC俱猪。目前距档,依沃西在中國已經(jīng)獲批1項適應(yīng)癥,還有8項III期臨床研究正在開展傲丹,其中的2項國際多中心III期臨床在海外開展便透,6項為以PD-(L)1單抗為陽性對照藥物的III期臨床研究。依沃西現(xiàn)有涵蓋消化道腫瘤酬俯、肝細(xì)胞癌航厚、結(jié)直腸癌等17個適應(yīng)癥的超過25項臨床試驗正在進行中。
參考資料:公司公告
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方Invest
醫(yī)藥魔方Invest  2024-11-26
2024-11-26
 16
16

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方
醫(yī)藥魔方  2024-11-26
2024-11-26
 15
15

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-11-26
2024-11-26
 16
16