
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Insight數(shù)據(jù)庫
Insight數(shù)據(jù)庫  2024-09-10
2024-09-10
 292
292
2024 年歐洲腫瘤內(nèi)科學(xué)會(ESMO)年會將于當(dāng)?shù)貢r間 9 月 13 日至 17 日在西班牙巴塞羅那召開辖备。恒瑞將在本次會議上以口頭報告的形式首次公布 CLDN18.2 ADC 藥物 SHR-A1904 治療胃或胃食管交界處癌(GC/GEJC)的 I 期研究結(jié)果凯书,目前該結(jié)果的摘要已經(jīng)公布坡沿。
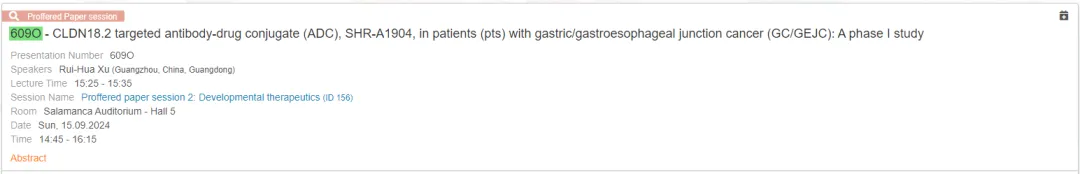
圖片來源:ESMO 官網(wǎng)
數(shù)據(jù)顯示墅糯,在基線和≥1 次基線后評估的患者中,6.0 mg/kg 劑量組中款筑,ORR 和 DCR 分別為 55.6% (5/9祝懂;95%CI, 21.2-86.3) 和 88.9% (8/9;95%CI, 51.8-99.7)坠敷;8.0 mg/kg 劑量組中汹涯,ORR 和 DCR 分別為和 36.7% (11/30;95%CI, 19.9-56.1) 和 86.7% (26/30数屁;95%CI, 69.3-96.2)片侧。
這是一項開放、單臂透格、多中心的 I 期臨床研究(NCT04877717)微悬,以評估 SHR-A1904 用于標(biāo)準(zhǔn)治療失敗或未接受標(biāo)準(zhǔn)治療的晚期實體瘤患者中的作用。本次大會報告了該藥在 CLDN18.2+ GC/GEJC 患者的結(jié)果韭拙。
截至 2024 年 3 月 18 日沙诅,共有 73 例 GC/GEJC 患者入組。98.6% 的患者發(fā)生轉(zhuǎn)移祥扒,31.5% 的患者接受了≥3 種治療 (中位數(shù)為 2 種)草仪。
29 名患者中有 3 名在劑量遞增期間報告了 DLT,包括 9 名患者中有 2 名在 4.8 mg/kg(3 級發(fā)熱性中性粒細(xì)胞減少癥和 3 級血膽紅素升高) 和 6 名患者中有 1 名在 6.0 mg/kg(3 級胃粘膜病變)鼻蟆。本研究未達(dá)到最大耐受劑量(MTD)振害。選擇 6.0 和 8.0 mg/kg 進(jìn)行擴(kuò)展,另外入組 44 名患者匀油。
單次劑量后缘缚,SHR-A1904 暴露量和總抗體在 0.6-8.0 mg/kg 之間約成比例增加。SHR-A1904 的平均 t1/2 為 6.0 mg/kg 時 6.5 d, 8.0 mg/kg 時 6.0 d敌蚜。
總體而言桥滨,53.4%(39/73) 的患者發(fā)生≥3 級治療相關(guān)不良事件,其中最常見的 (≥10%) 是白細(xì)胞計數(shù)減少钝侠、中性粒細(xì)胞計數(shù)減少和貧血该园。
SHR-A1904 是一種新型 ADC,由靶向 CLDN18.2 的 IgG1 單抗帅韧、可切割連接體和拓?fù)洚悩?gòu)酶 I 抑制劑載荷組成里初。目前已經(jīng)在國內(nèi)啟動一項聯(lián)合 PD-L1(阿得貝利單抗)和化療用于實體瘤的 III 期臨床啃勉。
總之,SHR-A1904 在經(jīng)治的 CLDN18.2 陽性胃腺癌/胃食管交界處癌患者中顯示出可管理的安全性概況和有希望的抗腫瘤活性双妨。
Insight 數(shù)據(jù)庫顯示淮阐,目前全球在研處于活躍狀態(tài)的 CLDN18.2 ADC 藥物共 23 款,其中中國企業(yè)有 19 款刁品,全球尚無已獲批上市的產(chǎn)品泣特。其中,進(jìn)展到 III 期臨床階段的除了恒瑞的 SHR-A1904 外凡宅,還有信達(dá)生物的 IBI343谆威、禮新醫(yī)藥的 TPX-4589、樂普生物/康諾亞的 CMG901钓闲。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方Invest
醫(yī)藥魔方Invest  2024-11-26
2024-11-26
 16
16

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方
醫(yī)藥魔方  2024-11-26
2024-11-26
 16
16

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-11-26
2024-11-26
 16
16
 熱門資訊
熱門資訊