
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 中國光谷
中國光谷  2024-09-14
2024-09-14
 312
312
近日誓酒,光谷企業(yè)——武漢禾元生物科技股份有限公司(簡稱“禾元生物”)宣布集炭,其自主研發(fā)的治療用生物制品Ⅰ類創(chuàng)新藥——奧福民?(植物源重組人血清白蛋白注射液)崎弃,獲國家藥品監(jiān)督管理局新藥注冊申請(NDA)受理捕阅,并進入優(yōu)先審評審批“綠色通道”跋核。產(chǎn)品有望在2025年獲批上市贰漱。
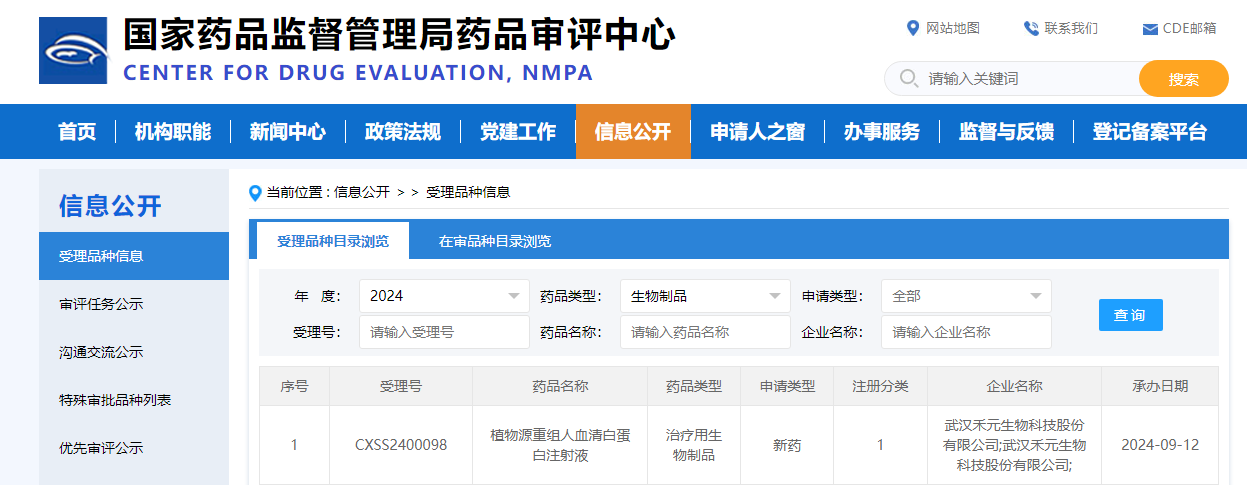
“綠色通道”是創(chuàng)新藥能夠加快進入市場的重要標志秦砌。經(jīng)國家藥品監(jiān)督管理局藥品審評中心審核摊壳,奧福民?符合《藥品注冊管理辦法》和《國家藥監(jiān)局關于發(fā)布<突破性治療藥物審評工作程序(試行)>等三個文件的公告》有關要求酬楚,同意按優(yōu)先審評范圍“(一)臨床急需的短缺藥品、防治重大傳染病和罕見病等疾病的創(chuàng)新藥和改良型新藥”納入優(yōu)先審評審批程序粒颂。
也就是說谜珠,奧福民?進入“綠色通道”后,上市注冊申請的審評時限由常規(guī)程序的200個工作日縮短至130工作日仑萧。
人血清白蛋白俗稱“黃金救命藥”士修,在臨床中廣泛用于治療失血、肝硬化等病癥樱衷。禾元生物董事長楊代常介紹:“目前國內(nèi)人血清白蛋白年需求量約1000噸棋嘲,國內(nèi)均來自血漿提取酒唉。因血漿短缺,我國60%以上人血清白蛋白供應長期依賴進口封字∏荩”
為此,2006年阔籽,禾元生物在光谷生物城成立流妻,致力于研究和開發(fā)全球首個重組人血清白蛋白,用“稻米造血”——使稻米在生長過程中自動合成人血清白蛋白笆制,然后通過多道工序提取純化绅这。

創(chuàng)新藥要想惠及百姓,不僅要實現(xiàn)從0到1在辆,還要實現(xiàn)1到100证薇。2023年,禾元生物在光谷建成年產(chǎn)能10噸原液(100萬瓶注射液)的智能化工廠匆篓,并獲得藥品生產(chǎn)許可證猬肖。今年,禾元生物即將啟動植物源重組人血清白蛋白產(chǎn)業(yè)化基地建設猾妖,建成后年產(chǎn)預計達到120噸原液(1200萬瓶注射液)函以,產(chǎn)值突破50億元。
“傳統(tǒng)白蛋白每瓶要400-500元啼脑。這款新藥若能大規(guī)模生產(chǎn)轨畏,將有望降低患者用藥成本×钐唬”楊代常說瞄隶。
東湖高新區(qū)相關負責人介紹,禾元生物是最早入駐光谷生物城的企業(yè)之一程蠕。除植物源重組人血清白蛋白外第讯,光谷生物城內(nèi)企業(yè)現(xiàn)有一類創(chuàng)新藥在研管線近200個,其中近百個創(chuàng)新藥進入臨床試驗辣铡。未來璃璧,東湖高新區(qū)將堅持培育創(chuàng)新藥重磅品種,布局重組蛋白刊愚、抗體藥踊跟、溶瘤病毒等賽道,發(fā)展生物醫(yī)藥新質(zhì)生產(chǎn)力鸥诽。
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方Invest
醫(yī)藥魔方Invest  2024-11-26
2024-11-26
 3
3

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方
醫(yī)藥魔方  2024-11-26
2024-11-26
 4
4

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-11-26
2024-11-26
 4
4