
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2021-09-17
2021-09-17
 2396
2396
今日铡急,武田(Takeda)公司宣布董翻,美國(guó)FDA已加速批準(zhǔn)其口服酪氨酸激酶抑制劑Exkivity(mobocertinib)上市熔布,用于治療攜帶EGFR外顯子20插入突變的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)患者聚假。他們?cè)诮邮芎K化療治療中或治療后疾病出現(xiàn)進(jìn)展掘鱼。新聞稿指出快耿,這是美國(guó)FDA批準(zhǔn)的首款專門為攜帶EGFR外顯子20插入突變的NSCLC患者設(shè)計(jì)的口服療法糯彬。

FDA的批準(zhǔn)是基于在1/2期臨床試驗(yàn)中曾接受過含鉑化療治療的患者群體。在今年ASCO年會(huì)上公布的數(shù)據(jù)顯示忿峻,根據(jù)獨(dú)立數(shù)據(jù)監(jiān)控中心的評(píng)估薄啥,mobocertinib達(dá)到28%的確認(rèn)客觀緩解率,中位緩解持續(xù)時(shí)間為17.5個(gè)月逛尚,中位總生存期為24個(gè)月垄惧,中位無進(jìn)展生存期為7.3個(gè)月刁愿。
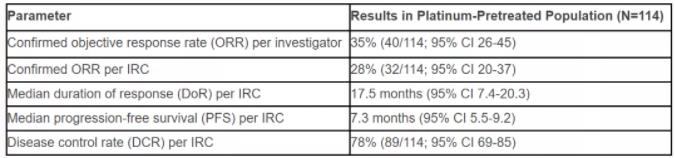
▲Mobocertinib的1/2期臨床試驗(yàn)結(jié)果(圖片來源:參考資料[2])
非小細(xì)胞肺癌是最常見的一種肺癌,據(jù)世界衛(wèi)生組織統(tǒng)計(jì)搜计,約占全球每年新診斷肺癌病例的85%宋旭。EGFR外顯子20插入陽性的轉(zhuǎn)移性NSCLC患者約占NSCLC患者的1-2%,該疾病在亞洲人群中更常見杉藐。這類患者比其他EGFR突變的預(yù)后更差枯橱。現(xiàn)有的EGFR酪氨酸激酶抑制劑和化療為這些患者提供的益處有限。
Mobocertinib是一種專門設(shè)計(jì)用于選擇性靶向EGFR外顯子20插入突變的強(qiáng)效口服小分子酪氨酸激酶抑制劑攒置。它在2020年4月獲得FDA授予的突破性療法認(rèn)定粹岁,用于治療含鉑化療期間或之后疾病進(jìn)展的EGFR外顯子20插入陽性轉(zhuǎn)移性NSCLC患者。2020年10月尖坦,mobocertinib在中國(guó)被藥品審評(píng)中心(CDE)指定為突破性治療產(chǎn)品骂领。今年5月,它在中國(guó)被擬納入優(yōu)先審評(píng)装屈。
“Exkivity的獲批為攜帶EGFR外顯子20插入突變的NSCLC患者提供了一個(gè)新的有效治療選擇怒晕,填補(bǔ)了這一難于治療癌癥患者的迫切需求°嫡ǎ”武田全球腫瘤學(xué)業(yè)務(wù)部總裁Teresa Bitetti女士說。
參考資料:

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 9
9

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方Info
醫(yī)藥魔方Info  2024-11-25
2024-11-25
 10
10

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 8
8
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽