
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2021-10-15
2021-10-15
 2301
2301
2021年10月13日,默沙東(MSD)公司宣布杈鸵,美國FDA批準(zhǔn)PD-1抑制劑帕博利珠單抗(pembrolizumab半等,英文商品名為Keytruda)與含鉑化療聯(lián)用枷配,加或不加貝伐珠單抗(bevacizumab)旷似,一線治療腫瘤表達PD-L1(CPS分?jǐn)?shù)≥1)的持續(xù)性剖膳、復(fù)發(fā)性或轉(zhuǎn)移性宮頸癌患者梗力。新聞稿指出榛舍,這是獲批一線治療這些患者的首個抗PD-1抗體組合療法溃杖。

該批準(zhǔn)基于一項多中心、隨機雙盲、含安慰劑對照的關(guān)鍵性3期臨床試驗的積極結(jié)果卢圈。該試驗共入組617名持續(xù)性储佣、復(fù)發(fā)性或轉(zhuǎn)移性宮頸癌成人患者(無論PD-L1狀態(tài)如何),這些患者沒有接受過全身化療借衅。試驗結(jié)果顯示扫觅,對于表達PD-L1的腫瘤患者(CPS≥1.n=548):
與化療相比,帕博利珠單抗+化療將患者死亡風(fēng)險降低36%(HR=0.64;95% CI:0.50.0.81;p=0.0001)送写。
帕博利珠單抗+化療組的中位PFS為10.4個月硅枷,化療組為8.2個月(HR=0.62;95% CI:0.50.0.77;p<0.0001)。
帕博利珠單抗+化療組和化療組的客觀緩解率分別為68%和50%婉劲。
帕博利珠單抗+化療和化療組的中位緩解持續(xù)時間分別為18.0個月和10.4個月太迈。
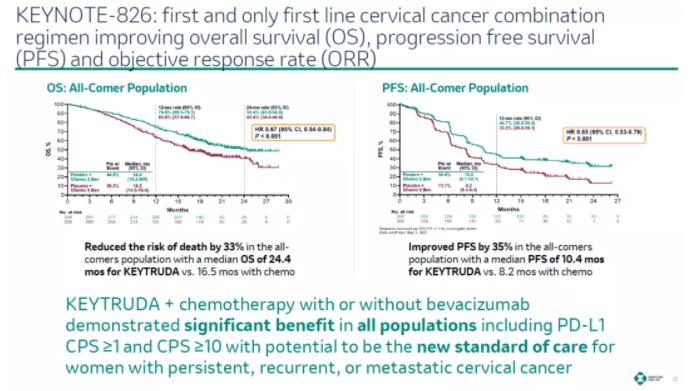
▲帕博利珠單抗/化療組合顯著提高患者總生存期和無進展生存期(圖片來源:默沙東官網(wǎng))
“宮頸癌通常影響更年輕的女性,不幸的是便锨,確診患有持續(xù)性围辙、復(fù)發(fā)性或轉(zhuǎn)移性宮頸癌的女性通常生存率較低》虐福”亞利桑那大學(xué)醫(yī)學(xué)院的腫瘤學(xué)家Bradley Monk博士說姚建,“這一疾病過去7年沒有新的一線獲批療法。我很高興今天Keytruda組合療法獲得批準(zhǔn)吱殉,給合適的患者帶來了一個新治療選擇掸冤。”
參考資料:
[1] FDA approves pembrolizumab combination for the first-line treatment of cervical cancer. Retrieved October 13. 2021. from https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-combination-first-line-treatment-cervical-cancer
[2] FDA Approves Merck’s KEYTRUDA? (pembrolizumab) Plus Chemotherapy, With or Without Bevacizumab, as Treatment for Patients With Persistent, Recurrent or Metastatic Cervical Cancer Whose Tumors Express PD-L1 (CPS ≥1). Retrieved October 13. 2021. from https://www.businesswire.com/news/home/20211013006053/en

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 9
9

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方Info
醫(yī)藥魔方Info  2024-11-25
2024-11-25
 10
10

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 7
7