
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2021-11-22
2021-11-22
 2212
2212
2021年11月17日堆缘,艾伯維(AbbVie)宣布筛武,歐盟委員會(huì)(EC)已批準(zhǔn)白細(xì)胞介素-23(IL-23)抑制劑Skyrizi(risankizumab)第二項(xiàng)適應(yīng)癥喇勋,單藥或聯(lián)合甲氨蝶呤(MTX)纵竖,用于治療對(duì)一種或多種改變疾病進(jìn)展的抗風(fēng)濕藥物(DMARDs)應(yīng)答不足或不耐受的成人活動(dòng)性銀屑病關(guān)節(jié)炎俊啼。

銀屑病關(guān)節(jié)炎是一種異質(zhì)性咒饼、全身性炎癥性疾病钢墩,在多個(gè)系統(tǒng)(包括關(guān)節(jié)和皮膚)具有標(biāo)志性表現(xiàn)顶赎。免疫系統(tǒng)產(chǎn)生的炎癥嫂焕,可導(dǎo)致關(guān)節(jié)疼痛、疲勞疯坤、僵硬报慕,并引起紅色鱗屑性皮疹。
Skyrizi通過(guò)與IL-23的p19亞基結(jié)合压怠,選擇性阻斷IL-23眠冈。IL-23是一種參與炎癥過(guò)程的細(xì)胞因子,被認(rèn)為與許多慢性免疫介導(dǎo)的疾病有關(guān)菌瘫,包括銀屑病蜗顽。Skyrizi已經(jīng)獲得美國(guó)FDA和歐盟批準(zhǔn)治療銀屑病。它還在3期臨床試驗(yàn)中用于治療克羅恩病和潰瘍性腸炎等炎癥疾病突梦。
本次批準(zhǔn)基于兩項(xiàng)隨機(jī)雙盲诫舅、多中心羽利、安慰劑對(duì)照的3期臨床試驗(yàn)獲得的積極數(shù)據(jù)。兩項(xiàng)試驗(yàn)均達(dá)到其主要終點(diǎn)刊懈,在治療第24周時(shí)这弧,接受Skyrizi治療的患者分別有57.3%和51.3%達(dá)到ACR20應(yīng)答(表示疾病嚴(yán)重程度與基線相比降低至少20%),安慰劑組為33.5%和26.5%(p<0.001)虚汛。此外匾浪,試驗(yàn)也達(dá)到序列次要終點(diǎn),患者的皮膚癥狀清除率(使用PASI 90測(cè)量)珊辛、身體功能(使用HAQ-DI指數(shù)檢測(cè))和最小疾病活動(dòng)度(MDA)均得到顯著改善,具體數(shù)據(jù)請(qǐng)見(jiàn)下圖蚜烹。
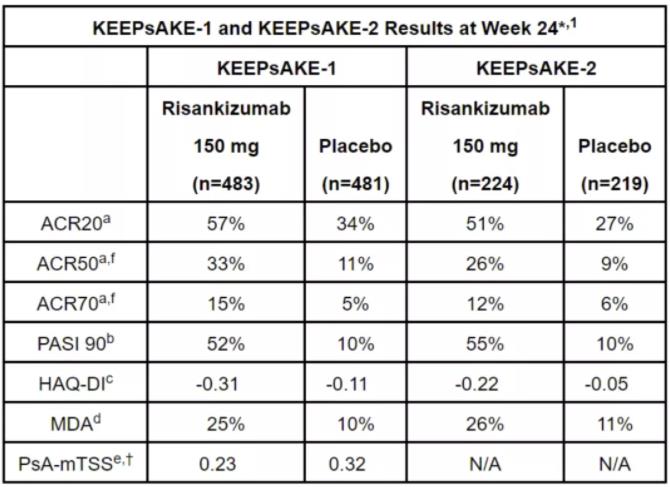
▲Skyrizi在兩項(xiàng)3期臨床試驗(yàn)中主要終點(diǎn)和次要終點(diǎn)的表現(xiàn)(圖片來(lái)源:參考資料[2])
“患有銀屑病關(guān)節(jié)炎的患者,不斷與引起腫脹和疼痛的銀屑病病變和關(guān)節(jié)炎癥艱苦斗爭(zhēng)障渡。減輕這些癥狀有望讓他們恢復(fù)日潮ò福活動(dòng),并提高生活質(zhì)量篙袄「б荆”艾伯維副主席兼總裁Michael Severino博士表示,“我們非常高興能夠?qū)⑦@種新治療選擇帶給患者接骄∑氨Γ”

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 303
303

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 278
278

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時(shí)間
醫(yī)藥時(shí)間  2024-11-18
2024-11-18
 63
63
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽