
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2022-01-10
2022-01-10
 2428
2428
2022年1月4日抑片,艾伯維(AbbVie)宣布,美國FDA已授予在研抗體偶聯(lián)藥物(ADC)telisotuzumab vedotin(Teliso-V)突破性療法認(rèn)定(BTD),用于治療在鉑類藥物治療期間或治療后發(fā)生疾病進(jìn)展更鼻、c-Met過表達(dá)的晚期/轉(zhuǎn)移性表皮生長因子受體(EGFR)野生型非鱗狀非小細(xì)胞肺癌(NSCLC)患者。

據(jù)世界衛(wèi)生組織(WHO)統(tǒng)計(jì)馒索,在2020年姻灶,肺癌是全球癌癥死亡的首因。全球新發(fā)肺癌病例超過200萬赶站,死于肺癌者約180萬幔虏。
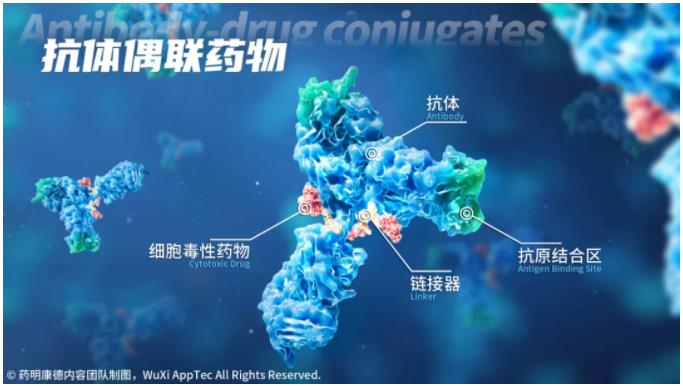
Teliso-V是艾伯維管線中研發(fā)進(jìn)展最快的ADC項(xiàng)目。該藥物靶向c-Met惕秧,以微管蛋白抑制劑MMAE作為毒性有效載荷奥徒。c-Met是一種在包括NSCLC在內(nèi)的多種腫瘤中過度表達(dá)的受體酪氨酸激酶。目前的炫,尚無獲批用于治療c-Met過表達(dá)NSCLC患者的抗癌療法吐捞。
該BTD認(rèn)定獲得了一項(xiàng)正在進(jìn)行的2期臨床試驗(yàn)的支持。該試驗(yàn)旨在確定在二線或三線治療背景中蜕裳,最適合接受Teliso-V單藥治療的c-Met過表達(dá)NSCLC人群吹蜡,然后進(jìn)一步評(píng)估在選定人群中的療效。試驗(yàn)主要終點(diǎn)是在≥12周隨訪中呈锣,患者根據(jù)中心審評(píng)的總緩解率(ORR)锤衡。
中期分析結(jié)果表明,在EGFR野生型非鱗狀NSCLC患者中秒准,c-Met高表達(dá)組的ORR為53.8%洞逼,c-Met表達(dá)水平中等組的ORR為25.0%。并且憾汛,Teliso-V聯(lián)合表皮生長因子受體(EGFR)酪氨酸激酶抑制劑(TKI)奧希替尼(osimertinib党饮,泰瑞沙),治療經(jīng)治c-Met過表達(dá)NSCLC患者的1期臨床試驗(yàn)也正在進(jìn)行中驳庭。未來刑顺,公司將在一項(xiàng)隨機(jī)化3期臨床試驗(yàn)中進(jìn)一步評(píng)估Teliso-V單藥治療,在經(jīng)治c-Met過表達(dá)NSCLC患者中的療效饲常。
“非小細(xì)胞肺癌患者有很高的未滿足需求蹲堂,Teliso-V有望為他們提供一種額外的治療選擇來管理他們的疾病。”艾伯維副總裁兼腫瘤臨床開發(fā)全球負(fù)責(zé)人Mohamed Zaki博士表示柒竞,“這一突破性療法認(rèn)定是向?yàn)槎喾N癌癥類型開發(fā)創(chuàng)新療法政供,提高癌癥患者護(hù)理標(biāo)準(zhǔn)的目標(biāo)邁出的重要一步⌒嗷”

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 300
300

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 275
275

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時(shí)間
醫(yī)藥時(shí)間  2024-11-18
2024-11-18
 62
62
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽