
 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)麥客News
醫(yī)麥客News  2022-12-19
2022-12-19
 2608
2608
2022年12月16日/醫(yī)麥客新聞 eMedClub News/--近日,藍(lán)鳥生物和諾華在2022ASH大會上公布了其用于治療鐮狀細(xì)胞貧血病基因療法的最新進(jìn)展野崇。
藍(lán)鳥生物:Lovo-cel
Lovo-cel是一款基于慢病毒的用于治療鐮狀細(xì)胞貧血不Ψ濉(SCD)的自體干細(xì)胞療法士复,通過慢病毒載體將具備功能的人βA-T87Q-珠蛋白基因拷貝至取自患者體內(nèi)的造血干細(xì)胞中衅洞,再將這些干細(xì)胞回輸?shù)交颊唧w內(nèi)赏迟,使其自主生成β-珠蛋白约素,從而消除或大幅降低繼續(xù)輸血需求。值得一提的是贝攒,2021年2月盗誊,F(xiàn)DA暫停了lovo-cel的臨床試驗,并在同年解除限制隘弊。
本次ASH年會藍(lán)鳥生物公布了正在進(jìn)行的I/II期HGB-206試驗C組的最新數(shù)據(jù)哈踱。HGB-206研究是目前業(yè)內(nèi)規(guī)模最大,隨訪時間最長梨熙,最成熟的SCD基因療法臨床試驗之一开镣。截至2022年8月,藍(lán)鳥Lovo-cel的三項臨床研究中锯忱,已有50名患者接受了治療常籍,患者隨訪時間長達(dá)7年,(中位數(shù):37.7個月)闰妓。
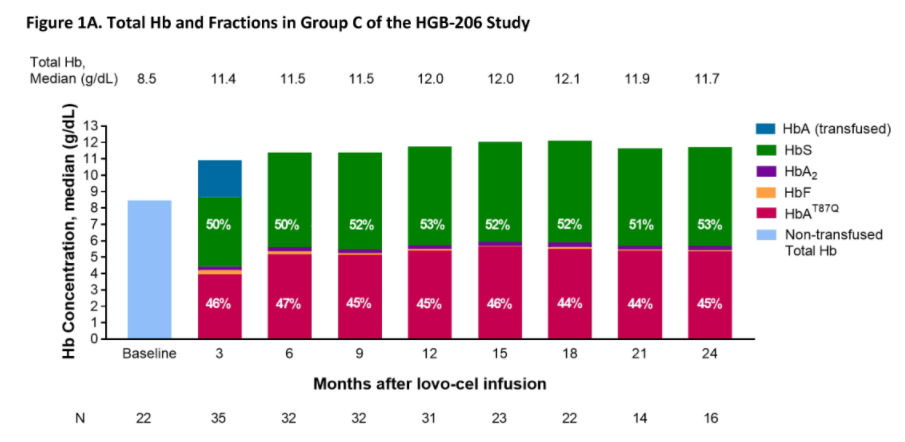
?研究結(jié)果
數(shù)據(jù)截至2021年7月锨圣,C組35例患者接受了lovo-cel輸注,中位隨訪時間為20.9個月(8.5-28.5)过腰。在29名可評估的患者中骗采,截至最后一次隨訪,在2年的母研究中橄看,28名患者在輸注lovo-cel后嚴(yán)重血管閉塞發(fā)作(VOEs)完全解決词趾,而在入組前2年,每年3.5例(1.0-13.5例);在長期隨訪研究中未見嚴(yán)重VOE的報告硅跌。關(guān)鍵溶血指標(biāo)接近正常水平审陌。
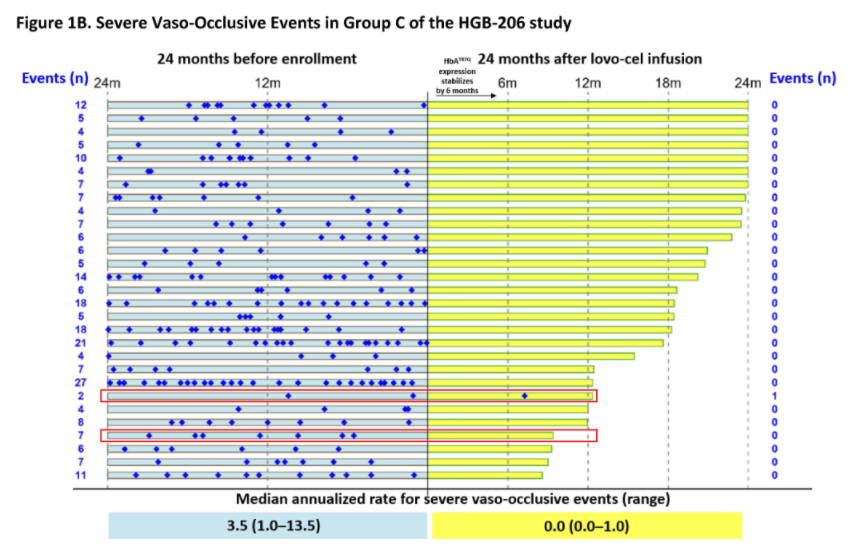
總的來看,該種治療技術(shù)可使大多數(shù)紅細(xì)胞持續(xù)產(chǎn)生β-珠蛋白闲涕,從而減少溶血疤格,并解決嚴(yán)重的血管阻塞事件。據(jù)業(yè)內(nèi)人士稱姓建,藍(lán)鳥生物仍有望在2023年第一季度提交lovo-cel 的生物制品許可申請(BLA)诞仓。
Intellia/諾華:OTQ923
OTQ923是一種基于CRISPR/Cas9基因組編輯的體外自體干細(xì)胞(HSCs)療法缤苫,用于治療鐮狀細(xì)胞病(SCD)速兔。本次ASH大會上公布的是OTQ923用于治療鐮狀細(xì)胞病(SCD)的I/II期試驗的最新數(shù)據(jù)。
截至2022年7月8日活玲,2名參與者接受了OTQ923治療涣狗,隨訪分別為9個月和3個月。
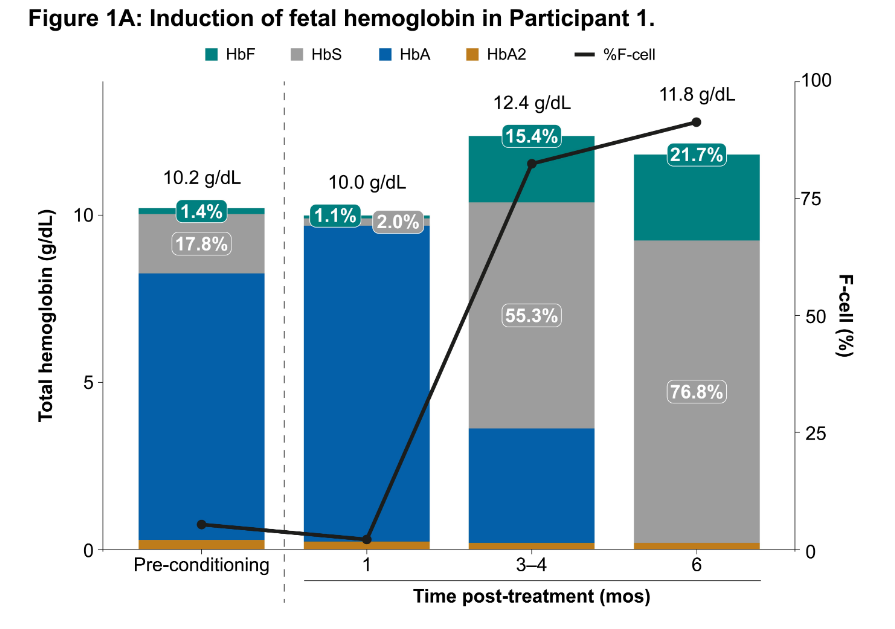
研究結(jié)果顯示舒憾,參與者1的HbF水平在輸注6個月后上升镀钓,并在數(shù)據(jù)截止時保持穩(wěn)定,即在輸注9個月時的HbF水平為22.1%。參與者2在輸注3個月后HbF水平達(dá)到了15.9%丁溅。此外唤蔗,直到輸注完成后的第6個月,受試者1的外周血中編輯等位基因的比例一直維持在60%以上窟赏。
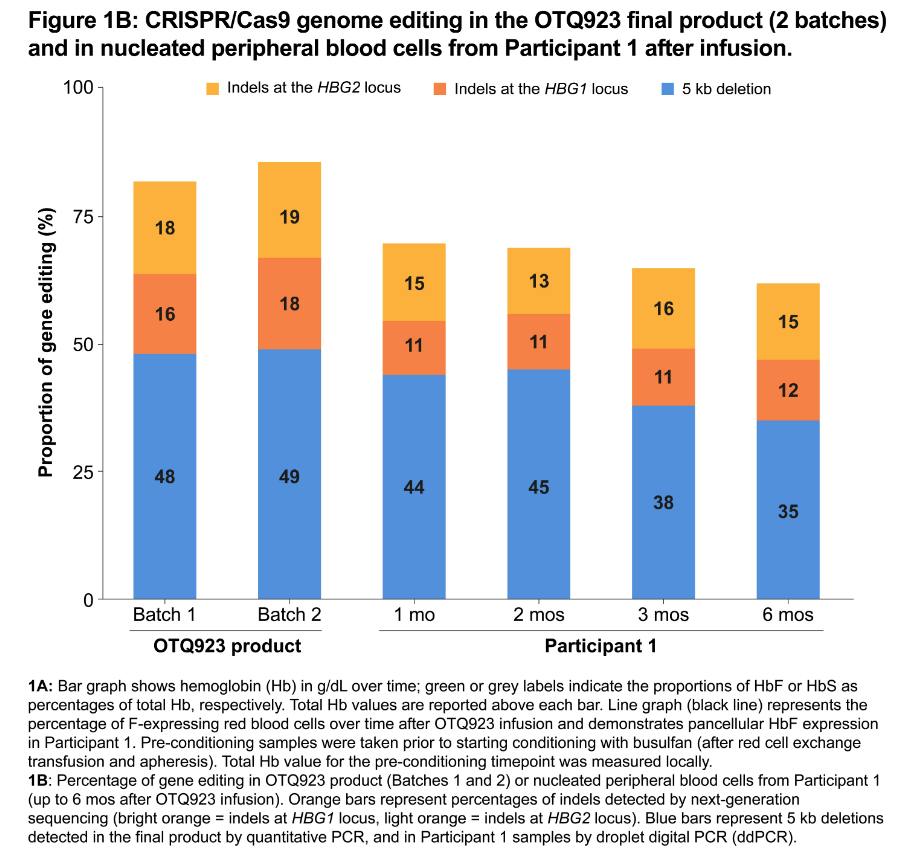
總的來說妓柜,初步數(shù)據(jù)顯示,在接受治療后棕健,兩名患者均有獲益寸纠,兩者的HbF水平均有臨床意義的增加,并且該療法安全性可控秕肚,有望成為嚴(yán)重SCD患者一種潛在的治療選擇帮课。
結(jié)語
事實上,藍(lán)鳥的基因療法研發(fā)是頗為曲折的袭吗,慢病毒技術(shù)路線也曾經(jīng)遭到過FDA和業(yè)內(nèi)專家的質(zhì)疑八泡,并且藍(lán)鳥已上市的基因療法并沒有為其創(chuàng)造太大的利潤。但是乡纸,藍(lán)鳥仍然在前進(jìn)扛聂,近期藍(lán)鳥賣掉了優(yōu)先審查券補(bǔ)貼家用。做創(chuàng)新藥本就九死一生坪秒,龍頭企業(yè)也不例外栏付,尤其是在基因治療這一新興賽道研發(fā)風(fēng)險更為放大。因此煞嫩,無論成功或失敗组弥,先行者值得敬佩,其研發(fā)經(jīng)驗?zāi)軌蚪o后來者以借鑒逗爹。此外亡嫌,藍(lán)鳥一直也在對基因療法和商業(yè)模式進(jìn)行優(yōu)化,有望讓基因療法惠及更多患者掘而。

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 269
269

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 246
246

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 58
58
 熱門資訊
熱門資訊