
 研發(fā)追蹤
研發(fā)追蹤
 凱萊英藥聞
凱萊英藥聞  2022-12-19
2022-12-19
 2811
2811
2022年12月12日,Mirati Therapeutics(以下簡稱“Mirati”)宣布FDA已加速批準(zhǔn)KRAZATI(adagrasib)雳誉,作為具有KRAS G12C突變的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)患者的靶向治療選擇呛靡。KRAZATI是全球第2款獲批的口服KRAS抑制劑幔憋。

關(guān)于KRAZATI
KRAZATI是一種高選擇性和強效的 KRAS G12C口服小分子抑制劑辐椎, 經(jīng)過優(yōu)化以維持靶點抑制肴焊;由于 KRAS G12C 蛋白每 24-48 小時再生一次其屏,這一屬性對于治療 KRAS G12C突變的癌癥十分重要唧瘾。KRAZATI將繼續(xù)作為單一療法措译,并與其他抗癌療法聯(lián)合用于晚期 KRAS G12C突變實體瘤患者,包括非小細(xì)胞肺癌禀丁、結(jié)直腸癌和胰腺癌翼辱。2021年6月乃描,再鼎醫(yī)藥預(yù)付6500萬美元、總價3.38億美元獲adagrasib (MRTX849)引入大中華區(qū)(中國大陸吴烹、香港斯凑、澳門和臺灣地區(qū))獨家權(quán)益,目前已向中國國家藥監(jiān)局藥品審評中心(CDE)提交的adagrasib(阿達格拉西)臨床試驗申請眨攀。
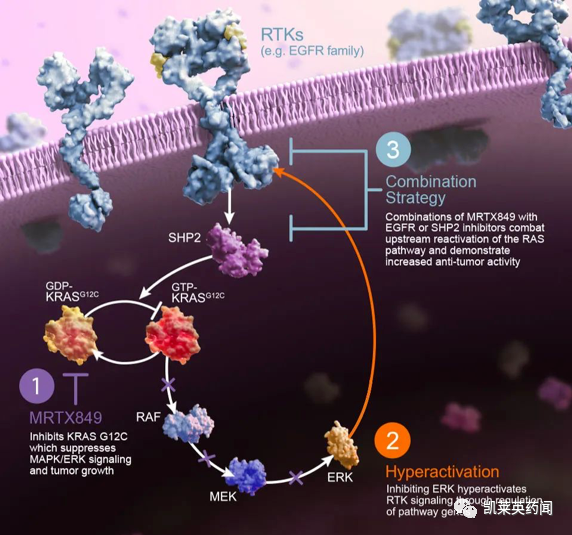
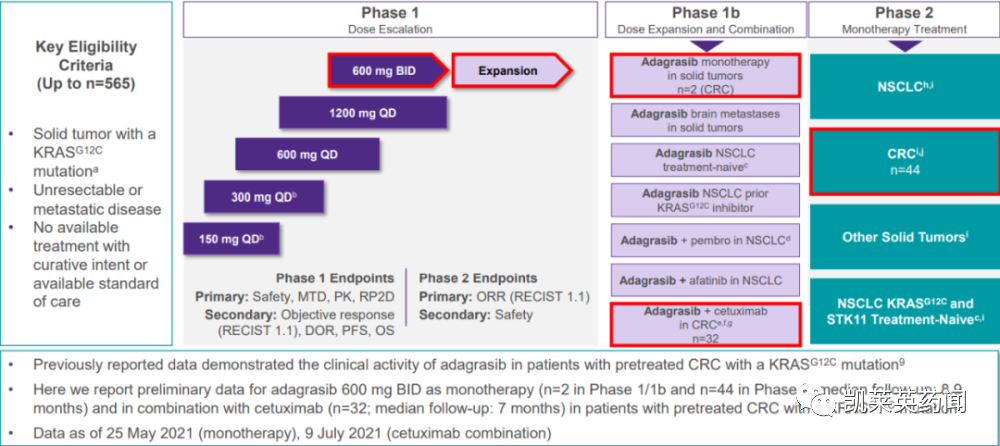
該藥物在FDA的加速獲批是基于2期KRYSTAL-1注冊研究的數(shù)據(jù)蛀颓,在116名早前接受過鉑類方案和免疫檢查點抑制劑的治療的KRASG12C突變晚期NSCLC患者中,給予600mg KRAZATI膠囊每天兩次口服扛聂,根據(jù)實體瘤反應(yīng)評估標(biāo)準(zhǔn)(RECIST v1.1)艘尊,通過盲法獨立中心評價(BICR)評估,確認(rèn)患者的客觀緩解率(ORR) 和緩解持續(xù)時間 (DOR)栏付。結(jié)果顯示:ORR 為 43% (95% CI:34-53)罚考,80% (95% CI:71-87) 的患者實現(xiàn)了疾病控制。中位DOR為8.5個月(95%CI:6.2-13.8)组弥。
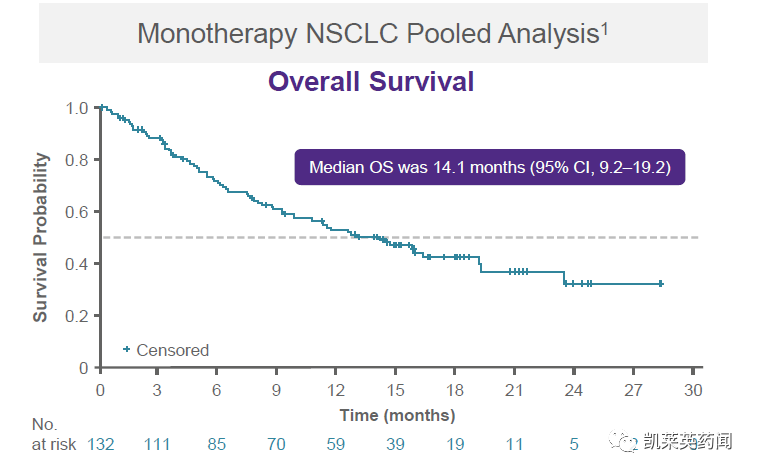
此外笼踩,在包括來自KRYSTAL-1研究的1/1b期NSCLC和注冊2期NSCLC隊列的匯總療效分析(n=132)中,評估adagrasib單藥每日口服2次治療的效果终抽,結(jié)果顯示:ORR為44%,疾病控制率為81%桶至,中位DOR為12.5個月(95%CI昼伴, 7.3-NE),中位總生存期為14.1個月(94%CI镣屹,9.2-19.2)圃郊。
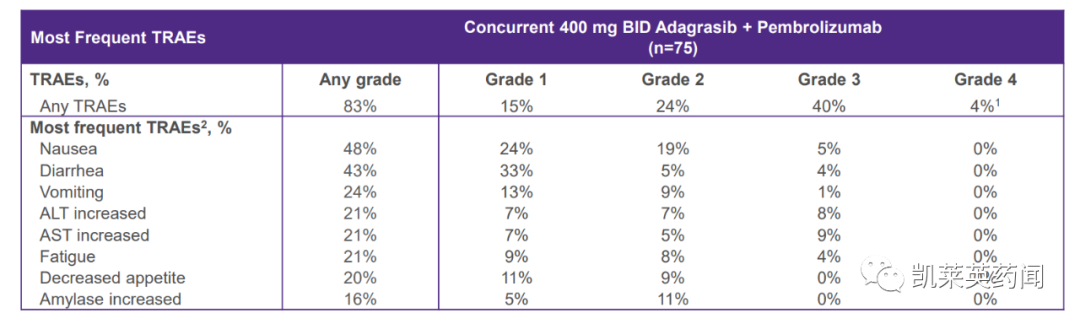
在不良反應(yīng)上,在 366 名參加 KRYSTAL-1 和 KRYSTAL-12 的患者中女蜈,最常見的(≥25%)不良反應(yīng)是惡心持舆、腹瀉、嘔吐伪窖、疲勞逸寓、肌肉骨骼疼痛、肝毒性覆山、腎功能損害竹伸、水腫、呼吸困難和食欲下降福互。由于不良反應(yīng)刹由,KRAZATI的永久性停藥發(fā)生在13%的患者中。
關(guān)于KRAS
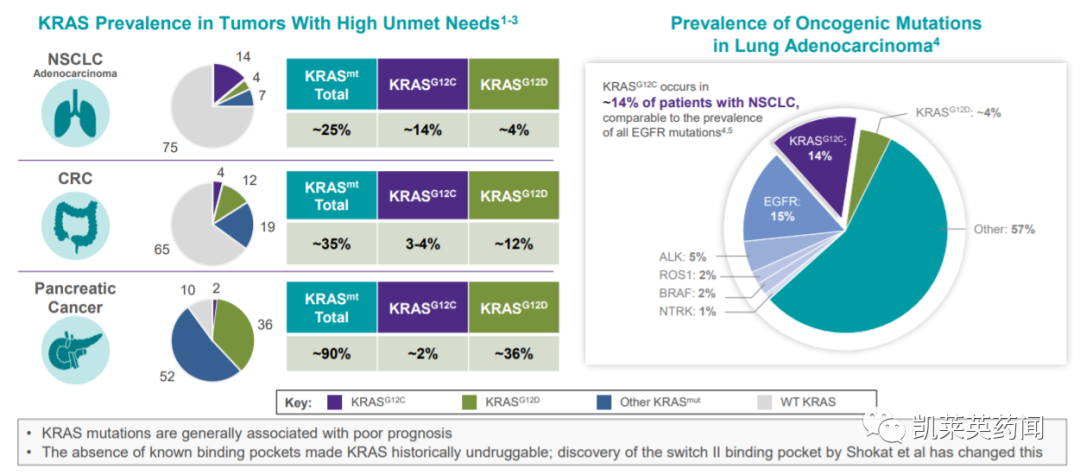
由于KRAS突變體的結(jié)構(gòu)特點鹉鉴、信號通路的復(fù)雜性以及KRAS突變型腫瘤的耐藥性妨菩,KRAS一度被稱為“不可成藥靶點”糙枚。其中,KRAS G12C作為一種特定的KRAS亞突變厚饱,是第12個密碼子的甘氨酸被半胱氨酸取代檐伞,約占所有KRAS突變的44%,其中非小細(xì)胞肺癌腺癌中最常見惊眠,占14%纳傍,其次是大腸腺癌占3-4%,胰腺癌占2%尖鲜,全球每年超過100000人確診為KRAS G12C突變拧亡。
隨著KRAS抑制劑研究不斷取得新進展,近年來越來越多的企業(yè)開始布局KRAS抑制劑領(lǐng)域宣璧,探索新的組合療法谤碳, 下表是有關(guān)KRAS近年來的交易情況:

除KRAZATI外,目前全球上市的另一款KRAS抑制劑是安進的 Lumakras(sotorasib)溢豆。根據(jù)Fierce Pharma預(yù)測蜒简, 2025年的sotorasib預(yù)測市場為13億美元,而adagrasib在2026年預(yù)測市場可達17億美元漩仙。將全球處于臨床以上階段的KRAS藥物統(tǒng)計如下:

關(guān)于Mirati
Mirati是一家處于臨床階段的生物技術(shù)公司搓茬,其使命是發(fā)現(xiàn),設(shè)計和提供突破性療法队他,以改變癌癥患者及其親人的生活卷仑。公司堅持不懈地致力于推出解決包括肺癌在內(nèi)的高度未滿足需求的領(lǐng)域的療法,并推進針對癌癥遺傳和免疫驅(qū)動因素的新型療法的管線麸折。

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 269
269

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 247
247

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 58
58