
 研發(fā)追蹤
研發(fā)追蹤
 佰傲谷BioValley
佰傲谷BioValley  2022-12-30
2022-12-30
 3208
3208
近日(2022年12月28日)焚惰,TG Therapeutics公司宣布倔晚,其CD20單抗ublituximab獲FDA批準(zhǔn)上市拔较,用于治療復(fù)發(fā)型多發(fā)性硬化癥(MS)蟋真。
此次批準(zhǔn)主要基于ULTIMATE I和ULTIMATE II的兩項(xiàng)III期臨床數(shù)據(jù)站号。兩項(xiàng)臨床試驗(yàn)均達(dá)到臨床終點(diǎn)洗出。試驗(yàn)結(jié)果結(jié)果顯示静檬,治療96周后宽档,與對照組相比尉姨,ublituximab顯著降低了RMS患者的年化復(fù)發(fā)率(ARR)。在ULTIMATE I試驗(yàn)中吗冤,ublituximab組(n=271)的ARR為0.076卓召,對照組(n=274)則為0.188。在ULTIMATE II試驗(yàn)中沐虐,ublituximab組患者(n=272)的ARR為0.091伶摄,對照組(n=272)為0.178骚目。
ublituximab為TG Therapeutics開發(fā)的一種靶向CD20shagn獨(dú)特表位的糖化工程單克隆抗體,作用機(jī)制與已獲批的抗CD20單抗相似历劣。ublituximab通過巖藻糖修飾冷沿,大幅度提高了ADCC活性,增加了ublituximab效力根丈。
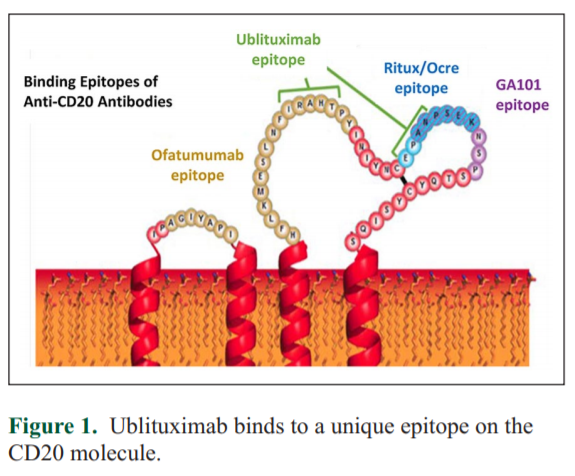
1997年第一款藥品批準(zhǔn)上市至今病唁,抗CD20單抗已經(jīng)發(fā)展到了第三代,藥物活性和免疫原性都有了很大改善使宽。第一代以人鼠嵌合單抗——利妥昔單抗為代表羞菊;第二代以人源化單抗——奧法木單抗為代表;第三代以單抗Fc段被修飾的阿妥珠單抗為代表厦嘹,隨著人源化程度的提高隐户,新一代抗CD20單抗顯示出越來越高的活性和越來越低的耐藥性及副作用;同時新的適應(yīng)癥也不斷被發(fā)掘姐赡。
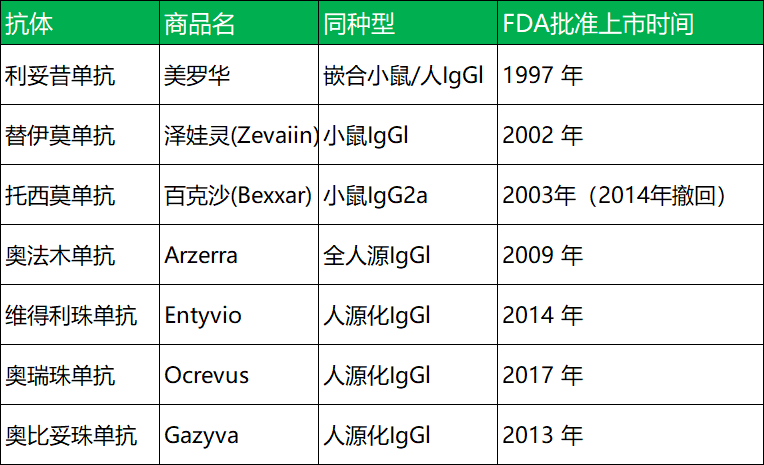
作為治療B細(xì)胞淋巴瘤的理想靶點(diǎn)莱预,除了CD20 單抗以外,越來越多的靶向療法選擇CD20项滑,包括雙抗依沮、ADC、CAR-T等等枪狂。
英文原文:https://www.tgtherapeutics.com/our-pipeline/ublituximab/

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 269
269

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 246
246

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 58
58
 熱門資訊
熱門資訊