
 研發(fā)追蹤
研發(fā)追蹤
 邁極康insight
邁極康insight  2023-01-13
2023-01-13
 2988
2988
1月9日睹簇,武田制藥和Arrowhead公司聯(lián)合公布fazirsiran (TAK-999/ARO-AAT)用于治療與α-1抗胰蛋白酶缺乏(AATD-LD)相關的肝臟疾病的2期SEQUOIA臨床試驗研究的主要結(jié)果。
fazirsiran (TAK-999/ARO-AAT)是一種潛在的“first-in-class”研究性RNA干擾(RNAi)療法,旨在減少突變α-1抗胰蛋白酶蛋白(Z-AAT)的產(chǎn)生,作為一種與AATD相關的罕見遺傳性肝病的潛在治療方法。Z-AAT積累被認為是AATD患者進行性肝病的原因牢酵。減少炎癥性Z-AAT蛋白的產(chǎn)生有望阻止肝臟疾病的進展伦窜,并有可能使肝臟再生和修復蜡瓜。farzirsiran于2021年7月被美國FDA授予突破性治療指定(BTD)脓大,并于2018年2月獲得孤兒藥指定屋骇,用于治療AATD-LD。
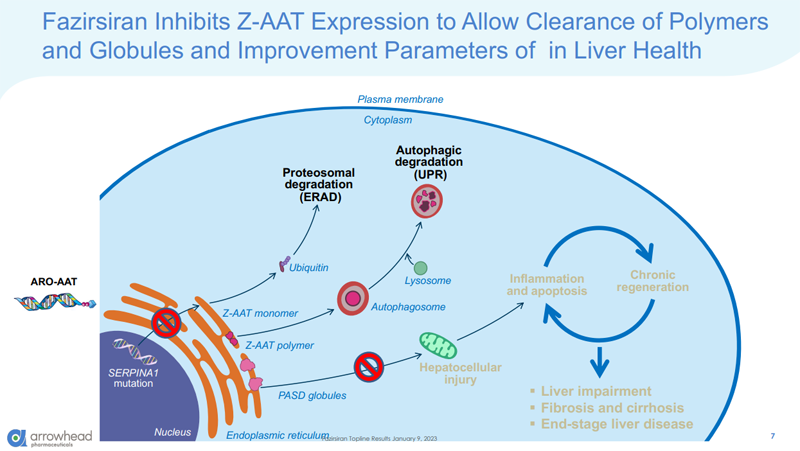
fazirsiran (TAK-999/ARO-AAT)作用機制
SEQUOIA(NCT03945292)是一項安慰劑對照过桌、多劑量殷彰、2期研究,旨在確定fazirsiran(TAK-999/ARO-AAT)在42例AATD-LD患者中的安全性诚摹、耐受性和藥效學效果哺肘。患者被納入三個隊列渗稍,分別接受25mg(n=9)佩迟、100mg(n=8)、200mg(n=9)或匹配的安慰劑(n=14)免胃。
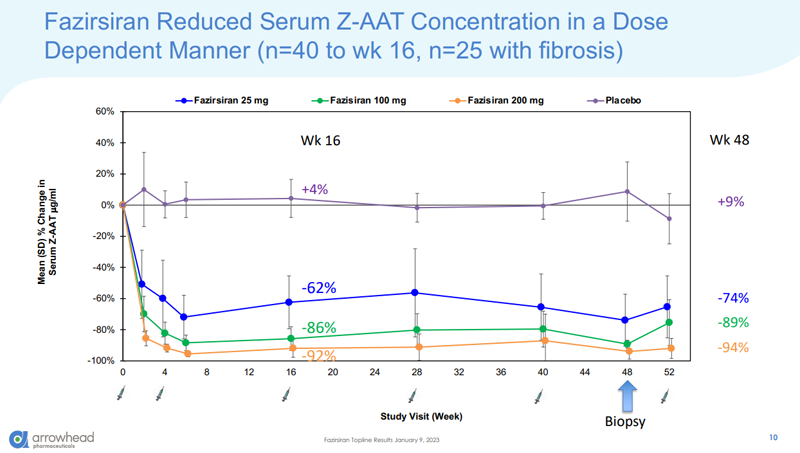
試驗研究結(jié)果表明音五,接受25 mg、100 mg或200 mg fazirsiran且有基線纖維化的患者(n=16)在第48周時羔沙,
1. 血清突變體α-1抗胰蛋白酶蛋白(Z-AAT)濃度的劑量依賴性平均降低了74%躺涝、89%和94%;
2. 所有三種劑量均顯示總肝臟Z-AAT顯著降低扼雏,基線后肝活檢就診時中位數(shù)降低94%坚嗜。此外,在基線后肝活檢時诗充,PAS-D染色從基線平均5.9降低到基線后平均2.3苍蔬;
3. 42%的患者門靜脈炎癥得到改善,只有7%的患者出現(xiàn)惡化蝴蜓;
4. 50%患者的Metavir評分(肝組織纖維化分期評分碟绑,分數(shù)越高表明肝臟纖維化程度越嚴重)下降≥1。
相比之下榛舍,到48周接受安慰劑的基線纖維化患者(n=9)血清Z-AAT與基線相比沒有顯著變化溃杖,肝臟Z-AAT增加26%,PAS-D染色無顯著變化耽慌,患者門靜脈炎癥沒有得到改善卢圈,且44%的患者發(fā)生惡化。
Fazirsiran具有良好的耐受性辅任,迄今為止報告的治療緊急不良事件在fazirsiran和安慰劑組之間總體平衡借衅。在任何研究組中均未出現(xiàn)導致停藥、劑量中斷或過早退出研究的治療緊急不良事件立漏。與安慰劑相比鹊属,在1年以上的肺功能測試中冶媚,fazirsiran未觀察到劑量依賴性或臨床意義的變化。
“目前還沒有治療α-1抗胰蛋白酶缺乏癥引起的肝病的方法婉劲。今天來自SEQUOIA研究的結(jié)果對于需要安全有效治療這種罕見遺傳疾病的醫(yī)生和患者來說是非常鼓舞人心的太迈,”佛羅里達大學胃腸病學、肝臟病學和營養(yǎng)學系醫(yī)學博士便锨、理學碩士Virginia Clark說围辙。“我們認為放案,肝臟中錯誤折疊蛋白質(zhì)的積累是肝臟疾病發(fā)展的重要一步姚建,因此阻斷蛋白質(zhì)產(chǎn)生的療法可能會讓肝臟清除有毒蛋白質(zhì),并有可能治愈吱殉〉г”
關于α-1抗胰蛋白酶缺乏相關性肝病
α-1抗胰蛋白酶缺乏癥(AATD)是一種罕見的遺傳性疾病,與兒童和成人的肝臟疾病以及成人的肺部疾病有關友雳。據(jù)估計稿湿,在美國,每3000-5000人中就有一人患AATD押赊,在歐洲饺藤,每2500人中就有一人患AATD,其中35%的人可能會患上肝臟疾病流礁。AAT蛋白主要由肝細胞合成和分泌涕俗。它的作用是抑制能分解正常結(jié)締組織的酶。最常見的疾病變異神帅,Z突變體山堵,有一個氨基酸取代,導致蛋白質(zhì)折疊不當几菲。突變蛋白不能有效分泌硅决,并積聚在肝細胞內(nèi)的小球中。這會引發(fā)持續(xù)的肝細胞損傷杉唇,導致纖維化猫乃、肝硬化,并增加肝細胞癌的風險铣才。

 研發(fā)追蹤
研發(fā)追蹤
 藥研網(wǎng)
藥研網(wǎng)  2024-11-18
2024-11-18
 266
266

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-18
2024-11-18
 244
244

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥時間
醫(yī)藥時間  2024-11-18
2024-11-18
 57
57