
 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方Pro
醫(yī)藥魔方Pro  2023-12-25
2023-12-25
 1941
1941
12月18日腾啥,華盛頓大學(xué)David Baker教授團(tuán)隊(duì)及其合作伙伴在Nature雜志發(fā)表最新論文,報(bào)道了人工智能(AI)技術(shù)能夠從頭設(shè)計(jì)高親和力的蛋白进每,這一進(jìn)步有望讓科學(xué)家們創(chuàng)造出更便宜的抗體替代品矫钓,用于疾病檢測和治療摸进。

來源:Nature
結(jié)合傳統(tǒng)和基于深度學(xué)習(xí)的分子設(shè)計(jì)方法恨递,研究人員創(chuàng)造出了與各種具有挑戰(zhàn)性的生物標(biāo)志物(包括人類激素)具有極高親和力和特異性的蛋白質(zhì)。研究人員指出栗哥,他們實(shí)現(xiàn)了計(jì)算機(jī)生成的生物分子與其靶標(biāo)之間的最高結(jié)合親和力鞍歌。
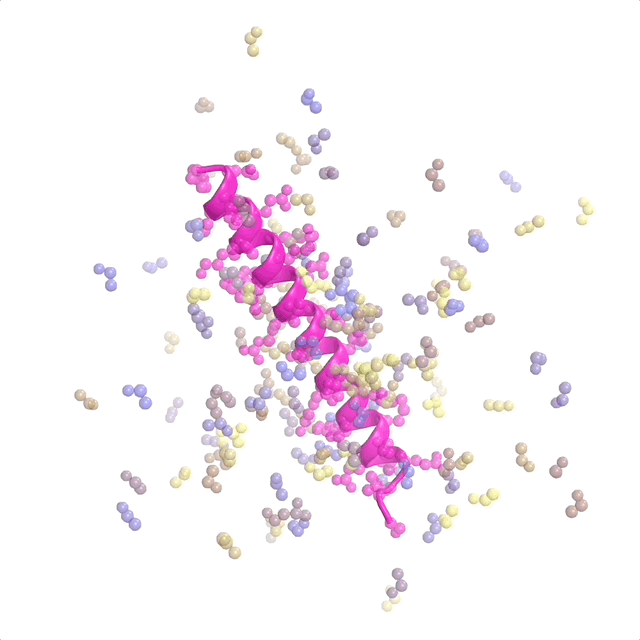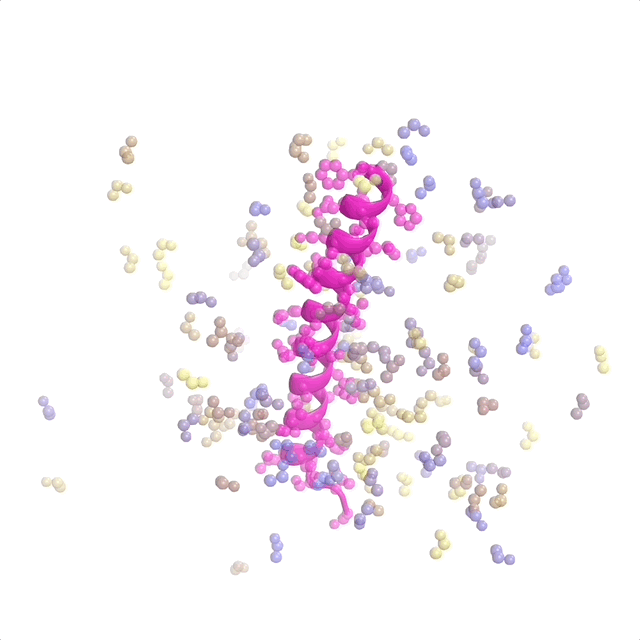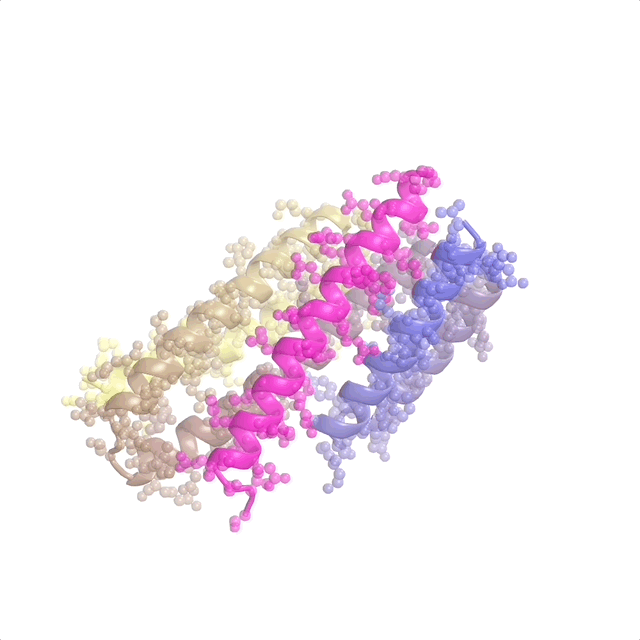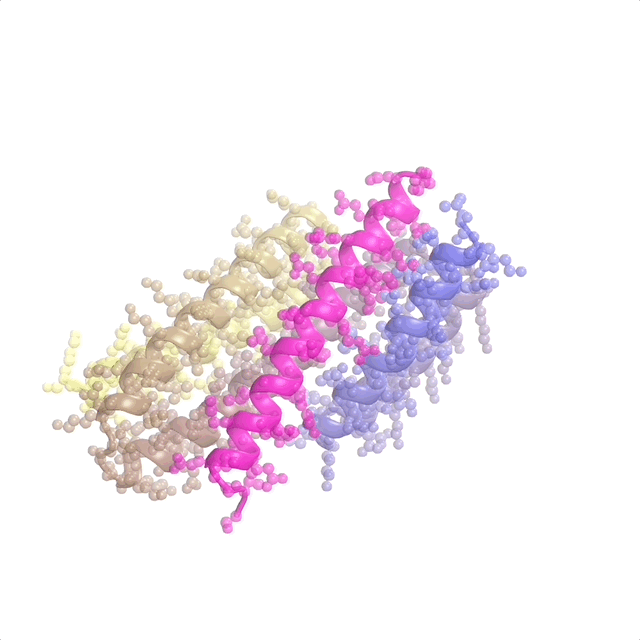
AI支持蛋白設(shè)計(jì)軟件運(yùn)行 | 從一個(gè)目標(biāo)結(jié)合靶點(diǎn)(粉色)和一團(tuán)斷開的氨基酸開始,RFdiffusion迭代地“雕刻”出一個(gè)新的蛋白質(zhì)結(jié)構(gòu)。最后褂删,ProteinMPNN將氨基酸側(cè)鏈分配給新的蛋白質(zhì)結(jié)構(gòu)飞醉,從而產(chǎn)生完整的蛋白質(zhì)分子。實(shí)驗(yàn)室測試表明屯阀,與迄今為止報(bào)道的計(jì)算機(jī)生成的蛋白(未經(jīng)任何實(shí)驗(yàn)優(yōu)化)相比缅帘,通過這種方法生成的蛋白展現(xiàn)出了最高的靶點(diǎn)結(jié)合親和力。(來源:Institute for Protein Design, University of Washington)
研究小組首先創(chuàng)造了能夠結(jié)合胰高血糖素难衰、神經(jīng)肽Y股毫、甲狀旁腺激素和其它螺旋肽類靶點(diǎn)的蛋白質(zhì)。這些靶點(diǎn)分子在生物系統(tǒng)中至關(guān)重要召衔,但藥物和診斷工具識(shí)別這些分子極具挑戰(zhàn)性,因?yàn)樗鼈兺ǔH狈Ψ€(wěn)定的分子結(jié)構(gòu)祭陷。
該研究引入了一種創(chuàng)建新蛋白形狀的生成式模型RFdiffusion(RoseTTAFold Diffusion)苍凛,并聯(lián)合了序列設(shè)計(jì)工具ProteinMPNN。這些程序均由David Baker教授實(shí)驗(yàn)室開發(fā)兵志,Rfdiffusion能生成各種功能性蛋白質(zhì)醇蝴,包括在天然蛋白質(zhì)中從未見過的拓?fù)浣Y(jié)構(gòu),相關(guān)論文于2023年7月11日發(fā)表在Nature雜志上萝轰;ProteinMPNN可以在幾秒鐘內(nèi)設(shè)計(jì)出蛋白質(zhì)推吼,相關(guān)論文于2022年9月15日發(fā)表在Science雜志上(推薦閱讀:比AlphaFold更強(qiáng)?1天2篇Science疹咕,這個(gè)團(tuán)隊(duì)的新技術(shù)幾秒鐘生成全新蛋白質(zhì))贮殊。
在最新的研究中,通過以新的方式結(jié)合這些工具铲恃,科學(xué)家們利用有限的靶點(diǎn)信息(如一個(gè)肽的氨基酸序列)就能夠生成結(jié)合蛋白(binding proteins)夫咏。
通過與哥本哈根大學(xué)和華盛頓大學(xué)醫(yī)學(xué)院的研究者合作,Baker教授團(tuán)隊(duì)進(jìn)行了實(shí)驗(yàn)室測試四雏,以驗(yàn)證這種新的蛋白質(zhì)設(shè)計(jì)方法勿见。質(zhì)譜法被用于檢測與人類血清中低濃度肽結(jié)合的設(shè)計(jì)蛋白,結(jié)果顯示AI生成蛋白具有用于疾病診斷的潛力百擒。此外资村,研究發(fā)現(xiàn),這些蛋白即使在高溫等惡劣條件下仍桌,也能保持其與靶點(diǎn)的結(jié)合能力为猩。
隨著設(shè)計(jì)結(jié)合蛋白(binding proteins)的方法得到改進(jìn),研究小組向設(shè)計(jì)新的生物傳感器(biosensors)發(fā)起挑戰(zhàn)忱叭。為了生成能夠檢測甲狀旁腺激素(PTH)的傳感器膝舅,科學(xué)家們將高親和力的PTH結(jié)合劑引入到之前報(bào)道的lucCage生物傳感器系統(tǒng)中。當(dāng)與甲狀旁腺激素混合時(shí)窑多,生物發(fā)光增加了21倍仍稀。
研究者們認(rèn)為洼滚,針對構(gòu)象變化的靶點(diǎn)設(shè)計(jì)結(jié)合劑(binder)的能力具有廣泛的用途。
“我們正在見證一個(gè)令人興奮的蛋白質(zhì)設(shè)計(jì)時(shí)代技潘。先進(jìn)的人工智能工具正在加速蛋白質(zhì)活性的提高遥巴。這一突破將重新定義生物技術(shù)的前景∠碛模” 共同領(lǐng)導(dǎo)這項(xiàng)研究的Susana Vazquez-Torres說道铲掐。
“設(shè)計(jì)具有如此高親和力和特異性的蛋白質(zhì)的能力為疾病的治療和診斷開辟了新的可能性≈底”David Baker教授總結(jié)道摆霉。

 研發(fā)追蹤
研發(fā)追蹤
 藥時(shí)代
藥時(shí)代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125
 熱門資訊
熱門資訊