
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-03-11
2024-03-11
 1348
1348
諾和諾德(Novo Nordisk)今天公布了司美格魯肽(semaglutide)于FLOW臨床3期試驗的主要結(jié)果方椎。分析顯示了袁,1.0 mg司美格魯肽可使2型糖尿病和慢性腎步(CKD)患者發(fā)生腎病相關(guān)事件風(fēng)險降低24%付魔。根據(jù)新聞稿楚瘾,大約有40%的2型糖尿病患者帶有CKD聪戳,而司美格魯肽具潛力成為這類患者的首款胰高血糖素樣肽-1(GLP-1)類療法押赋。諾和諾德計劃于2024年向美國和歐盟遞交Ozempic標(biāo)簽擴(kuò)展的監(jiān)管審批申請牙娇。FLOW研究的詳細(xì)結(jié)果也預(yù)計將在2024年的科學(xué)會議上發(fā)布。
FLOW臨床試驗是一項隨機雙盲仙冕、安慰劑對照的臨床試驗粱快,旨在檢視劑量為1.0 mg的注射型司美格魯肽與安慰劑相比,作為標(biāo)準(zhǔn)治療的輔助療法叔扼,在2型糖尿病和CKD患者中預(yù)防腎損傷的進(jìn)展事哭,以及腎和心血管死亡風(fēng)險的效果。該試驗招募了3533名患有2型糖尿病和CKD的患者瓜富。試驗主要終點為由多個部分組成的復(fù)合終點鳍咱,包括:與基線相比,估計腎小球濾過率(eGFR)持續(xù)下降≥50%的出現(xiàn)時間与柑;eGFR下降至<15 mL/min/1.73 m2的時間谤辜;開始慢性腎臟替代治療(透析或腎移植);2型糖尿病和慢性腎病患者死于腎病或死于心血管疾病价捧。關(guān)鍵次要終點包括eGFR的年變化率丑念、主要不良心血管事件(非致死性心肌梗死涡戳、非致死性卒中、心血管死亡)和全因死亡渠欺。
2023年10月妹蔽,由于司美格魯肽的效果達(dá)到預(yù)先設(shè)定提前終止試驗的療效標(biāo)準(zhǔn),諾和諾德基于獨立數(shù)據(jù)監(jiān)查委員會(DMC)的建議提前終止FLOW試驗酥丛。
這次公布的試驗結(jié)果顯示绎疟,與安慰劑相比,接受1.0 mg司美格魯肽治療的患者的腎臟疾病進(jìn)展以及心血管和腎臟死亡風(fēng)險顯著降低了24%蘸暮,達(dá)成試驗主要終點曼砾。分析顯示,復(fù)合主要終點的CKD和心血管部分均對風(fēng)險降低有所貢獻(xiàn)懊据。此外跑著,在驗證性次要終點方面,1.0 mg司美格魯肽相對于安慰劑的優(yōu)效性亦得到證實接纽。
安全性方面门幌,1.0 mg司美格魯肽顯示具有良好的安全性與耐受性,與之前的試驗結(jié)果一致阶铝。
司美格魯肽是一種GLP-1受體激動劑熏盲,它能夠刺激胰島素的生成,并抑制胰高血糖素分泌惊也,降低食欲和食物攝入量券雕。司美格魯肽最初作為2型糖尿病的治療藥物獲批上市(商品名:Ozempic),鑒于其在減重方面的顯著效果统台,2021年6月FDA批準(zhǔn)其用于治療普通肥胖患者(商品名:Wegovy)雕擂,它是自2014年以來美國FDA批準(zhǔn)的首款用于控制普通肥胖癥或超重的新藥。該藥物并在同年晚些時候再獲歐盟批準(zhǔn)治療肥胖適應(yīng)癥贱勃。
參考閱讀:潛在5款重磅下一代GLP-1療法
除了延緩腎損傷井赌,近期所公布的臨床試驗結(jié)果也顯示司美格魯肽具有心血管保護(hù)的潛在益處。去年8月募寨,司美格魯肽達(dá)成SELECT臨床3期試驗的主要終點族展,每周一次皮下注射2.4 mg司美格魯肽可使超重或肥胖成人發(fā)生重大不良心血管事件的風(fēng)險降低20%(患者無糖尿病史)。在同月公布的STEP HFpEF臨床3期試驗結(jié)果也顯示拔鹰,每周一次2.4 mg司美格魯肽可使患有射血分?jǐn)?shù)保留型心力衰竭(HFpEF)肥胖成人患者的心力衰竭相關(guān)癥狀與身體限制大幅減少仪缸、改善運動功能,并導(dǎo)致更大幅度的體重下降列肢。
近年來諾和諾德積極地探索司美格魯肽在不同劑量恰画、不同用藥方式、不同領(lǐng)域應(yīng)用的潛力瓷马。例如拴还,CagriSema為司美格魯肽與長效胰淀素類似物cagrilintide的固定劑量組合跨晴。去年8月公布的2期臨床試驗結(jié)果顯示,CagriSema與司美格魯肽或cagrilintide單藥治療相比症影,在體重超重的2型糖尿病患者中曹是,導(dǎo)致糖化血紅蛋白水平(HbA1c)和體重更大幅度的下降。經(jīng)過32周的治療后垦亲,CagriSema房睁、司美格魯肽與cagrilintide組病患的HbA1c分別下降2.18、1.79與0.93個百分點常迹。此外侈吨,CagriSema、司美格魯肽與cagrilintide組病患的體重分別下降了15.6%奖卒、5.1%與8.1%均膛。目前CagriSema治療超重或肥胖患者的3期臨床試驗已于2022年展開,預(yù)計在2025年獲得結(jié)果淘巩。而CagriSema用于治療2型糖尿病服英、心血管疾病患者的3期試驗,也分別在去年啟動遇穷。這款療法被行業(yè)媒體Evaluate Pharma評為2024年潛在重磅的10項研發(fā)管線之一陈莽。
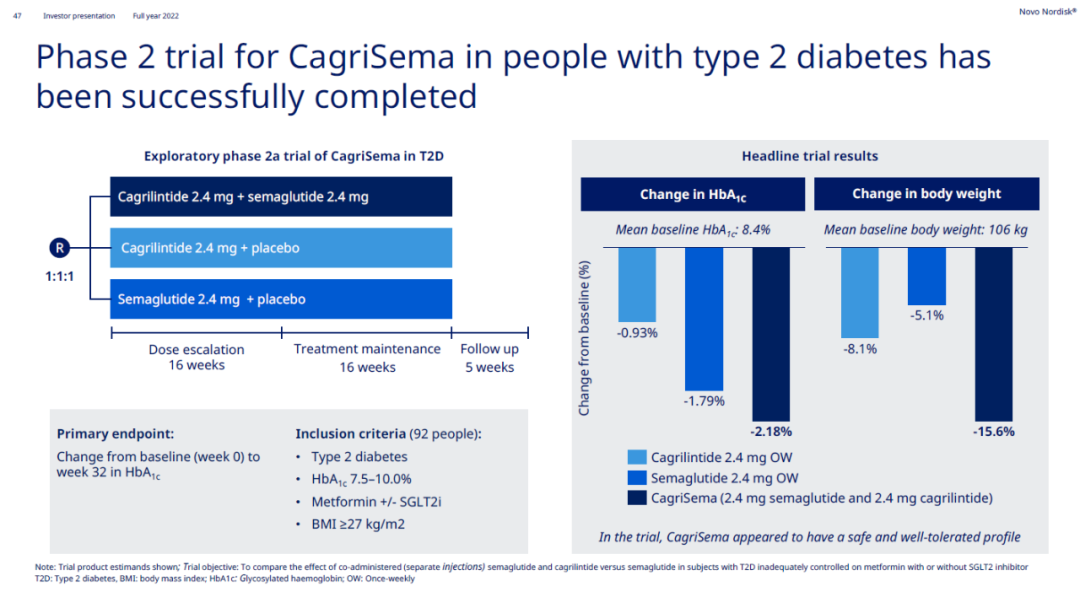
▲CagriSema在2期臨床試驗中的療效結(jié)果(圖片來源:諾和諾德官網(wǎng))
此外,目前有兩項隨機3期試驗EVOKE與EVOKE Plus的病患招募正在進(jìn)行中虽抄,旨在檢視口服司美格魯肽用于治療早期阿爾茨海默病患者的療效與安全性,每項試驗預(yù)計招募1840位患者独柑,試驗結(jié)果預(yù)計在2025年時會公布迈窟。而在一項包含320名非酒精性脂肪性肝炎(NASH)患者的2期臨床試驗中,司美格魯肽可劑量依賴性改善患者NASH癥狀的消除忌栅。在治療72周后车酣,與安慰劑相比,顯著改善NASH癥狀清除的同時索绪,未導(dǎo)致肝纖維化的惡化湖员。相關(guān)3期試驗ESSENCE也已經(jīng)啟動,預(yù)計招募1200位患者瑞驱,試驗預(yù)計于2029年完成娘摔。
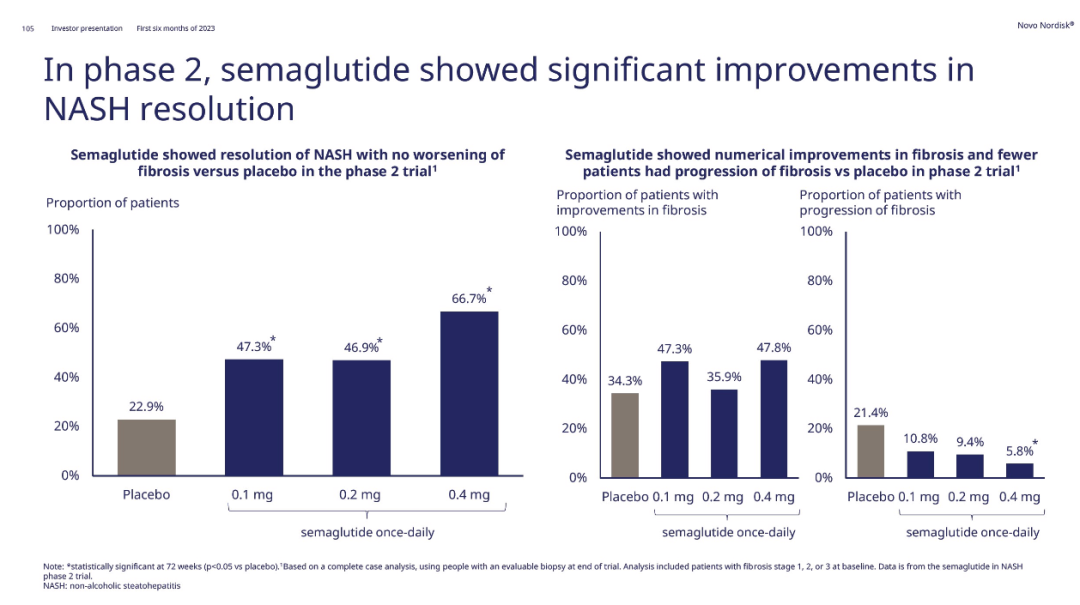
▲司美格魯肽治療NASH患者的2期臨床結(jié)果(圖片來源:諾和諾德官網(wǎng))
原文鏈接:https://www.novonordisk.com/news-and-media/news-and-ir-materials/news-details.html?id=167028

 研發(fā)追蹤
研發(fā)追蹤
 藥時代
藥時代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125
 熱門資訊
熱門資訊