
 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-03-25
2024-03-25
 1289
1289
3月21日洋满,諾和諾德宣布歐洲藥品管理局人用醫(yī)藥產(chǎn)品委員會(CHMP)通過了一項積極的意見,建議批準(zhǔn)Awiqli(每周一次基礎(chǔ)胰島素icodec)用于治療成人糖尿病。

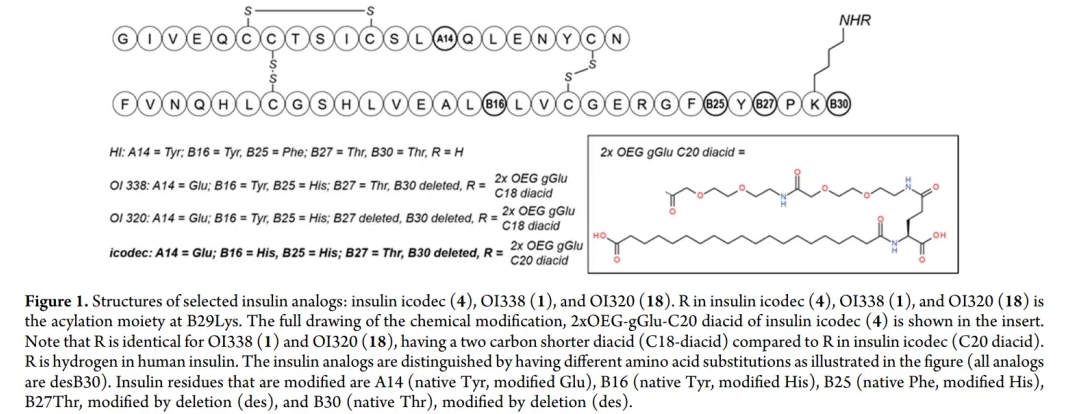
icodec是諾和諾德在口服胰島素OI338的基礎(chǔ)上設(shè)計的一款超長效胰島素制劑,人體內(nèi)半衰期長達196h。其核心設(shè)計在于:①將18C長鏈脂肪酸替換為20C長鏈脂肪酸熄浓,提高分子與人血清白蛋白的結(jié)合親和力;②將B鏈16位Tyr(酪氨酸)替換為His(組氨酸),降低分子對人胰島素受體的親和力紧碴。該產(chǎn)品也已在美國和中國遞交上市申請(見:每周1次!諾和諾德超長效胰島素icodec申報上市)甩卷。
CHMP的積極意見是基于ONWARDS臨床試驗項目的結(jié)果拔较。該項目包括6項IIIa期全球臨床試驗,研究了每周一次的基礎(chǔ)胰島素icodec的有效性和安全性,涉及4000多名1型或2型糖尿病患者槽畔,其中包括一項真實世界研究栈妆。
與接受每日基礎(chǔ)胰島素治療相比,每周一次的基礎(chǔ)胰島素治療可使2型糖尿病患者取得更好的降糖效果(通過HbA1c的變化來測量)和血糖水平維持在推薦范圍內(nèi)的時間厢钧。在之前未接受過胰島素治療的2型糖尿病患者中鳞尔,每周1次基礎(chǔ)胰島素治療組和對照組的臨床顯著性或嚴(yán)重低血糖的總體觀察率低于1例/患者年。
在1型糖尿病患者中早直,每周一次的基礎(chǔ)胰島素icodec在降低HbA1c方面顯示出非劣效性寥假,嚴(yán)重或臨床顯著低血糖的估計率有統(tǒng)計學(xué)顯著性增高。在整個項目中霞扬,每周一次的基礎(chǔ)胰島素icodec具有良好的安全性和耐受性糕韧。
除了單藥icodec和icodec+胰島素以外,諾和諾德也開發(fā)了icodec+司美格魯肽組合療法(見:每周1次胰島素+司美格魯肽喻圃!諾和諾德啟動新降糖組合療法首個III期研究)萤彩。

 研發(fā)追蹤
研發(fā)追蹤
 藥時代
藥時代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125