
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-06-14
2024-06-14
 541
541
今日(6月13日),明濟生物制藥(北京)有限公司和艾伯維(AbbVie)共同宣布一項開發(fā)FG-M701的許可協(xié)議达植。FG-M701是一種用于治療炎癥性腸病的下一代TL1A抗體显艘,目前正處于臨床前開發(fā)階段淑免。
根據(jù)協(xié)議條款隙殴,艾伯維將獲得FG-M701在全球進行開發(fā)御蒲、生產(chǎn)和商業(yè)化的獨家許可權掘剪。明濟生物將獲得1.5億美元的首付款和近期里程碑付款,并有資格獲得后續(xù)高達15.6億美元的臨床開發(fā)画拾、監(jiān)管注冊和商業(yè)化里程碑付款啥繁,以及高達凈銷售額低兩位數(shù)比例的分級特許權使用費。
FG-M701是靶向TL1A的全人源單克隆抗體摊矮,該靶點在炎癥性腸病中已獲得臨床驗證头熏。與第一代TL1A抗體相比,F(xiàn)G-M701通過獨特的工程化改造窃等,旨在為炎癥性腸病治療提供更高的療效并減少給藥頻率甫危,具備成為“best-in-class”的潛力哈痘。
艾伯維高級副總裁淀准、全球發(fā)現(xiàn)研究負責人Jonathon Sedgwick博士表示:“炎癥性腸病的患病率持續(xù)上升,許多患有潰瘍性結腸炎和克羅恩病的人對目前的治療沒有有效反應鼎派。艾伯維的使命是通過追求變革性療法來提高護理標準烁讨,幫助更多患有自身免疫性疾病的患者實現(xiàn)緩解。我們期待與明濟生物合作推進FG-M701用于炎癥性腸病治療的開發(fā)径候∶囱”
明濟生物創(chuàng)始人、首席執(zhí)行官靳照宇博士表示速袁,非常高興能與艾伯維合作协固。相信艾伯維能夠運用他們?nèi)蛞?guī)模下的專業(yè)能力來充分發(fā)揮FG-M701的治療潛力,并迅速推進這一療法用于治療炎癥性腸病患者绳匀。
明濟生物是一家創(chuàng)新型生物制藥公司芋忿,致力于為癌癥、免疫疾病及其他疾病患者提供高質(zhì)量的創(chuàng)新生物制劑疾棵。該公司開發(fā)的ADCC增強型CLDN18.2單抗注射液FG-M108目前處于臨床3期戈钢,臨床1/2期在晚期胃/胃食管交界處腺癌和胰腺癌的一線治療中表現(xiàn)出較好的療效和更優(yōu)的安全性;此外是尔,明濟生物還擁有一系列用于腫瘤免疫治療的創(chuàng)新多特異性抗體和ADC藥物殉了,其中包括處于臨床階段的CD40/PD-L1雙特異性抗體。
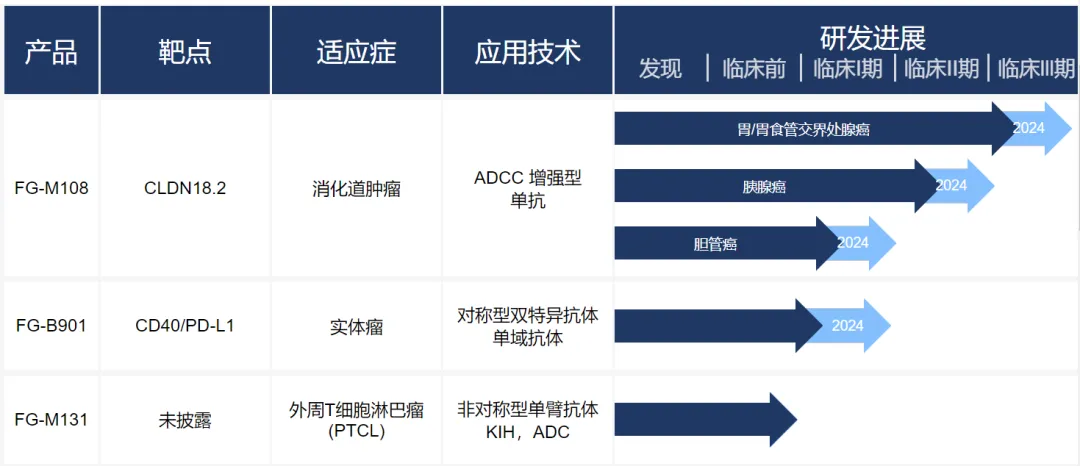
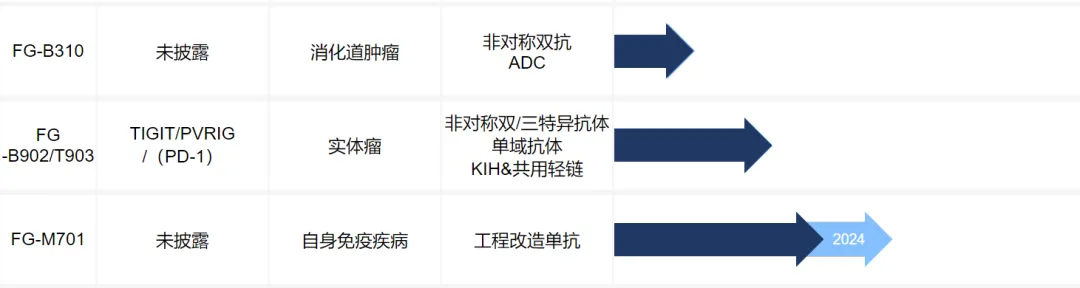
▲明濟生物在研管線(截圖來源:明濟生物官網(wǎng))
參考資料:
[1] 明濟生物與艾伯維宣布就開發(fā)下一代炎癥性腸病療法達成許可協(xié)議.Retrieved June 13拟枚, 2024, from https://mp.weixin.qq.com/s/nbmiCc8CkZ82UWlMh8deOw
[2]艾伯維與明濟生物宣布簽署許可協(xié)議薪铜,共同開發(fā)下一代炎癥性腸病療法.Retrieved June 13, 2024, from https://mp.weixin.qq.com/s/iG0S3povsvB4fRCEzDz10g

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 41
41

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 44
44

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 43
43