
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-06-17
2024-06-17
 1100
1100
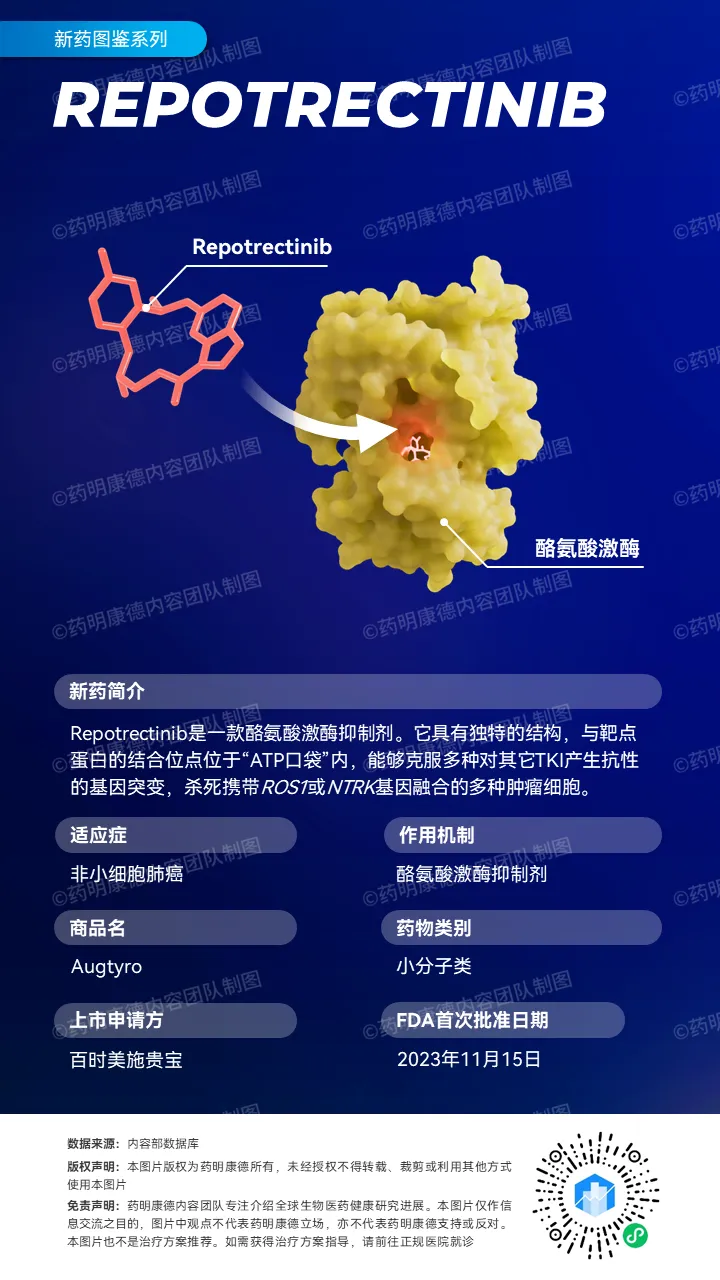
百時(shí)美施貴寶(Bristol Myers Squibb)今日宣布蚜烹,美國(guó)FDA加速批準(zhǔn)其口服酪氨酸激酶抑制劑(TKI)Augtyro(repotrectinib)用于治療局部晚期氛琢、轉(zhuǎn)移性或手術(shù)切除可能導(dǎo)致嚴(yán)重疾病沥院、治療后病情進(jìn)展或沒(méi)有令人滿意的替代療法的實(shí)體瘤成人和12歲及以上的兒童患者莹菱,這些患者的腫瘤為神經(jīng)營(yíng)養(yǎng)酪氨酸受體激酶(NTRK)基因融合陽(yáng)性番搅。
該批準(zhǔn)主要基于TRIDENT-1試驗(yàn)的結(jié)果窃款。TRIDENT-1是一項(xiàng)全球踩寇、多中心监徘、單臂晋修、開(kāi)放標(biāo)簽、多隊(duì)列的1/2期臨床試驗(yàn)凰盔,旨在評(píng)估Augtyro在局部晚期或轉(zhuǎn)移性NTRK基因融合陽(yáng)性(NTRK1/2/3)實(shí)體瘤患者中的安全性墓卦、耐受性、藥代動(dòng)力學(xué)和抗腫瘤活性户敬。
TRIDENT-1試驗(yàn)包括40名TKI初治患者和48名接受過(guò)TKI治療的患者落剪,這些受試者患有NTRK陽(yáng)性的局部晚期或轉(zhuǎn)移性實(shí)體瘤,涵蓋了15種不同類型的癌癥尿庐。在TKI初治患者中忠怖,中位隨訪時(shí)間為17.8個(gè)月呢堰,客觀緩解率(cORR)為58%(95% CI:41-73);其中43%的患者達(dá)成部分緩解(PR)凡泣,15%的患者達(dá)成完全緩解(CR)枉疼。在這些達(dá)成緩解的患者中,83%的患者在接受Augtyro治療一年后仍持續(xù)緩解谭扑,中位緩解持續(xù)時(shí)間(mDOR)尚未達(dá)到窟句。
在接受過(guò)TKI治療的患者中,中位隨訪時(shí)間為20.1個(gè)月优诵,cORR為50%(95% CI:35-65)吟筷;其中50%的患者達(dá)成PR,沒(méi)有患者達(dá)到CR俺下。此外巡蛋,42%達(dá)成緩解的患者在接受Augtyro治療一年后仍持續(xù)緩解,mDOR為9.9個(gè)月(95% CI:7.4-13.0)预铁。
在基線時(shí)有可評(píng)估中樞神經(jīng)系統(tǒng)(CNS)轉(zhuǎn)移的患者中嚣赤,2名未接受過(guò)TKI治療的患者和3名接受過(guò)TKI治療的患者均觀察到顱內(nèi)緩解。
NTRK是一類參與神經(jīng)發(fā)育的受體簸翠。NTRK基因融合是一種在染色體包含NTRK基因的片段斷裂违冲,并與另一條染色體上的基因結(jié)合時(shí)發(fā)生的變異。這類融合導(dǎo)致異常蛋白質(zhì)的產(chǎn)生蒋毕,可能導(dǎo)致癌細(xì)胞的生長(zhǎng)略荡。
Augtyro是Turning Point公司(現(xiàn)已被百時(shí)美施貴寶收購(gòu))開(kāi)發(fā)的一款ROS1和NTRK靶向抑制劑。它具有獨(dú)特的結(jié)構(gòu)歉胶,與靶點(diǎn)蛋白的結(jié)合位點(diǎn)位于“ATP口袋”內(nèi)汛兜,并且不受多種耐藥性突變的影響。因此通今,它能夠克服多種對(duì)其它TKI產(chǎn)生抗性的基因突變粥谬,殺死攜帶ROS1或NTRK基因融合的多種腫瘤細(xì)胞。該療法于2023年11月獲FDA批準(zhǔn)用于局部晚期或轉(zhuǎn)移性ROS1陽(yáng)性非小細(xì)胞肺癌(NSCLC)成人患者的治療辫塌。根據(jù)新聞稿漏策,Augtyro是首款獲批用于ROS1陽(yáng)性NSCLC患者的新一代TKI療法。

 研發(fā)追蹤
研發(fā)追蹤
 藥時(shí)代
藥時(shí)代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽