
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-06-19
2024-06-19
 317
317
上周宴凉,NMPA針對(duì)血液制品行業(yè)發(fā)出了三份有較大影響的文件:《藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)血液制品附錄修訂稿》普舆、《血液制品生產(chǎn)智慧監(jiān)管三年行動(dòng)計(jì)劃(2024—2026年)》恬口、《血液制品生產(chǎn)檢驗(yàn)電子化記錄技術(shù)指南(試行)》。三份文件剛好形成了一個(gè)規(guī)劃-規(guī)章-技術(shù)指導(dǎo)的層次速痹,指向的都是同一件事 — 血液制品生產(chǎn)企業(yè)信息化裂蝉。而其中《血液制品生產(chǎn)檢驗(yàn)電子化記錄技術(shù)指南(試行)》是本次信息化的具體要求的體現(xiàn)。值得注意的是锦镶,疫苗行業(yè)在2022年就開(kāi)始符合定稿的《疫苗生產(chǎn)檢驗(yàn)電子化記錄技術(shù)指南》的信息化要求虑庇。本次的血液制品信息化也是必然走向。
為什么是血液制品
血液制品偶屯,特指人血漿蛋白類制品光丢,是從人血漿中分離出各類蛋白制成的無(wú)菌制劑。在具有無(wú)菌制劑的固有風(fēng)險(xiǎn)之外冶习,還因原材料是人源的血漿而增加了會(huì)被病毒污染的風(fēng)險(xiǎn)镰掐。因此血液制品也都和疫苗產(chǎn)品一樣需要經(jīng)過(guò)批簽發(fā)程序才能出廠銷售。
血液制品的生產(chǎn)鏈條包括了兩個(gè)環(huán)節(jié):?jiǎn)尾裳獫{站和血液制品生產(chǎn)企業(yè)琐幔。單采血漿站是進(jìn)行血漿采集(即原材料獲日ǔ稀)的場(chǎng)所,因此血液制品生產(chǎn)過(guò)程的追溯要從單采血漿站這一不屬于生產(chǎn)企業(yè)內(nèi)的場(chǎng)所開(kāi)始齐秕,增加了追溯過(guò)程的風(fēng)險(xiǎn)程度沈机。
信息化的范圍
藥品的生產(chǎn)企業(yè)一般都會(huì)進(jìn)行一定程度的信息化建設(shè)仙蛉,但是對(duì)于信息化建設(shè)究竟要做哪些方面、做到何種程度還不甚明朗碱蒙。從這份指南中引用的文件(未全部列出)可以窺見(jiàn)信息化要求的范圍:

可以看出荠瘪,信息化要求是要結(jié)合藥事管理、質(zhì)量管理赛惩、數(shù)據(jù)安全哀墓、信息追溯等多個(gè)領(lǐng)域。
涵蓋生產(chǎn)檢驗(yàn)全過(guò)程
指南中對(duì)血液制品的生產(chǎn)檢驗(yàn)的信息化要求覆蓋很廣喷兼。從時(shí)間上涵蓋了從起始的單采血漿采集到最終的制劑放行的各環(huán)節(jié)篮绰;從空間上涵蓋了車(chē)間、實(shí)驗(yàn)室季惯、庫(kù)房等不同場(chǎng)地吠各。而且雖然指南的題目是生產(chǎn)檢驗(yàn),但其中的內(nèi)容也包括了質(zhì)量管理的模塊勉抓。下圖是對(duì)其中要求的內(nèi)容的羅列贾漏。
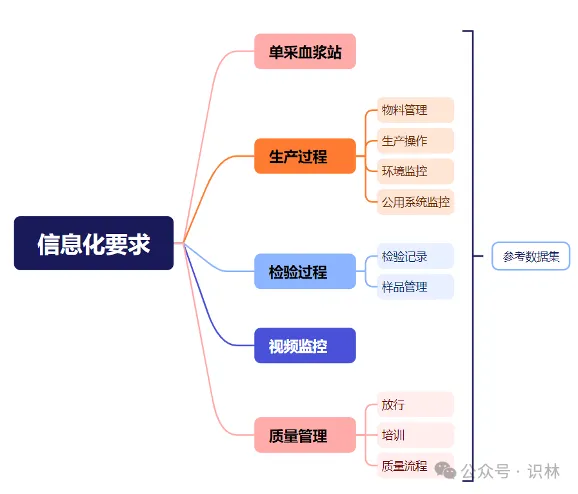
對(duì)生產(chǎn)檢驗(yàn)過(guò)程的改變
對(duì)生產(chǎn)過(guò)程的信息化是其中的重頭,但并非簡(jiǎn)單將由人員手工填寫(xiě)批記錄轉(zhuǎn)變?yōu)樵陔娔X/平板上填充批記錄藕筋。這涉及到對(duì)物料和設(shè)備的信息化轉(zhuǎn)化键腹,簡(jiǎn)單說(shuō)包括以下方面:
(1)物料:依據(jù)物料編碼規(guī)程使用計(jì)算機(jī)化系統(tǒng)對(duì)輔料、原材料蒂抒、包裝材料賦予唯一物料編碼溪客,編碼展現(xiàn)形式包括但不限于:一維碼,二維碼先兆。建議通過(guò)掃描物料編碼的方式對(duì)物料的稱量肢箕、配料、轉(zhuǎn)移褥欺、接收芍迫、儲(chǔ)存和使用進(jìn)行電子化記錄。
(2)設(shè)備:應(yīng)當(dāng)采用信息化手段對(duì)生產(chǎn)現(xiàn)場(chǎng)設(shè)備進(jìn)行合規(guī)性管理盔鬼,對(duì)設(shè)備進(jìn)行標(biāo)識(shí)(如一維碼哪趟、二維碼等)。設(shè)備可以實(shí)現(xiàn)運(yùn)行參數(shù)的自動(dòng)化采集女饺、監(jiān)測(cè)和控制纹怨。如因一些原因限制不能實(shí)現(xiàn)自動(dòng)化,應(yīng)當(dāng)采用人工錄入或其他輔助方式(如照片或視頻等)及時(shí)將生產(chǎn)及檢測(cè)過(guò)程信息轉(zhuǎn)化為電子數(shù)據(jù)儒恋。
在實(shí)現(xiàn)對(duì)物料和設(shè)備的信息轉(zhuǎn)化后善绎,再結(jié)合電子批記錄,設(shè)定操作順序和操作步驟間邏輯關(guān)聯(lián)诫尽,控制各工序和崗位的生產(chǎn)操作禀酱,提供生產(chǎn)操作指導(dǎo)并規(guī)范操作人員嚴(yán)格按照工藝規(guī)程執(zhí)行生產(chǎn)任務(wù)炬守。
對(duì)質(zhì)量管理的改變
在實(shí)現(xiàn)生產(chǎn)和檢驗(yàn)過(guò)程的信息化,自然就會(huì)帶來(lái)質(zhì)量管理方式的變化剂跟。尤其是對(duì)以往企業(yè)普遍感到棘手的偏差上報(bào)和調(diào)查時(shí)證據(jù)不足的情況减途,可以對(duì)信息化做如下要求:
根據(jù)預(yù)設(shè)的標(biāo)準(zhǔn)自動(dòng)捕獲或人工記錄異常情況,經(jīng)確認(rèn)為質(zhì)量偏差的曹洽,根據(jù)工藝規(guī)程和操作SOP中的規(guī)定鳍置,記錄生產(chǎn)過(guò)程中產(chǎn)生的偏差相關(guān)的電子數(shù)據(jù),包括但不限于偏差事件描述送淆、發(fā)生時(shí)間税产、緊急處理措施、受影響批次偷崩、偏差記錄人和復(fù)核人辟拷。
信息化的趨勢(shì)
雖然這份指南是對(duì)血液制品的信息化要求,但是在其他類別藥品行業(yè)中并非沒(méi)有類似要求蛾藐。如細(xì)胞治療產(chǎn)品行業(yè)也已經(jīng)出現(xiàn)了這種類似的系統(tǒng)瘤希,即COC/COI(監(jiān)管鏈/鑒別鏈)。它的出現(xiàn)背景也是因?yàn)榧?xì)胞產(chǎn)品需要嚴(yán)格追溯細(xì)胞供者來(lái)源保懈,避免污染和混淆差錯(cuò)。COC/COI有別于現(xiàn)有的藥品追溯碼的一大特點(diǎn)就是拆翘,它要求覆蓋細(xì)胞產(chǎn)品的全過(guò)程锉辫,而且將產(chǎn)品信息和各業(yè)務(wù)部門(mén)的操作(如批準(zhǔn)、傳達(dá)生產(chǎn)計(jì)劃等)結(jié)合囊脉。在CGT行業(yè)瑰兄,由于大多數(shù)企業(yè)還在早期研發(fā)和臨床試驗(yàn)期間,因此基本都沒(méi)有真正搭建引用電子化的COC/COI屉争,依靠一些獨(dú)立模塊的系統(tǒng)和紙質(zhì)記錄進(jìn)行從供者到受者的信息追溯和管控锤距。目前尚無(wú)對(duì)COC/COI的規(guī)范的定義和要求,市場(chǎng)上已有商業(yè)化的軟件系統(tǒng)也多是廠家各自調(diào)研后開(kāi)發(fā)檩讯,CGT企業(yè)在選擇時(shí)也面臨著選擇困境脸夜。
從設(shè)計(jì)角度,在企業(yè)要降本增效的同時(shí)仍需控制污染和差錯(cuò)風(fēng)險(xiǎn)干跛,必須要在企業(yè)內(nèi)進(jìn)行合理的信息化子姜,尤其是對(duì)生產(chǎn)和檢驗(yàn)過(guò)程,打破過(guò)往一些企業(yè)內(nèi)部分生產(chǎn)細(xì)節(jié)只有少數(shù)操作人員才知道的尷尬局面楼入。因此在其他一些高風(fēng)險(xiǎn)的生物制品行業(yè)哥捕,進(jìn)行更高程度的信息化建設(shè)也許是一個(gè)必要的趨勢(shì)。綜合分析嘉熊,血液制品已經(jīng)開(kāi)啟了全面信息化的道路遥赚,CGT行業(yè)在有了疫苗和血液制品的經(jīng)驗(yàn)后扬舒,可能會(huì)更快地開(kāi)展信息化建設(shè)。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍(lán)觀
深藍(lán)觀  2024-11-28
2024-11-28
 34
34

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 39
39

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 38
38
 熱門(mén)資訊
熱門(mén)資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽