
 產業(yè)資訊
產業(yè)資訊
 醫(yī)藥魔方
醫(yī)藥魔方  2024-06-28
2024-06-28
 535
535
癌癥锚拳,這個現(xiàn)代醫(yī)學面臨的最重大的課題,似乎已變得并非那么不可戰(zhàn)勝档徘。尤其是近十年來,以PD-(L)1為代表的免疫腫瘤藥物橫空出世咖迄,多次刷新各個腫瘤領域的治療標準刃纽,在深刻改變了癌癥治療格局的同時也收獲了巨大的商業(yè)成功,甚至成為化療之后溉浙,又一腫瘤治療的基石烫止。
正因如此,這一賽道從產品數(shù)量到獲批適應癥都已呈現(xiàn)極為擁擠的態(tài)勢:一邊是全球已有22款PD-(L)1單抗獲批上市戳稽,其中17款已在中國上市馆蠕、7款還在等待監(jiān)管機構批準;另一邊則是非小細胞肺癌惊奇、胃癌互躬、食管癌等大癌種的單藥/聯(lián)合化療方案幾乎被探索殆盡。留給后來者的市場空間只會越來越小颂郎。
另一方面吼渡,未被滿足的臨床需求始終存在,對更高療效目標的追求也遠未到盡頭乓序。而療效的突破往往建立在前人探索的基礎之上寺酪,正如同PD-(L)1的成功要很大程度上歸功于在各種標準化療方案上做“加法”,在PD-(L)1隱約已成為又一標準治療的當下替劈,探索“PD-(L)1+”治療模式——與更多藥物組成搭檔寄雀,或開發(fā)PD-(L)1多靶點藥物——已成為業(yè)界公認的重要突破口之一,各路玩家紛紛圍繞不同的思路展開了探索娇建。
各花入各眼百睹,PD-(L)1搭檔怎么選?
長期以來厘举,抗血管生成藥物是各家PD-(L)1產品除化療外最常規(guī)的搭檔阳框,例如卡博替尼、侖伐替尼屋赌、阿帕替尼船酗,以及大分子的貝伐珠單抗等。但這種組合療法的適應癥覆蓋局限于肝細胞癌弊肢、腎細胞癌等幾個特定癌種收泥。此外還有一些依賴特定靶點的靶向藥物(如抗HER2靶向藥物),與PD-(L)1的聯(lián)用更是僅局限于個別適應癥蠕为。
近年來琐店,隨著多款新型ADC展現(xiàn)出色的療效數(shù)據(jù)后贩俺,PD-(L)1+ADC組合隨即成為如今熱點之一,首個PD-1+ADC的聯(lián)用方案也已于去年4月獲FDA批準上市俊势。此外洋魂,其他新型方案,如各種新型免疫檢查點抑制劑(TIGIT等)與PD-(L)1的聯(lián)用喜鼓,以及各種PD-(L)1雙抗副砍,如PD-(L)1/CTLA-4雙抗、PD-(L)1/VEGF雙抗的探索同樣如火如荼庄岖。
不過豁翎,前沿治療模式的推廣總是伴隨著長時間的摸索、驗證過程隅忿。就目前而言心剥,上述新型“PD-(L)1+”模式的探索、應用都還處在起步階段背桐,其整體的獲益-風險比還有待在更大規(guī)模的真實世界應用中進一步驗證优烧,治療相關不良事件(TRAE)的管理經驗也還需進一步累積。處在當下免疫單藥/聯(lián)合化療的探索空間逐步縮小链峭、而新型方案仍然“青黃不接”的階段畦娄,面臨尚未被滿足的治療需求,臨床更亟需的可能是應用范圍更廣弊仪、且既能提升療效熙卡,又具有更高確定性的“PD-(L)1+”方案。
相對而言系亭,在另一條“PD-(L)1+”的路線——雙免領域,得益于更早的起步差赂,現(xiàn)有選擇已發(fā)展得更為成熟晋合。例如,全球首個“PD-1+CTLA-4”雙免疫聯(lián)合方案“O+Y”組合(納武利尤單抗+伊匹木單抗)至今已經過了近10年長期拨俏、廣泛的驗證掐腕,堪稱現(xiàn)階段“PD-(L)1+”方案中的“明牌”。
一方面智复,“O+Y”的協(xié)同作用機制明確捺再,且雙免的特點使得其不受特定靶點限制,覆蓋瘤種廣泛光樱,目前已在全球獲批9項適應癥糜隶,涵蓋黑色素瘤、腎細胞癌尿愿、結直腸癌会激、非小細胞肺癌、肝癌、胸膜間皮瘤锐涯、食管鱗癌磕诊,是迄今為止除聯(lián)合化療外,獲批適應癥最多的PD-(L)1組合療法纹腌。
另一方面霎终,“O+Y”經過了長時間、大規(guī)模人群的探索和應用升薯,其開展的10余項III期研究中莱褒,多數(shù)的最低隨訪時間已超過4年,部分研究(CheckMate-214/067)最低隨訪甚至已達到了90個月覆劈,有效性明確保礼,安全性可控。
盡管BMS同樣手握ADC等新型藥物管線责语,但目前來看炮障,“O+Y”這手“明牌”在陣中仍扮演著不可替代的角色。尤其是近期坤候,可以看到“O+Y”在適應癥拓展方面明顯發(fā)力胁赢,僅最近半年,就相繼取得了CheckMate-8HW與CheckMate-9DW兩項重量級III期臨床研究的成功投篇。
值得一提的是欠杀,這兩項研究對應的癌種分別為結直腸癌和肝細胞癌,均屬于消化腫瘤爸备,這也延續(xù)了O藥一直以來在中國市場深耕高發(fā)的消化道癌種讯策、緊盯未滿需求的傳統(tǒng):早在胃癌、食管癌等上消化道大適應癥仍存未被覆蓋的時代荤勤,O藥就憑借CheckMate-649/648/577等經典研究购烹,在所有PD-(L)1中率先完成了上消化道領域疾病部位和病理類型的全面覆蓋,填補了大量臨床空白鹉陪。
從CheckMate-8HW與CheckMate-9DW可以看出底教,O藥在中國市場的擴張步伐仍在延續(xù)上述思路,從上消化道拓展到了更廣泛的消化腫瘤領域——其實不停變化的不只是持續(xù)更迭的治療方案戴悔,疾病負擔也在變:根據(jù)最新數(shù)據(jù)[1]扑澜,肝癌和結直腸癌已超越胃癌,成為中國發(fā)病率最高的兩類消化腫瘤俏汇。不僅如此鹿响,中國肝癌和結直腸癌患者也是更容易從免疫治療獲益的群體。因而谷饿,于中國患者而言抢野,上述兩項免疫治療的突破顯得尤為關鍵拷淘。
但此時畢竟不同于2020年:目前,免疫治療早已成為了這兩大癌種的一線標準治療指孤。不過启涯,這一背景恰恰也給了“PD-(L)1+”模式更大的施展舞臺:通過發(fā)掘其中仍未被滿足的臨床需求,“O+Y”組合在兩項研究中均成功突破了現(xiàn)有治療方式的瓶頸恃轩,觸達了更高的療效目標结洼。
接下來,本文也將結合“O+Y”的機制及療效特點叉跛,圍繞具體研究試對上述思路做進一步闡釋松忍。
優(yōu)勢互補、高效協(xié)同:雙免組合的機制奧秘
“O+Y”不僅在既往多項III期研究中被證實獲益顯著筷厘,而且在后續(xù)隨訪中表現(xiàn)出長期鸣峭、持續(xù)的應答。以今年的ASCO大會上土汽,針對食管鱗癌一線治療的III期CheckMate-648研究45個月隨訪結果為例音虹,經過近4年隨訪,接受“O+Y”組合治療的患者在長期生存率和緩解持續(xù)時間(DOR)上獲益更為明顯奥挑。這一療效特點的背后次新,是“O+Y”明確的作用機制優(yōu)勢。
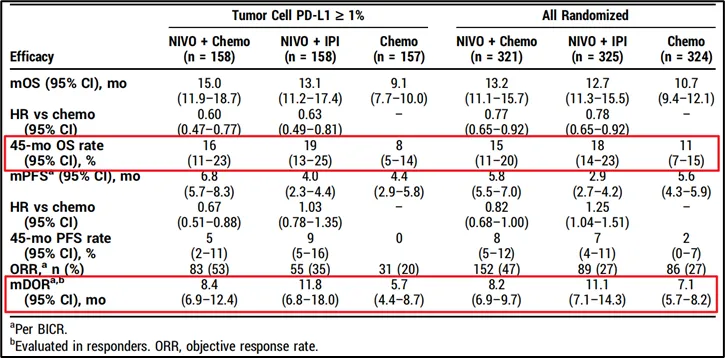
CheckMate-648研究45個月隨訪結果 來源:ASCO 2024大會摘要[2]
O藥和Y藥分別靶向的PD-1與CTLA-4均為免疫檢查點分子声锤,但兩者的作用階段傲枕、機制有所不同,分工明確:
CTLA-4抑制劑——Y藥主要作用于T細胞的活化階段衙文,可控制初始T細胞(包括記憶性T細胞)的活化辩芦,激活T細胞識別低親合力抗原,增殖為效應T細胞浆菇,增加能夠識別腫瘤的克隆數(shù)遥加;
而PD-1抑制劑——O藥主要作用于T細胞的效應階段,直接阻斷腫瘤細胞上的程序性死亡配體1(PD-L1)和T細胞上PD-1結合赫斥,解除腫瘤細胞的免疫“剎車”作用卤竭,重新激活T細胞沪么,增強了T細胞效應功能硼婿。
除了上述經典機制解釋外,近年來有一種觀點認為[3]禽车,Y藥還可通過其抗體依賴細胞介導的細胞毒性作用(ADCC效應)寇漫,清除腫瘤微環(huán)境內異常高表達CTLA-4的調節(jié)性T細胞(Treg)[4],從而進一步解除免疫抑制殉摔、加強抗腫瘤效果州胳,這一機制使得“O+Y”有別于現(xiàn)有的PD-1/CTLA-4雙抗藥物:PD-1/CTLA-4雙抗的靶細胞也包括效應階段的T細胞记焊,因此在藥物設計中必須去除其ADCC效應以防止活化的T細胞被吞噬[5],而這也可能導致?lián)p失ADCC效應帶來的這部分潛在療效栓撞。
總之遍膜,“O+Y”組合通過合理的機制互補與協(xié)同效應,可以充分調動人體內的免疫“大軍”瓤湘,并改善長期免疫監(jiān)視瓢颅,實現(xiàn)高效、持久的抗腫瘤效果弛说。也正是通過將其機制挽懦、療效優(yōu)勢與未滿足的臨床需求相結合,“O+Y”近期在CheckMate-8HW與CheckMate-9DW兩項重磅研究中取得成功舷到,進一步夯實了自身地位这旋。
CheckMate-8HW研究:MSI-H/dMMR結直腸癌一線療效創(chuàng)新高
國家癌癥中心最新數(shù)據(jù)顯示[1],結直腸癌(CRC)已取代胃癌夹卒,成為中國最高發(fā)的消化腫瘤忌舔,在所有癌癥中位居第二,僅次于肺癌鉴何。CRC的治療現(xiàn)狀不容樂觀茴夯,其一線治療首選仍為化療,但其中有一類人群較為特殊——微衛(wèi)星高度不穩(wěn)定/錯配修復缺陷表型(MSI-H/dMMR)結直腸癌患者矢妄。這類患者對一般的靶向療法應答不佳屁茁,但對免疫檢查點抑制劑敏感。因此汇氛,這類患者也是免疫治療的重點人群组伐。
目前,全球僅有一項PD-1單藥適應癥獲批用于一線治療MSI-H/dMMR CRC呛靡。相比于化療硕帖,PD-1單藥雖能將患者的疾病進展或死亡風險降低41%,但其在短期和長期獲益上仍有提高的空間铅鲤。短期方面划提,患者對PD-1單藥的應答率較低,約30%的患者無法從中獲益邢享,用藥后快速出現(xiàn)進展鹏往;長期來看,2年PFS率不足50%[6]骇塘。
那么伊履,在PD-1單藥的基礎上加入另一免疫治療藥物,是否會成為該類患者療效進一步提升的突破口款违?年初舉行的ASCO-GI大會上唐瀑,CheckMate-8HW研究用震撼性的數(shù)據(jù)給出了回答:相比于化療方案群凶,“O+Y”組合可將患者的疾病進展風險降低79%,2年PFS率高達72%[7]哄辣。

CheckMate-8HW主要終點:PFS
以上數(shù)據(jù)為雙免療法在機制層面良好的協(xié)同效應提供了又一項有力例證请梢,且這一效應在MSI-H/dMMR這一優(yōu)勢人群中可能被進一步放大,最終使得整體療效在PD-1單藥的高水準之上實現(xiàn)了又一次突破力穗。不僅如此驳疚,“O+Y”的安全性一如既往得穩(wěn)定可控,其3-4級TRAE發(fā)生率僅為化療組一半(23% vs. 48%)浅腥。
如果說CheckMate-8HW的PFS數(shù)據(jù)帶給人的感受是“震撼”贞触,那么本次ASCO大會上公布的PFS2結果[7](即一線治療進展+二線治療進展/死亡的時間)則更深層次地體現(xiàn)了雙免治療強大而獨特的“記憶”效應,可為后續(xù)免疫治療的全過程提供獲益:在對照組高達67%患者接受后續(xù)免疫治療的情況下鱼雇,“O+Y”仍可降低73%的二次進展或死亡風險吗屏。
值得一提的是,這項研究還包括一個O藥單藥對照組(尚未披露結果)礼猪。從這一設計可以看出來菱戒,“O+Y”在追求更高的絕對療效的同時,也并不回避和目前標準的PD-1單藥進行比較硅盹,這在PD-(L)1藥物逐漸坐穩(wěn)腫瘤治療“基石”地位的當下倒是頗有些未雨綢繆的意味慧跋。
近期,NMPA已授予“O+Y”組合用于一線治療MSI-H結直腸癌的新適應癥上市申請優(yōu)先審評資格又竞,國內這類患者有望很快迎來全新的一線治療方案械兽。
CheckMate-9DW研究:免疫治療用于肝癌一線首次優(yōu)于侖伐替尼
而在中國同樣高發(fā)的肝癌領域,如今已不再缺乏治療選擇咸唇,但缺少療效足夠好的藥物:
一方面呈驶,現(xiàn)有的一線免疫治療方案ORR多數(shù)不足30%,且應答短暫疫鹊,長期生存獲益局限袖瞻;
另一方面,翻閱這些免疫治療方案III期研究的設計拆吆,會發(fā)現(xiàn)獲批近20年之久的索拉非尼仍是對照組的“常駐嘉賓”——盡管早在2018年聋迎,REFLECT研究就證實侖伐替尼幾乎全面優(yōu)于索拉非尼,但截至CheckMate-9DW前枣耀,仍沒有任何免疫療法在III期研究中頭對頭打敗侖伐替尼霉晕。
在此背景下開展的CheckMate-9DW并不滿足于拿到一個和同類研究相近的結果,從研究設計便足見其雄心勃勃:試驗主角選擇了“O+Y”組合的同時奕枢,挑戰(zhàn)對象也從一位(索拉非尼)增加至兩位(研究者選擇的侖伐替尼或索拉非尼)娄昆。
事后來看佩微,CheckMate-9DW的對照組高達85%的患者選用了侖伐替尼缝彬,側面反映出研究的設計不僅更貼合臨床實踐萌焰,以患者為中心,也意在挑戰(zhàn)更高的療效目標谷浅。
今年ASCO篱瀑,CheckMate-9DW研究作為肝膽腫瘤領域唯一的LBA入選大會。結果不負眾望椅砸,“O+Y”組合成為了第一個在頭對頭研究中戰(zhàn)勝侖伐替尼的肝癌一線治療方案送县,將整體療效提升到了一個新的高度——ORR首次達到36%,而且一旦有效嫡服,獲益持久:中位獲益時間超過30個月桌偎,近一半患者的OS可達到兩年,使其得以在一眾治療方案中脫穎而出伴竹。

CheckMate-9DW:主要結果 來源:ASCO 2024大會摘要[8]
不僅如此徊岂,以上數(shù)據(jù)都是中期分析的結論(中位隨訪35.2個月)”ㄈ考慮到“O+Y”目前表現(xiàn)出的突出應答率田漓、應答持續(xù)時間和既往研究中普遍觀察到的“長尾效應”,隨著隨訪時間延長付找,可以期待其長期生存優(yōu)勢還有進一步擴大的空間歧胃。
PD-(L)1成為基石后的下一步:變化的環(huán)境,與不變的應對
在免疫治療的競爭進入下半場艰争,“PD-(L)1+”模式的競爭成為主旋律之一的當下坏瞄,如何才能確保自身的競爭優(yōu)勢?“O+Y“雙免組合提供了頗具價值的參考:在不斷動態(tài)變化的外界環(huán)境中甩卓,我們仍能總結出一些不變的應對之道惦积。
首先,做好充分的前瞻性布局猛频,才能在轉變來臨時手握具有確定性的“明牌”狮崩,穩(wěn)健地謀得“先手”;
其次鹿寻,不止步于現(xiàn)有療效睦柴,不斷挑戰(zhàn)更高標準:即便是在免疫治療已成為標準的領域,療效始終存在進一步提升的空間毡熏;
最后坦敌,也是最關鍵的一點:始終將未被滿足的臨床需求作為突破口:創(chuàng)新藥的競爭,歸根結底還是洞悉臨床需求痢法、滿足臨床需求的競爭狱窘。
參考資料
[1] Cancer incidence and mortality in China, 2022.
[2] Nivolumab (NIVO) plus chemotherapy (chemo) or ipilimumab (IPI) vs chemo as first-line (1L) treatment for advanced esophageal squamous cell carcinoma (ESCC): 45-month (mo) follow-up from CheckMate 648.
[3] https://mp.weixin.qq.com/s/AJ9Xytw2FGEXYxPuYD7FZQ
[4] Anti-CTLA-4 antibodies in cancer immunotherapy: selective depletion of intratumoral regulatory T cells or checkpoint blockade?
[5] Cadonilimab, a tetravalent PD-1/CTLA-4 bispecific antibody with trans-binding and enhanced target binding avidity
[6] Pembrolizumab versus chemotherapy for microsatellite instability-high or mismatch repair-deficient metastatic colorectal cancer (KEYNOTE-177): final analysis of a randomised, open-label, phase 3 study.
[7] Nivolumab (NIVO) plus ipilimumab (IPI) vs chemotherapy (chemo) as first-line (1L) treatment for microsatellite instability-high/mismatch repair-deficient (MSI-H/dMMR) metastatic colorectal cancer (mCRC): Expanded efficacy analysis from CheckMate 8HW.
[8] Nivolumab (NIVO) plus ipilimumab (IPI) vs lenvatinib (LEN) or sorafenib (SOR) as first-line treatment for unresectable hepatocellular carcinoma (uHCC): First results from CheckMate 9DW.

 產業(yè)資訊
產業(yè)資訊
 深藍觀
深藍觀  2024-11-28
2024-11-28
 22
22

 產業(yè)資訊
產業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 27
27

 產業(yè)資訊
產業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 26
26