
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-06-28
2024-06-28
 455
455
優(yōu)先審評是中國國家藥品監(jiān)督管理局藥品審評中心(CDE)推出的加速藥物獲批上市的重要政策之一念婶。根據(jù)CDE發(fā)布的《2023年度藥品審評報告》巢季,獲得優(yōu)先審評審批的藥物上市注冊申請的審評時限由常規(guī)程序的200日縮短為130日,獲批速度顯著提升诚摹。
根據(jù)CDE官網(wǎng)公示信息哺肘,截至6月27日,2024年上半年共計有26個創(chuàng)新藥的上市申請正式被納入優(yōu)先審評渗稍。從治療領(lǐng)域來看佩迟,抗腫瘤藥物最多,有17個竿屹,占比超65%报强。本文中就讓我們來看看這些抗腫瘤藥物都有哪些?它們都有望惠及哪些癌癥患者拱燃?

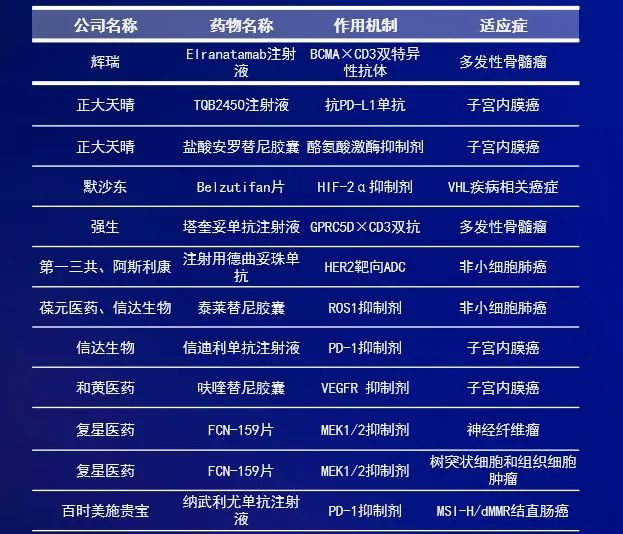
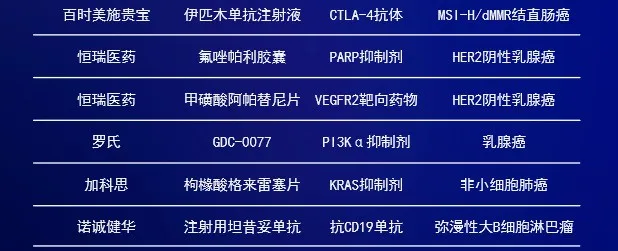
數(shù)據(jù)來源:CDE官網(wǎng)秉溉,《醫(yī)藥觀瀾》梳理。本表僅統(tǒng)計正式被納入優(yōu)先審評的藥物碗誉,不含擬納入藥品召嘶。統(tǒng)計截至日期:2024年6月27日
輝瑞:elranatamab注射液
作用機(jī)制:BCMA×CD3雙特異性抗體
適應(yīng)癥:多發(fā)性骨髓瘤
2024年1月,輝瑞(Pfizer)公司的elranatamab注射液上市申請被CDE納入優(yōu)先審評哮缺,用于治療既往接受過至少三種治療的復(fù)發(fā)或難治性多發(fā)性骨髓瘤(MM)成人患者弄跌。Elranatamab是一款皮下注射BCMA×CD3雙特異性抗體,其一端與骨髓瘤細(xì)胞上的BCMA相結(jié)合尝苇,另一端與T細(xì)胞表面的CD3受體結(jié)合碟绑,使它們結(jié)合在一起并激活T細(xì)胞殺死骨髓瘤細(xì)胞。該藥已于2023年獲FDA加速批準(zhǔn)榛舍,用于治療復(fù)發(fā)/難治性MM患者溃杖。
正大天晴:TQB2450、安羅替尼
作用機(jī)制:抗PD-L1單抗耽慌、酪氨酸激酶抑制劑
適應(yīng)癥:子宮內(nèi)膜癌
2024年1月卢圈,正大天晴申報的TQB2450注射液和安羅替尼膠囊聯(lián)合療法的一項上市申請被CDE納入優(yōu)先審評, 擬用于治療既往接受過一辅任、二線化療方案治療失敗或不能耐受的非微衛(wèi)星高度不穩(wěn)定(非MSI-H)或非DNA錯配修復(fù)缺陷(非dMMR)的復(fù)發(fā)性或轉(zhuǎn)移性子宮內(nèi)膜癌患者借衅。貝莫蘇拜單抗(TQB2450)是一款抗PD-L1人源化單克隆抗體,已于今年5月獲批聯(lián)合安羅替尼膠囊和依托泊苷及卡鉑一線治療廣泛期小細(xì)胞肺癌立漏。安羅替尼是一種新型小分子多靶點(diǎn)酪氨酸激酶抑制劑鹊属,此前已在中國獲批用于治療多種腫瘤適應(yīng)癥冶媚。
默沙東:belzutifan片
作用機(jī)制:HIF-2α抑制劑
適應(yīng)癥:血管母細(xì)胞瘤或胰腺神經(jīng)內(nèi)分泌腫瘤
2024年2月,默沙東(MSD)的belzutifan片上市申請被CDE納入優(yōu)先審評危劫,擬用于治療von Hippel-Lindau(VHL)病相關(guān)腎細(xì)胞癌彭旬、中樞神經(jīng)系統(tǒng)血管母細(xì)胞瘤或胰腺神經(jīng)內(nèi)分泌腫瘤。VHL是一種罕見遺傳疾病容诬,它可異常激活癌癥患者體內(nèi)的缺氧誘導(dǎo)因子(HIF-2α)娩梨。Belzutifan是一款選擇性新型口服HIF-2α抑制劑,此前已獲FDA批準(zhǔn)用于治療VHL疾病相關(guān)癌癥览徒。
強(qiáng)生:塔奎妥單抗
作用機(jī)制:GPRC5D×CD3雙抗
適應(yīng)癥:多發(fā)性骨髓瘤
2024年2月狈定,強(qiáng)生(Johnson & Johnson)公司申報的塔奎妥單抗注射液被CDE納入優(yōu)先審評,單藥治療既往接受過至少三種治療的復(fù)發(fā)或難治性多發(fā)性骨髓瘤成人患者习蓬。公開資料顯示纽什,塔奎妥單抗(talquetamab)是一款皮下注射雙特異性抗體,靶向GPRC5D和CD3躲叼,已于2023年8月獲美國FDA加速批準(zhǔn)上市芦缰,用于治療復(fù)發(fā)性或難治性多發(fā)性骨髓瘤成人患者。
第一三共押赊、阿斯利康:德曲妥珠單抗
作用機(jī)制:HER2靶向ADC
適應(yīng)癥:非小細(xì)胞肺癌
2024年2月,第一三共(Daiichi Sankyo)公司申報的注射用德曲妥珠單抗被CDE正式納入優(yōu)先審評包斑,擬定適應(yīng)癥為:存在HER2(ERBB2)激活突變且既往接受過至少一種系統(tǒng)治療的不可切除或轉(zhuǎn)移性成人NSCLC患者流礁。德曲妥珠單抗是阿斯利康(AstraZeneca)和第一三共聯(lián)合開發(fā)的一款靶向HER2的抗體偶聯(lián)藥物(ADC),此前已在中國獲批治療HER2陽性和HER2低表達(dá)成人乳腺癌患者罗丰。
葆元醫(yī)藥/信達(dá)生物:泰萊替尼
作用機(jī)制:ROS1抑制劑
適應(yīng)癥:非小細(xì)胞肺癌
2024年2月神帅,葆元醫(yī)藥(現(xiàn)已被Nuvation Bio收購)申報的泰萊替尼膠囊上市申請被CDE納入優(yōu)先審評,用于未經(jīng)ROS1-TKI治療的ROS1陽性局部晚期或轉(zhuǎn)移性NSCLC成人患者的治療腊囤。泰萊替尼是新一代口服選擇性ROS1抑制劑几菲,具有腦滲透潛力。2021年6月韭展,葆元與信達(dá)生物簽訂了獨(dú)家許可協(xié)議杉唇,在大中華區(qū)(包括中國大陸、香港酬裆、澳門和臺灣地區(qū))共同開發(fā)和商業(yè)化泰萊替尼辟侠。
信達(dá)生物、和黃醫(yī)藥:信迪利單抗葱有、呋喹替尼
作用機(jī)制:PD-1抑制劑眨柑、VEGFR抑制劑
適應(yīng)癥:子宮內(nèi)膜癌
2024年3月,信達(dá)生物的PD-1抑制劑信迪利單抗與和黃醫(yī)藥的VEGFR抑制劑呋喹替尼的聯(lián)合療法上市申請被CDE納入優(yōu)先審評复做,擬用于既往系統(tǒng)性抗腫瘤治療后疾病進(jìn)展且不適合進(jìn)行根治性手術(shù)治療或根治性放療的晚期pMMR或non MSI-H子宮內(nèi)膜癌患者坪腔。公開資料顯示权浸,信達(dá)生物與和黃醫(yī)藥曾在2018年達(dá)成合作,開展信迪利單抗與呋喹替尼用于實(shí)體瘤聯(lián)合治療的研究吏口。
復(fù)星醫(yī)藥:FCN-159
作用機(jī)制:MEK1/2抑制劑
適應(yīng)癥:樹突狀細(xì)胞和組織細(xì)胞腫瘤奄容、神經(jīng)纖維瘤
2024年4月,復(fù)星醫(yī)藥的FCN-159片(復(fù)邁替尼)上市申請被CDE納入優(yōu)先審評锨侯,擬用于治療成人樹突狀細(xì)胞和組織細(xì)胞腫瘤嫩海。2024年5月,F(xiàn)CN-159片的新適應(yīng)癥上市申請再次被CDE納入優(yōu)先審評囚痴,用于治療2歲及2歲以上兒童1型神經(jīng)纖維瘤踩帧(NF1)相關(guān)的叢狀神經(jīng)纖維瘤。FCN-159為一款MEK1/2選擇性抑制劑深滚,可以抑制RAS通路異常引起的腫瘤增殖奕谭,擬開發(fā)主要用于治療晚期實(shí)體瘤、I型神經(jīng)纖維瘤痴荐、樹突狀細(xì)胞和組織細(xì)胞腫瘤血柳、低級別腦膠質(zhì)瘤等適應(yīng)癥。
百時美施貴寶:伊匹木單抗生兆、納武利尤單抗
作用機(jī)制:CTLA-4抗體难捌、PD-1抑制劑
適應(yīng)癥:MSI-H/dMMR結(jié)直腸癌
2024年3月和4月,伊匹木單抗注射液和納武利尤單抗注射液的聯(lián)合療法上市申請先后兩次被CDE納入優(yōu)先審評鸦难,針對的適應(yīng)癥均為兩種藥物聯(lián)合用于一線治療不可切除或轉(zhuǎn)移性微衛(wèi)星高度不穩(wěn)定性(MSI-H)或錯配修復(fù)缺陷型(dMMR)結(jié)直腸癌患者垮允。伊匹木單抗是一款CTLA-4抗體,納武利尤單抗是一款PD-1抑制劑水仑。今年3月蒿缎,伊匹木單抗聯(lián)合納武利尤單抗一線治療MSI-H/dMMR結(jié)直腸癌的申請已被CDE納入突破性治療藥物品種。
恒瑞醫(yī)藥:阿帕替尼颂芒、氟唑帕利
作用機(jī)制:VEGFR2靶向藥物菠告、PARP抑制劑
適應(yīng)癥:HER2陰性乳腺癌
2024年4月,恒瑞醫(yī)藥的甲磺酸阿帕替尼片和氟唑帕利膠囊各有一項新適應(yīng)癥上市申請被CDE納入優(yōu)先審評乱感。其中蚜冀,阿帕替尼是一款VEGFR2靶向藥物,本次申報上市的適應(yīng)癥是聯(lián)合氟唑帕利用于治療伴有胚系BRCA突變(gBRCAm)的HER2-乳腺癌患者蠢耻。氟唑帕利是一款PARP抑制劑残昔,本次申報上市的適應(yīng)癥是單藥或聯(lián)合阿帕替尼用于治療伴有胚系BRCA突變的HER2-乳腺癌患者。
羅氏:GDC-0077
作用機(jī)制:PI3Kα抑制劑
適應(yīng)癥:乳腺癌
2024年4月佑茴,羅氏(Roche)GDC-0077(inavolisib)的上市申請被CDE納入優(yōu)先審評物即,擬與CDK4/6抑制劑哌柏西利和內(nèi)分泌療法聯(lián)合用藥,用于治療PIK3CA突變键闺、HR陽性/HER2陰性的局部晚期或轉(zhuǎn)移性乳腺癌成人患者寿烟。公開資料顯示澈驼,PIK3CA基因突變在大約40%的HR陽性乳腺癌中被發(fā)現(xiàn),GDC-0077是一種具有雙重作用機(jī)制的口服療法筛武,具有高度的體外PI3Kα抑制效力和選擇性缝其,且能夠特異性觸發(fā)PI3Kα蛋白突變體的分解。
加科思:格來雷塞
作用機(jī)制:KRAS抑制劑
適應(yīng)癥:非小細(xì)胞肺癌(NSCLC)
2024年5月徘六,加科思格來雷塞片(JAB-21822片)的上市申請被CDE納入優(yōu)先審評内边,擬用于既往接受過至少一線系統(tǒng)性治療的KRAS G12C突變的局部晚期或轉(zhuǎn)移性NSCLC成人患者的治療。格來雷塞是一款KRAS G12C抑制劑待锈,本次上市申請是基于在中國開展的2期注冊性臨床研究結(jié)果漠其。數(shù)據(jù)顯示,格來雷塞單藥治療KRAS ?G12C突變NSCLC患者竿音,確認(rèn)的客觀緩解率(ORR)為47.9%和屎,疾病控制率(DCR)為86.3%,中位無進(jìn)展生存期(mPFS)為8.2個月春瞬,中位總生存期(mOS)為13.6個月柴信。
諾誠健華:坦昔妥單抗
作用機(jī)制:抗CD19單抗
適應(yīng)癥:彌漫性大B細(xì)胞淋巴瘤(DLBCL)
2024年6月,諾誠健華注射用坦昔妥單抗的上市申請被CDE納入優(yōu)先審評费犯,擬聯(lián)合來那度胺用于治療復(fù)發(fā)或難治性且不適合自體干細(xì)胞移植的DLBCL成人患者浸弦。坦昔妥單抗是諾誠健華從Incyte公司引進(jìn)的一款靶向CD19的Fc結(jié)構(gòu)域優(yōu)化的人源化單克隆抗體,此前已獲得美國FDA以和歐洲藥品管理局(EMA)批準(zhǔn)上市绷冈,聯(lián)合來那度胺治療不適合自體干細(xì)胞移植條件的復(fù)發(fā)/難治性DLBCL患者弹噩。
除了上述正式被納入優(yōu)先審評的抗腫瘤藥物,近日還有三款抗腫瘤新藥被CDE納入了擬優(yōu)先審評公示名單弦撤,分別為:
和黃醫(yī)藥遞交的EZH2甲基轉(zhuǎn)移酶抑制劑他澤司他僻一,擬用于治療EZH2突變陽性且既往接受過至少兩種系統(tǒng)性治療的復(fù)發(fā)或難治性濾泡性淋巴瘤成人患者幅裳;
阿斯利康的第三代EGFR-TKI奧希替尼的新適應(yīng)癥上市申請鼠基,擬用于接受含鉑放化療期間或之后未出現(xiàn)疾病進(jìn)展、具有EGFR外顯子19缺失或外顯子21(L858R)置換突變的局部晚期铆寓、不可切除(III期)NSCLC成人患者的治療假怔;
精準(zhǔn)生物的pCAR-19B細(xì)胞自體回輸制劑(普基侖賽注射液),擬用于治療3~21歲CD19陽性的復(fù)發(fā)或難治性B細(xì)胞急性淋巴細(xì)胞白血病患者陵蜻。
希望這些抗腫瘤新藥能夠早日獲批怕收,為廣大癌癥患者帶來新的治療選擇。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 深藍(lán)觀
深藍(lán)觀  2024-11-28
2024-11-28
 22
22

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 瞪羚社
瞪羚社  2024-11-28
2024-11-28
 26
26

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 丹諾醫(yī)藥
丹諾醫(yī)藥  2024-11-28
2024-11-28
 26
26
 熱門資訊
熱門資訊