
 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-07-08
2024-07-08
 703
703
Vertex Pharmaceuticals今天宣布状答,美國(guó)FDA已接受其每日一次vanzacaftor/tezacaftor/deutivacaftor三聯(lián)療法(vanza三聯(lián)療法)治療6歲及以上的囊性纖維化(CF)患者的新藥申請(qǐng)(NDA)庵偏,這些患者至少帶有F508del突變或囊性纖維化跨膜傳導(dǎo)調(diào)節(jié)器(CFTR)基因中的另一個(gè)應(yīng)答性突變衬朗。帶有這些突變的患者對(duì)vanza三聯(lián)療法產(chǎn)生應(yīng)答。Vertex對(duì)此申請(qǐng)使用了優(yōu)先審評(píng)券盹挑,PDUFA的目標(biāo)日期為2025年1月2日免都。此外侮搭,歐洲藥品管理局(EMA)也完成Vertex在歐盟提交該療法針對(duì)6歲及以上CF患者的上市許可申請(qǐng)(MAA)的驗(yàn)證蝶桑。該公司也已在加拿大、澳大利亞柱丐、瑞士和英國(guó)提交了監(jiān)管申請(qǐng)腌径。
分析顯示,vanza三聯(lián)療法在三項(xiàng)3期臨床試驗(yàn)中獲得積極結(jié)果凉危。在名為SKYLINE 102和SKYLINE 103的隨機(jī)雙盲笔骏,含活性對(duì)照的3期臨床試驗(yàn)中,在隨機(jī)分組前粮森,患者接受了4周獲批療法Trikafta初始治療撒沦,以建立預(yù)測(cè)的一秒用力呼氣量百分比(ppFEV1)、汗液氯化物(SwCl)及其他療效參數(shù)的基線值。然后患者隨機(jī)接受Trikafta或vanza三聯(lián)療法的治療租藻。
試驗(yàn)結(jié)果顯示,接受治療24周后唉地,基于ppFEV1數(shù)值的評(píng)估据悔,vanza三聯(lián)療法的療效與活性對(duì)照藥物相當(dāng),達(dá)到試驗(yàn)的主要終點(diǎn)耘沼。
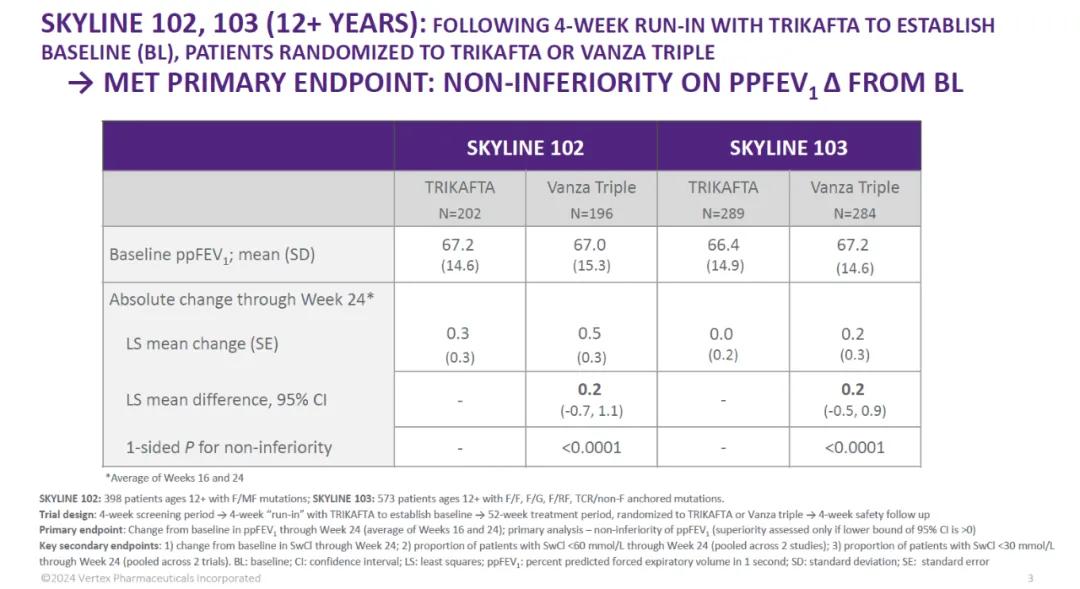
▲Vanza三聯(lián)療法在SKYLINE 102和SKYLINE 103中達(dá)到主要終點(diǎn)(圖片來(lái)源:Vertex公司官網(wǎng))
SKYLINE 102和SKYLINE 103中的關(guān)鍵次要終點(diǎn)包括與活性對(duì)照藥物相比极颓,第24周與基線相比的SwCl絕對(duì)變化,SwCl低于60 mmol/L的患者比例群嗤,以及SwCl低于30 mmol/L的患者比例菠隆。
試驗(yàn)結(jié)果顯示,vanza三聯(lián)療法在SKYLINE 102和SKYLINE 103的第一個(gè)關(guān)鍵次要終點(diǎn)上狂秘,在降低SwCl水平方面表現(xiàn)出優(yōu)效性骇径。
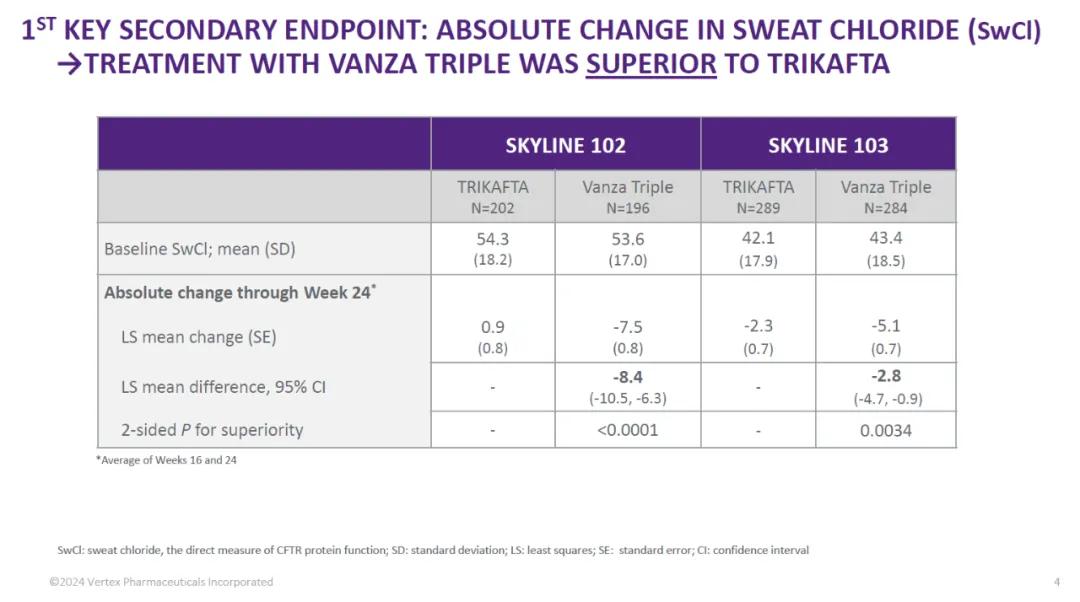
▲Vanza三聯(lián)療法與活性對(duì)照藥物相比,在降低SwCl水平方面表現(xiàn)出優(yōu)效性(圖片來(lái)源:Vertex官網(wǎng))
在第二和第三個(gè)關(guān)鍵次要終點(diǎn)上者春,vanza三聯(lián)療法也表現(xiàn)出優(yōu)效性破衔。其他次要終點(diǎn)的結(jié)果與主要終點(diǎn)和關(guān)鍵次要終點(diǎn)的結(jié)果一致。此外钱烟,52周的結(jié)果與24周的結(jié)果一致晰筛。
在RIDGELINE 105研究中,6-11歲兒童也遵循了相同的方案昆颇,先接受至少4周的Trikafta治療以建立基線值镐怔,然后再接受vanza三聯(lián)療法治療。這項(xiàng)研究主要關(guān)注的是安全性侣赘。在所有三項(xiàng)研究中麦葱,vanza三聯(lián)療法耐受性良好,與活性對(duì)照藥物治療組的安全性特征相似扳引。此外橡宪,vanza三聯(lián)療法在6至11歲的兒童中的安全性與12歲及以上人群中的安全性類似。
在CF患者中蛙府,CFTR基因的突變導(dǎo)致細(xì)胞表面CFTR蛋白通道的數(shù)量和/或功能減少慷尸。Vanzacaftor和tezacaftor旨在通過(guò)促進(jìn)CFTR蛋白的加工和運(yùn)輸,增加細(xì)胞表面CFTR蛋白數(shù)量的校正劑树聪。Deutivacaftor是一種增效劑瘤嗜,旨在增加送達(dá)細(xì)胞表面的CFTR蛋白的通道開(kāi)放概率,以改善細(xì)胞膜上鹽和水的流動(dòng)胡电。這款三聯(lián)療法已經(jīng)獲得美國(guó)FDA授予的快速通道資格和孤兒藥資格着还。

 研發(fā)追蹤
研發(fā)追蹤
 藥時(shí)代
藥時(shí)代  2024-09-02
2024-09-02
 107
107

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方
醫(yī)藥魔方  2024-09-02
2024-09-02
 111
111
 研發(fā)追蹤
研發(fā)追蹤
 藥融圈
藥融圈  2024-09-02
2024-09-02
 125
125
 熱門(mén)資訊
熱門(mén)資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽