
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-08-16
2024-08-16
 73
73
8月14日渔工,中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心(CDE)官網(wǎng)公示唬研,科倫博泰注射用蘆康沙妥珠單抗擬納入優(yōu)先審評(píng)炮捧,用于經(jīng)表皮生長(zhǎng)因子受體酪氨酸激酶抑制劑(EGFR-TKI)和含鉑化療治療失敗的局部晚期或轉(zhuǎn)移性EGFR突變非小細(xì)胞肺癌成人患者袱黎。公開資料顯示骇窍,蘆康沙妥珠單抗是一款靶向TROP2的ADC逾冬。在一項(xiàng)2期拓展臨床研究中,接受蘆康沙妥珠單抗單藥治療(5mg/kg,Q2W)的EGFR突變經(jīng)治局部晚期或轉(zhuǎn)移性NSCLC患者疾病控制率(DCR)達(dá)到100%瓮恭。
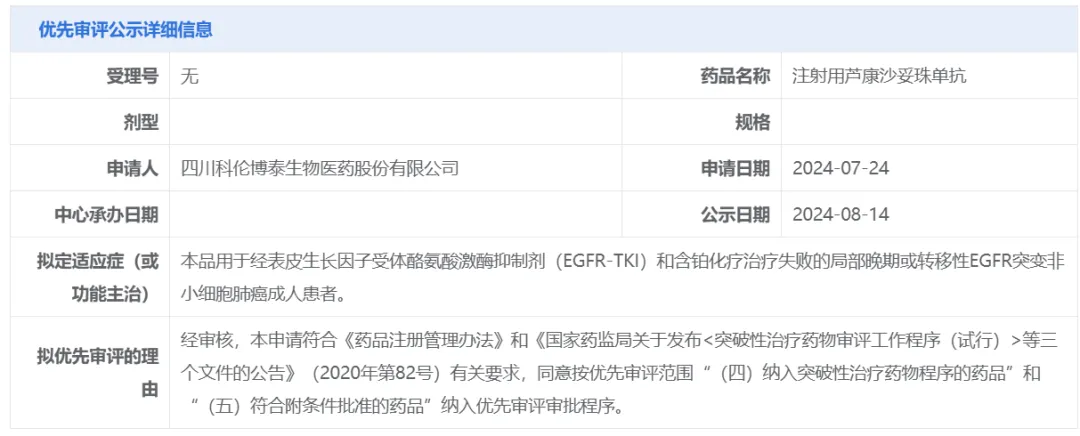
截圖來(lái)源:CDE官網(wǎng)
據(jù)科倫藥業(yè)早先新聞稿介紹雄坪,在亞洲人群中,EGFR突變是肺腺癌患者最常見的驅(qū)動(dòng)基因突變屯蹦,發(fā)生率約為50%维哈。目前,EGFR-TKI是EGFR突變晚期非小細(xì)胞肺癌的一線標(biāo)準(zhǔn)治療方案登澜。然而阔挠,三代TKI的無(wú)進(jìn)展生存期(PFS)約18-20個(gè)月,耐藥不可避免脑蠕,且耐藥后治療選擇和療效有限购撼,存在巨大的未滿足臨床需求。TROP-2的過(guò)表達(dá)在腫瘤生長(zhǎng)過(guò)程中起著關(guān)鍵作用稻沮,與更具侵襲性的疾病和預(yù)后不良相關(guān)纯亲。這些特點(diǎn)使得TROP-2成為了抗癌藥物開發(fā)的潛力靶點(diǎn)之一。
蘆康沙妥珠單抗(注射用SKB264)是科倫博泰與默沙東(MSD)聯(lián)合開發(fā)一款靶向TROP2的ADC谅沛。該產(chǎn)品已經(jīng)先后4次被CDE納入突破性治療品種羞遭,分別針對(duì):局部晚期或轉(zhuǎn)移性三陰乳腺癌、局部晚期或轉(zhuǎn)移性EGFR突變非小細(xì)胞肺癌策坏、局部晚期或轉(zhuǎn)移性HR陽(yáng)性/HER2陰性乳腺癌零反、PD-L1陰性三陰性乳腺癌。2023年11月烈肉,該藥的上市申請(qǐng)被CDE納入優(yōu)先審評(píng),用于既往至少接受過(guò)2種系統(tǒng)治療的不可切除的局部晚期或轉(zhuǎn)移性三陰性乳腺癌成人患者委丈。
本次該產(chǎn)品再次被CDE擬納入優(yōu)先審評(píng)甩高,針對(duì)EGFR突變非小細(xì)胞肺癌(NSCLC)成人患者。2023年6月什偷,科倫博泰宣布在美國(guó)臨床腫瘤學(xué)會(huì)(ASCO)年會(huì)以壁報(bào)形式公布了蘆康沙妥珠單抗用于經(jīng)治的局部晚期或轉(zhuǎn)移性NSCLC患者的2期拓展研究數(shù)據(jù)霸督。研究人員認(rèn)為,在經(jīng)過(guò)多線治療的NSCLC患者衅疙,尤其是EGFR突變患者莲趣,蘆康沙妥珠單抗展示出令人鼓舞的、可持續(xù)的抗腫瘤活性和可控的安全性饱溢,主要不良反應(yīng)是臨床常見的血液學(xué)毒性喧伞。
該2期拓展研究入組43例經(jīng)過(guò)多線治療的局部晚期或轉(zhuǎn)移性NSCLC患者,接受SKB264單藥治療(5mg/kg, Q2W)绩郎。數(shù)據(jù)截至2023年2月9日潘鲫,中位隨訪時(shí)間為11.5個(gè)月。其中22例為EGFR突變患者肋杖,21例為EGFR野生型患者溉仑。76.7%的患者既往接受過(guò)針對(duì)轉(zhuǎn)移性疾病的2種及以上方案治療挖函。在EGFR突變患者中,所有患者均為EGFR-TKI耐藥浊竟,50%的患者至少接受過(guò)一種化療方案怨喘,59.1%的患者接受過(guò)第三代EGFR-TKI治療。
數(shù)據(jù)顯示振定,39例患者療效可評(píng)估哲思,客觀緩解率(ORR)為43.6%(17/39),DCR為94.9%(37/39)蔓酣,中位持續(xù)緩解時(shí)間(mDoR)為9.3個(gè)月柴羞,6個(gè)月DoR率為77%。中位總生存期(mOS)尚未達(dá)到载甸,12個(gè)月OS率為70.6%稳嘁。
EGFR突變患者,ORR為60%(12/20)齐犀,DCR為100%(20/20)托习,mDoR為9.3個(gè)月,中位無(wú)進(jìn)展生存期(mPFS)為11.1個(gè)月滥捣,12個(gè)月OS率為80.7%虏淋。這也正是本次擬納入優(yōu)先審評(píng)的適應(yīng)癥。
EGFR野生型患者沦昆,ORR為26.3%(5/19)尸查,DCR為89.5%(17/19),mDoR為9.6個(gè)月愿凶,12個(gè)月OS率為60.6%竖伯。
目前,蘆康沙妥珠單抗針對(duì)局部晚期或轉(zhuǎn)移性EGFR突變NSCLC的3期臨床試驗(yàn)(SKB264-Ⅲ-09研究)正在開展因宇。這是一項(xiàng)比較SKB264單藥對(duì)比培美曲塞聯(lián)合鉑類治療EGFR-TKI治療失敗的EGFR突變的局部晚期或轉(zhuǎn)移性NSCLC的有效性和安全性的隨機(jī)七婴、開放性、多中心3期臨床研究察滑。計(jì)劃入組356例患者打厘,主要研究終點(diǎn)為IRC評(píng)估的無(wú)進(jìn)展生存期(PFS)。中國(guó)牽頭研究中心為中山大學(xué)腫瘤防治中心贺辰,計(jì)劃在42家中心進(jìn)行户盯。根據(jù)中國(guó)藥物臨床試驗(yàn)登記與信息公示平臺(tái)官網(wǎng),該研究目前正在招募患者魂爪。
本次蘆康沙妥珠單抗針對(duì)該適應(yīng)癥被擬納入優(yōu)先審評(píng)先舷,意味著該產(chǎn)品有望加速來(lái)到患者身邊
參考資料:
[1] 中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心官網(wǎng). Retrieved Aug 14, 2024, from https://www.cde.org.cn/main/xxgk/listpage/da6efd086c099b7fc949121166f0130c
[2]2023ASCO速遞 | 創(chuàng)新突破,科倫博泰SKB264(TROP2-ADC) NSCLC Ⅱ期詳細(xì)數(shù)據(jù)發(fā)布. Retrieved Jun 5, 2023, from https://mp.weixin.qq.com/s/qwuE5rcZBJshVijGvK99ZA

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽