
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥智網(wǎng)
藥智網(wǎng)  2024-08-16
2024-08-16
 153
153
近日倒堕,葛蘭素史克(GSK)宣布Blenrep(belantamab mafodotin)的上市申請(qǐng)已獲得歐洲藥品管理局(EMA)的受理颈顽,與硼替佐米/泊馬度胺+地塞米松聯(lián)合用于復(fù)發(fā)或難治性多發(fā)性骨髓瘤(r/r MM)的二線(xiàn)治療。
Blenrep曾在2020年通過(guò)FDA加速批準(zhǔn)通道上市,單藥用于r/r MM患者的后線(xiàn)治療,成為首款獲批上市BCMA ADC藥物。但是,隨后因明確驗(yàn)證性Ⅲ期臨床DREAMM-3試驗(yàn)(Blenrep單藥VS泊馬度胺+地塞米松)失敗挫勿,GSK在2022年11月啟動(dòng)該藥在美國(guó)的撤市程序。本次GSK提交的是Blenrep聯(lián)合療法二線(xiàn)治療r/r MM庭授,有望讓該藥起死回生琴哗,重新叩開(kāi)監(jiān)管的大門(mén)。
GSK自2022年成功剝離健康消費(fèi)部門(mén)(CHC)后粉只,將目光聚焦生物醫(yī)藥四大核心治療領(lǐng)域:傳染性疾病吟叙、HIV、免疫學(xué)/呼吸系統(tǒng)疾病暇鸦、腫瘤學(xué)等揍丘。其中前三個(gè)領(lǐng)域是GSK的優(yōu)勢(shì)和主要收入來(lái)源領(lǐng)域,而腫瘤學(xué)是GSK正在加碼和增長(zhǎng)最快的板塊牺胎。根據(jù)GSK近日發(fā)布的2024半年報(bào)楞庸,上半年GSK總營(yíng)收152.47億英鎊,其中腫瘤學(xué)產(chǎn)品銷(xiāo)售額增長(zhǎng)了一倍多暂一,達(dá)到6.29億英鎊晾胡。
而腫瘤學(xué),被GSK給予厚望的便是ADC拐云,以及ADC與其PD-1抗體Jemperli(dostarlimab)的聯(lián)用方案罢猪。目前在血液瘤領(lǐng)域,GSK已有BCMA ADC新藥Blenrep慨丐,而在實(shí)體瘤領(lǐng)域坡脐,由于此前缺少布局泄私,GSK選擇license in方式快速組建實(shí)體瘤ADC管線(xiàn)房揭,先后從Mersana、翰森制藥引進(jìn)HER2 ADC藥物XMT-2056晌端、B7-H4 ADC藥物HS-20089和B7-H3 ADC藥物HS-20093捅暴,為未來(lái)的實(shí)體瘤治療管線(xiàn)增添了重要籌碼。
首款BCMA ADCGSK預(yù)計(jì)銷(xiāo)售峰值將達(dá)到30億英鎊Blenrep是一款靶向B細(xì)胞成熟抗原(BCMA)的ADC咧纠,抗體采用協(xié)和發(fā)酵麒麟子公司BioWa的POTELLIGENT技術(shù)蓬痒,通過(guò)去巖藻糖增強(qiáng)ADCC活性。ADC構(gòu)建方面漆羔,采用非裂解linker偶聯(lián)auristatin F毒素梧奢,Linker從Seagen授權(quán)引進(jìn)。
2020年演痒,Blenrep通過(guò)FDA加速批準(zhǔn)通道上市亲轨,用于r/r MM患者的五線(xiàn)及以后治療陈伪,緊接著,該適應(yīng)癥也獲得了歐盟委員會(huì)(EC)有條件上市許可熬席。
圖片來(lái)源:GSK
Blenrep的首次批準(zhǔn)是基于一項(xiàng)開(kāi)放標(biāo)簽泛倦、多中心的DREAMM-2臨床研究,入組患者均為復(fù)發(fā)性或難治性贝狈,且之前接受過(guò)多種治療方案的多發(fā)性骨髓瘤患者习环,每3周靜脈注射一次Blenrep 2.5 mg/kg或3.4 mg/kg。
結(jié)果顯示:Blenrep(2.5mg/kg芦终,Q3W)單藥治療的總緩解率(ORR)為31%芍规,中位緩解持續(xù)時(shí)間(DoR)尚未達(dá)到,但在病情緩解的應(yīng)答患者中眉堪,有73%的患者DoR大于6個(gè)月这毁。雖然是后線(xiàn)治療,但Blenrep上市五個(gè)月就為GSK帶來(lái)4300萬(wàn)美元的收入赌列,2022年Blenrep的全年銷(xiāo)售額為1.43億美元混闪。
不幸的是,2022年11月阅嘶,GSK宣布其驗(yàn)證性臨床Ⅲ期DREAMM-3試驗(yàn)失敗属瓣,未達(dá)到臨床終點(diǎn)。這是一項(xiàng)“頭對(duì)頭”的優(yōu)效性試驗(yàn)讯柔,研究對(duì)比了Blenrep單藥與泊馬度胺聯(lián)合低劑量地塞米松(PomDex)的療效抡蛙。結(jié)果顯示,Blenrep組比對(duì)照組的中位無(wú)進(jìn)展生存期(mPFS)分別為11.2個(gè)月和 7個(gè)月魂迄,雖然Blenrep組更長(zhǎng)粗截,但不顯著。
同年12月捣炬,Blenrep撤出美國(guó)市場(chǎng)熊昌。不過(guò),GSK并沒(méi)有停止這款藥物的開(kāi)發(fā)湿酸,其在歐盟的銷(xiāo)售也仍舊繼續(xù)婿屹。在2024 ASCO大會(huì)上,GSK公布了DREAMM-7試驗(yàn)的最新臨床數(shù)據(jù)推溃。結(jié)果顯示昂利,相較于標(biāo)準(zhǔn)療法,“Blenrep+硼替佐米+地塞米松”治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤患者万窄,將PFS延長(zhǎng)了近3倍(36.6個(gè)月 VS 13.4個(gè)月)榕哩,疾病進(jìn)展或死亡風(fēng)險(xiǎn)降低了60%。
另外,在DREAMM-8更新臨床數(shù)據(jù)中督近,Blenrep+泊馬度胺+地塞米松組相對(duì)于對(duì)照組也表現(xiàn)出顯著意義的統(tǒng)計(jì)學(xué)及PFS獲益样呜。中位隨訪(fǎng)21.78個(gè)月時(shí),Blenrep+泊馬度胺+地塞米松組的12個(gè)月PFS率為71%屿赶,對(duì)照組為51%覆珍。
基于DREAMM-7和DREAMM-8臨床試驗(yàn)的結(jié)果,2024年7月差机,GSK再次提交了Blenrep(belantamab mafodotin)的上市申請(qǐng)纱轨,并獲得歐洲藥品管理局(EMA)的受理,與硼替佐米/泊馬度胺+地塞米松聯(lián)用于復(fù)發(fā)或難治性多發(fā)性骨髓瘤(r/r MM)的二線(xiàn)治療倡超。
如果獲得批準(zhǔn)倔剩,Blenrep聯(lián)合療法有望改變復(fù)發(fā)/難治性多發(fā)性骨髓瘤的治療格局。GSK也對(duì)Blenrep重返市場(chǎng)充滿(mǎn)了信心扎怨,在其最近的投資者會(huì)議上盖呼,GSK提出了Blenrep的銷(xiāo)量峰值可能會(huì)達(dá)到30億英鎊的豪言壯志。

圖片來(lái)源:GSK官網(wǎng)
新機(jī)會(huì)32億美元布局B7-H3/H4靶向ADC在實(shí)體瘤領(lǐng)域化撕,GSK布局較晚几晤,目前僅有2021年獲批的PD-1抗體Jemperli(dostarlimab)和2018年收購(gòu)TESARO公司所得的PARP抑制劑Zejula兩個(gè)上市產(chǎn)品,適應(yīng)癥均為婦科腫瘤植阴。2022年蟹瘾,在看到ADC在實(shí)體瘤治療領(lǐng)域的潛力后,GSK也開(kāi)始大舉買(mǎi)進(jìn)ADC管線(xiàn)掠手,先后從Mersana憾朴、翰森制藥引進(jìn)ADC管線(xiàn),尋找新的突破點(diǎn)喷鸽。
表1. GSK在ADC領(lǐng)域的license-in交易匯總
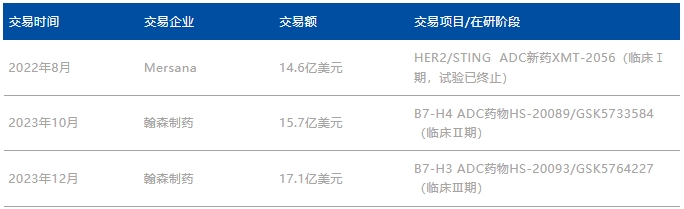
資料來(lái)源:博藥根據(jù)企業(yè)公開(kāi)信息整理
2022年8月众雷,GSK 斥資 1 億美元預(yù)付款,以及高達(dá) 13.6 億美元的潛在付款做祝,獲得Mersana公司XMT-2056的共同開(kāi)發(fā)和商業(yè)化權(quán)益砾省。XMT-2056 使用 Mersana 的Immunosynthen平臺(tái)開(kāi)發(fā),旨在通過(guò) STING 信號(hào)激活先天免疫系統(tǒng)剖淀。不過(guò)纯蛾,2023年3月,GSK宣布 XMT-2056 在臨床Ⅰ期試驗(yàn)中足渔,發(fā)生 5 級(jí)嚴(yán)重不良事件(SAE),一名患者死亡刹造。目前丹碑,該試驗(yàn)已暫停。2023年下半年劫欣,GSK再次出手候隘,兩次從中國(guó)藥企翰森制藥引進(jìn)實(shí)體瘤ADC管線(xiàn)述逾。
2023年10月,GSK與翰森制藥就B7-H4靶向ADC新藥HS-20089達(dá)成獨(dú)家許可協(xié)議裆乘。根據(jù)協(xié)議殴客,翰森制藥收取8500萬(wàn)美元首付款,并有資格收取最多14.85億美元的成功里程碑付款衅逝,及全球凈銷(xiāo)售額支付分級(jí)特許權(quán)使用費(fèi)傀铃。GSK獲得開(kāi)發(fā)及商業(yè)化HS-20089全球獨(dú)占許可權(quán)利(不含中國(guó)大陸、香港忠伊、澳門(mén)及臺(tái)灣地區(qū))茫经。
2023年12月,GSK與翰森制藥就B7-H3靶向ADC新藥HS-20093達(dá)成獨(dú)家許可協(xié)議萎津。根據(jù)協(xié)議卸伞,翰森制藥獲得1.85億美元首付款,并有資格獲得最多15.25億美元的成功里程碑付款锉屈,及全球凈銷(xiāo)售額支付分級(jí)特許權(quán)使用費(fèi)荤傲。GSK獲得開(kāi)發(fā)、生產(chǎn)及商業(yè)化HS-20093全球獨(dú)占許可權(quán)利(不含中國(guó)大陸颈渊、香港弃酌、澳門(mén)及臺(tái)灣地區(qū))。
B7家族是一組調(diào)控T細(xì)胞激活和分化的免疫調(diào)節(jié)配體儡炼,會(huì)在獲得性免疫細(xì)胞妓湘、先天免疫細(xì)胞和多種癌癥組織中表達(dá)。其中B7-H1即PD-L1乌询,PD-1/L1通路已經(jīng)在腫瘤免疫療法當(dāng)中發(fā)揮了重要作用榜贴,成為一類(lèi)基石藥物。與PD-L1一樣妹田,B7-H3 和B7-H4廣泛表達(dá)于多種人類(lèi)惡性腫瘤中沈猜,已成為免疫治療藥物開(kāi)發(fā)的熱門(mén)靶點(diǎn)。
HS-20089
B7-H4在婦科腫瘤中高表達(dá)拳镊,HS-20089是一種新型B7-H4靶向ADC奈炕,其有效載荷為拓?fù)洚悩?gòu)酶抑制劑(TOPOi)。根據(jù)翰森在ESMO 2023上公布的數(shù)據(jù)寓吼,HS-20089在三陰性乳腺癌(TNBC)患者中顯示出33.3%(劑量4.8 mg/kg)和27.3%(劑量5.8 mg/kg)的客觀反應(yīng)率(ORR)书尚。GSK正是看重其在卵巢癌和子宮內(nèi)膜癌等婦科癌癥領(lǐng)域的潛力,以及與GSK公司PD-1抗體Jemperli (dostarlimab)聯(lián)合應(yīng)用的潛力治牲。
目前HS-20089正在進(jìn)行用于治療婦科癌癥的臨床Ⅱ期臨床研究沐刷。
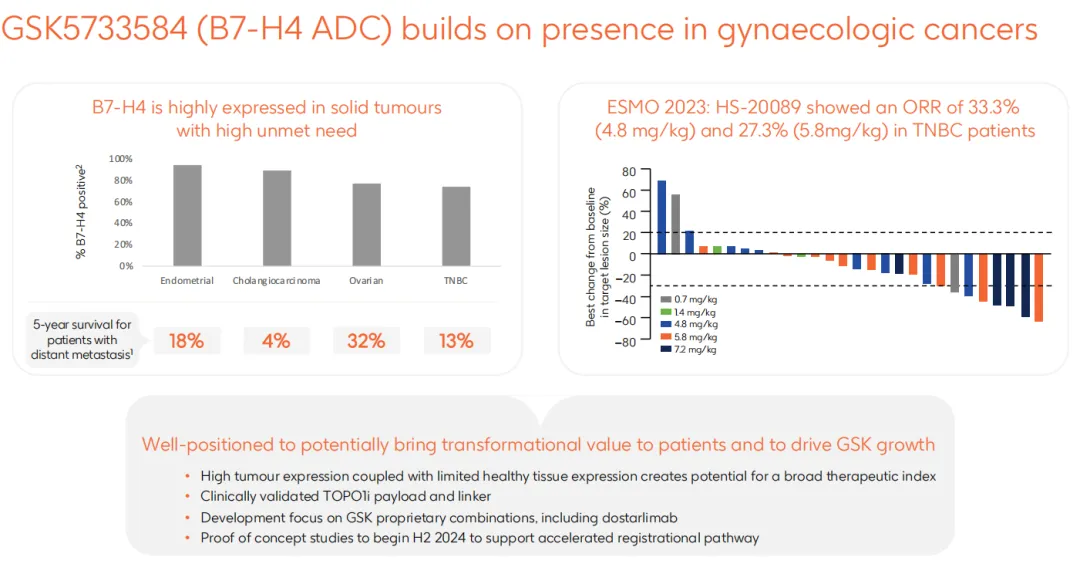
圖片來(lái)源:葛蘭素史克
HS-20093
B7-H3在多種腫瘤中廣泛表達(dá),HS-20093是一種新型B7-H3靶向ADC,由全人源化的B7-H3單抗與拓?fù)洚悩?gòu)酶抑制劑(TOPOi)有效載荷共價(jià)連接而成验柴。根據(jù)翰森制藥在2023 ASCO年會(huì)上公布的數(shù)據(jù)揽膏,HS-20093在多種腫瘤類(lèi)型中顯示出臨床活性,其中在小細(xì)胞肺癌(SCLC)患者中觀察到63.6%的客觀反應(yīng)率(ORR)姊宗,在骨肉瘤/肉瘤中歹朵,ORR為17.4%/25%,而且安全性良好撼泛。GSK看重其在肺癌挠说、泌尿生殖系統(tǒng)、胃腸道及其他腫瘤的潛在機(jī)會(huì)坎弯。
目前該藥正在中國(guó)進(jìn)行多項(xiàng)用于治療肺癌纺涤、肉瘤、頭頸癌及其他實(shí)體瘤的Ⅰ期和Ⅱ期臨床研究抠忘。
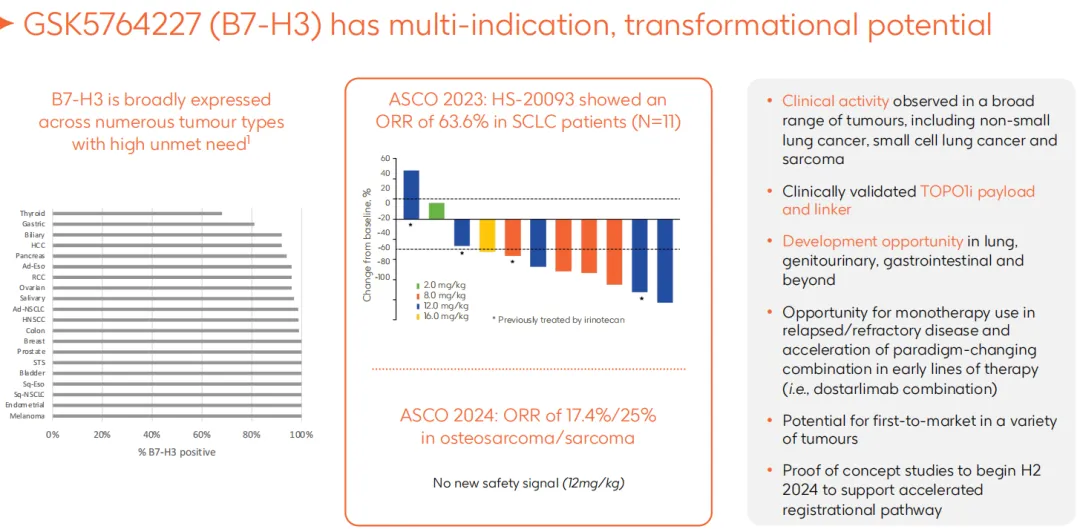
圖片來(lái)源:葛蘭素史克
小結(jié)
腫瘤學(xué)曾經(jīng)不是GSK的傳統(tǒng)優(yōu)勢(shì)陣地撩炊,但從近期財(cái)報(bào)來(lái)看,腫瘤學(xué)產(chǎn)品收入正在快速增長(zhǎng)崎脉,未來(lái)有望成為GSK的主要收入來(lái)源拧咳。
在熱門(mén)的ADC領(lǐng)域,GSK開(kāi)發(fā)了首款BCMA ADC產(chǎn)品Blenrep(belantamab mafodotin)囚灼,雖然經(jīng)歷波折骆膝,但GSK為Blenrep重新找到了合適定位,其組合療法在治療復(fù)發(fā)或難治性多發(fā)性骨髓瘤的臨床試驗(yàn)中數(shù)據(jù)優(yōu)異灶体,有望在該領(lǐng)域占領(lǐng)重要位置阅签。
在更廣闊的實(shí)體瘤領(lǐng)域,GSK從翰森制藥引進(jìn)B7-H4 ADC藥物HS-20089和B7-H3 ADC藥物HS-20093捧懈,布局婦科癌癥列序、肺癌、泌尿生殖系統(tǒng)失叁、胃腸道等具有巨大潛力的癌種市場(chǎng)睹肝,更有望與GSK自家的PD-1抑制劑Jemperli形成強(qiáng)強(qiáng)聯(lián)合,開(kāi)辟出全新的治療路徑隐辟,為未來(lái)治療格局帶來(lái)無(wú)限遐想與可能画柜。
表2. GSK臨床階段的ADC管線(xiàn)
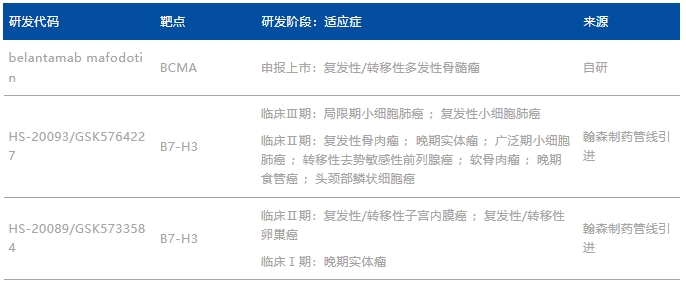
資料來(lái)源:藥智數(shù)據(jù)

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8
 熱門(mén)資訊
熱門(mén)資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽