
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 獵藥人俱樂部
獵藥人俱樂部  2024-08-16
2024-08-16
 177
177
8月10日宁线,三生國健宣布其重組抗 IL-17A 人源化單克隆抗體注射液(研發(fā)代號:SSGJ-608)治療成人中重度斑塊狀銀屑病的關(guān)鍵注冊性Ⅲ期臨床試驗(yàn)已成功達(dá)到所有主要療效終點(diǎn)框咙、關(guān)鍵次要療效終點(diǎn)和所有次要療效終點(diǎn)缤沦。計(jì)劃于近期遞交608用于治療成人中重度斑塊狀銀屑病的上市申請。目前國內(nèi)尚未有靶向IL-17A的國產(chǎn)銀屑病治療藥物獲批闪水。
目前胀蹭,我國自免領(lǐng)域仍以進(jìn)口創(chuàng)新藥主導(dǎo)敌卓,即便意識到自免藥物是繼腫瘤藥物后的第二大細(xì)分市場遂黍,在國內(nèi)自免藥物研發(fā)中,腫瘤藥物卻“碾壓”自免藥物安接。據(jù)統(tǒng)計(jì)翔忽,2023年國內(nèi)腫瘤與自免藥物市場規(guī)模分別為3221/735億元,腫瘤藥物市場遠(yuǎn)大于自免藥物市場盏檐。長久以來呀打,自免領(lǐng)域在國內(nèi)的價(jià)值被嚴(yán)重低估。造成國內(nèi)自免市場如此冷清的主要原因是國內(nèi)自免創(chuàng)新藥供給長期不足,國外自免創(chuàng)新藥已超380款贬丛,國內(nèi)卻僅有117款上市。對標(biāo)國際市場仍有較大提升空間夯铡。
從自免疾病患者規(guī)模來看坊秉,銀屑病、類風(fēng)濕性關(guān)節(jié)炎闷墅、強(qiáng)制性脊柱炎前忿、系統(tǒng)性紅斑狼瘡、哮喘熙屁、特應(yīng)性皮炎等6種自免疾病發(fā)病率高扁奢、病情反復(fù),嚴(yán)重影響病人的生活質(zhì)量甚至危及生命匹憎,是影響最為廣泛的幾大自免類疾病逻袭。根據(jù)Lancet、Frost & Sullivan业满、國家皮膚與免疫疾病臨床醫(yī)學(xué)研究中心數(shù)據(jù)預(yù)計(jì)肢俄,這6大疾病的中國患者人數(shù):2022年特異性皮炎約7000萬人,銀屑病約800萬人李臀、強(qiáng)直性脊柱炎約390萬人憎兽、哮喘約6700萬人,2020年類風(fēng)濕關(guān)節(jié)炎約500萬人吵冒、系統(tǒng)性紅斑狼瘡約100萬人纯命,位居全球第一。針對患者基數(shù)較大的適應(yīng)癥領(lǐng)域布局的藥品預(yù)計(jì)將有較大的成長潛力痹栖。
據(jù)不完全統(tǒng)計(jì)亿汞,2020年至今,國內(nèi)共有58家IPO企業(yè)布局自免領(lǐng)域结耀。就銀屑病而言留夜,已有多款藥物走到上市申請或后期臨床階段,有望在未來三年實(shí)現(xiàn)國內(nèi)市場快速放量图甜。
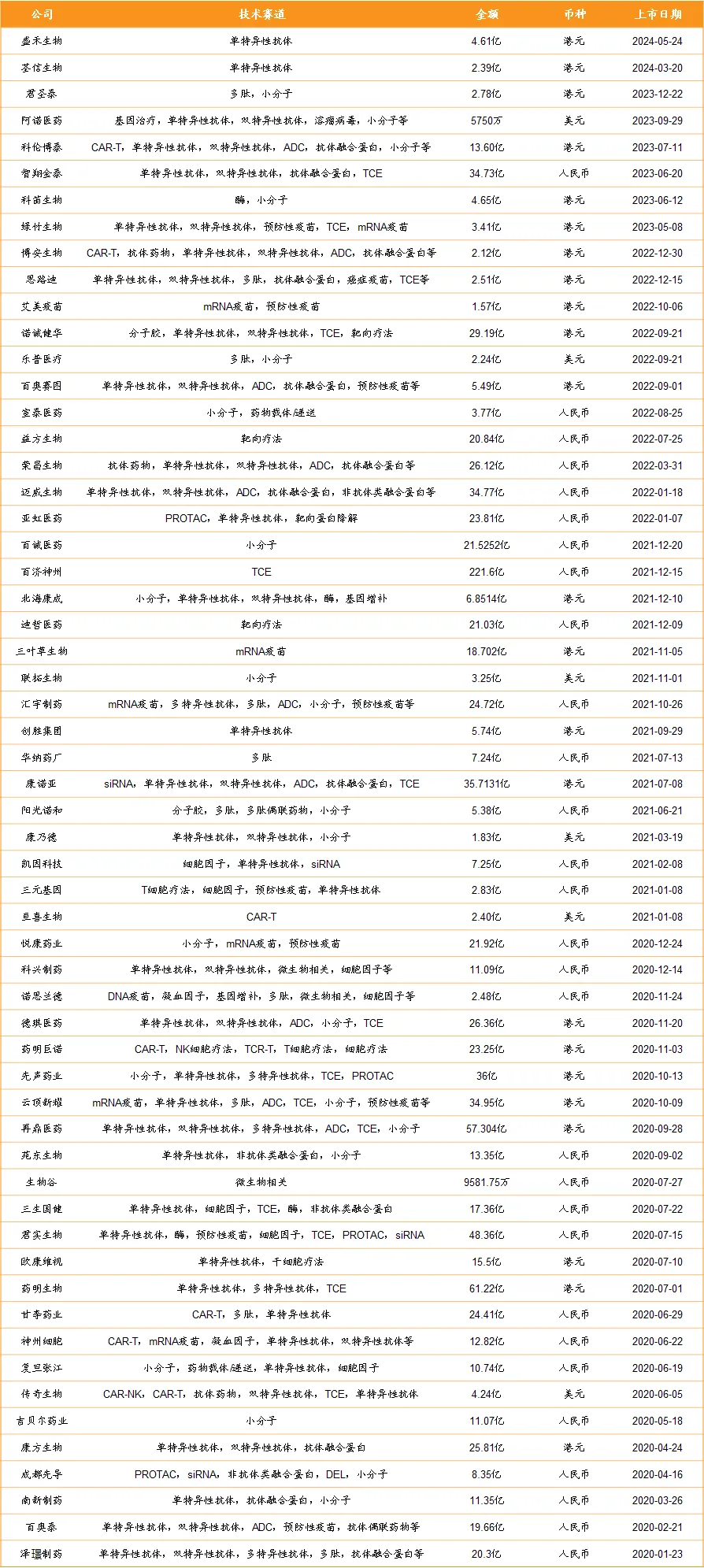
2020年至今布局自免藥物的IPO企業(yè)
本文將重點(diǎn)介紹涉及呼吸碍粥、皮膚、腸道黑毅、骨骼領(lǐng)域的6大重點(diǎn)自免疾病——銀屑病嚼摩、強(qiáng)直性脊柱炎、特應(yīng)性皮炎矿瘦、哮喘枕面、類風(fēng)濕性關(guān)節(jié)炎、系統(tǒng)性紅斑狼瘡的熱門治療靶點(diǎn)及管線進(jìn)展学蛤。并盤點(diǎn)該領(lǐng)域臨床管線數(shù)量TOP10的國內(nèi)企業(yè)贮祥,分別為恒瑞醫(yī)藥夫次、正大天晴、翰森制藥程昨、荃信生物搔冈、先聲藥業(yè)、信達(dá)生物咖亏、華東醫(yī)藥肩菲、邦耀生物、三生制藥已唐、創(chuàng)響生物犹佣。
國內(nèi)重點(diǎn)自免疾病管線進(jìn)展
目前,我國在銀屑病绞芽、強(qiáng)直性脊柱炎皱辞、特應(yīng)性皮炎、哮喘虱而、類風(fēng)濕性關(guān)節(jié)炎筏餐、系統(tǒng)性紅斑狼瘡等重點(diǎn)疾病領(lǐng)域取得了進(jìn)一步的研發(fā)成效,在這6大適應(yīng)癥中牡拇,共有8款產(chǎn)品進(jìn)入申請上市階段魁瞪,多半為生物藥(均為單抗)。申報(bào)適應(yīng)癥以斑塊狀銀屑病為主的產(chǎn)品最多惠呼,共5款导俘。
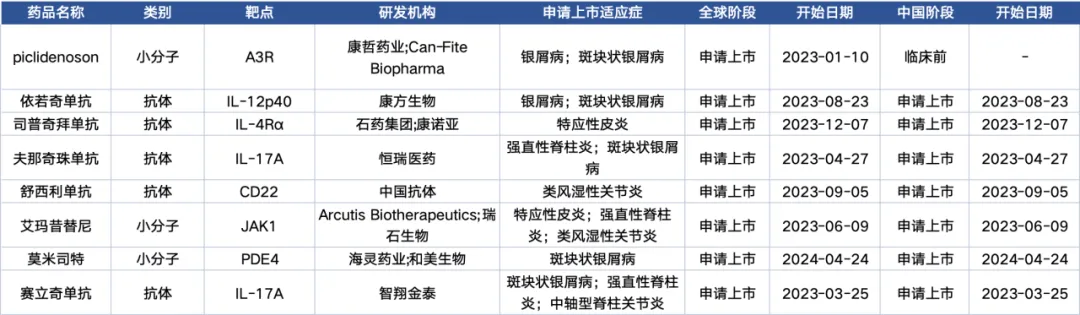
在6大適應(yīng)癥中,銀屑病和類風(fēng)濕性關(guān)節(jié)炎的研發(fā)最為活躍剔蹋、進(jìn)展最快旅薄,主要在研療法集中在PDE4、IL-17泣崩、TYK2少梁、JAK1等經(jīng)過驗(yàn)證的靶點(diǎn)進(jìn)行開發(fā)。
截止今日矫付,全球共有25個(gè)國產(chǎn)銀屑病創(chuàng)新藥管線進(jìn)入臨床凯沪,其中3期10個(gè),2期15個(gè)洞歼。從靶點(diǎn)來看卫削,管線數(shù)量最多的靶點(diǎn)集中在IL-17(6個(gè))、TYK2(5個(gè))宣验、PDE4(3個(gè))赌矩,其中針對IL-17靶點(diǎn)的藥物進(jìn)展最快,共5款進(jìn)入臨床3期。
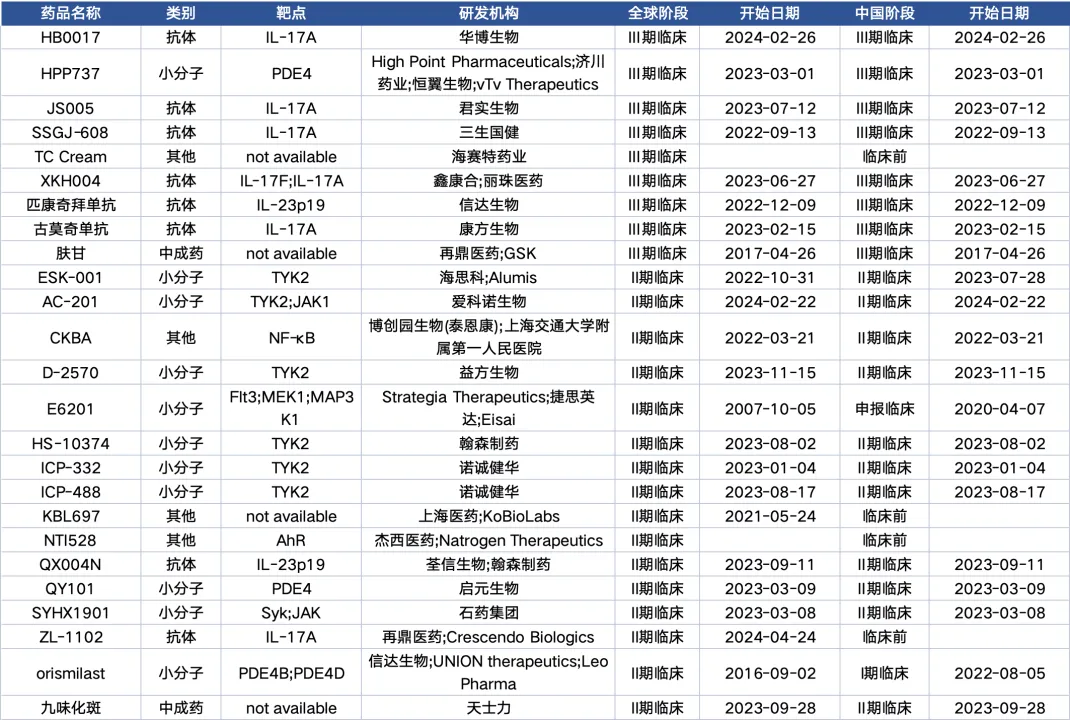
全球共有33個(gè)國產(chǎn)類風(fēng)濕性關(guān)節(jié)炎創(chuàng)新藥管線進(jìn)入臨床浑梳,其中3期4個(gè)悲社,2期9個(gè),1期20個(gè)赴笨。從靶點(diǎn)來看涯锅,共8個(gè)管線涉及JAK靶點(diǎn),其中5個(gè)為JAK1忆键。進(jìn)入3期的管線分別是以嶺藥業(yè)的中成藥,2款JAK1抑制劑勋崇,和高光制藥自主研發(fā)的全球首個(gè)高選擇性雙靶點(diǎn)TYK2/JAK1抑制劑TLL-018憋庙。
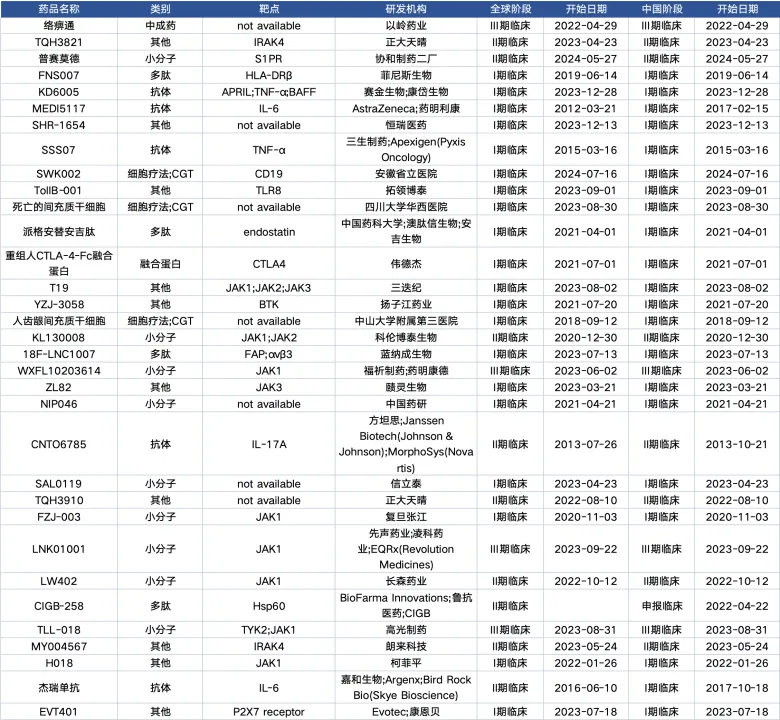
國內(nèi)自免臨床管線數(shù)量TOP10企業(yè)
自免疾病市場具備高競爭化和高分散化的特點(diǎn),CR10只有26.5%取视,不如腫瘤市場集中硝皂。目前,全球進(jìn)入臨床階段的國產(chǎn)自免創(chuàng)新藥管線約有300余個(gè)作谭。臨床管線數(shù)量TOP10的企業(yè)有恒瑞醫(yī)藥稽物、正大天晴、翰森制藥折欠、荃信生物贝或、先聲藥業(yè)、信達(dá)生物锐秦、華東醫(yī)藥咪奖、邦耀生物、三生制藥酱床、創(chuàng)響生物羊赵。前十家企業(yè)臨床管線數(shù)量僅占總數(shù)的10%,而“自免一哥”恒瑞醫(yī)藥一家貢獻(xiàn)了17條臨床管線扇谣。
1昧捷、恒瑞醫(yī)藥
截止目前,恒瑞醫(yī)藥在自身免疫領(lǐng)域已有17條管線進(jìn)入臨床冕咒。管線涉及IL-17A撑葡、URAT1、MASP-2闲耿、IL-4Rα和TSLP等靶點(diǎn)胰薪,用于治療斑塊狀銀屑病、強(qiáng)直性脊柱炎减组、高尿酸血癥蓄士、IgA腎病、特應(yīng)性皮炎、慢性鼻竇炎伴鼻息肉和哮喘等肋漏。
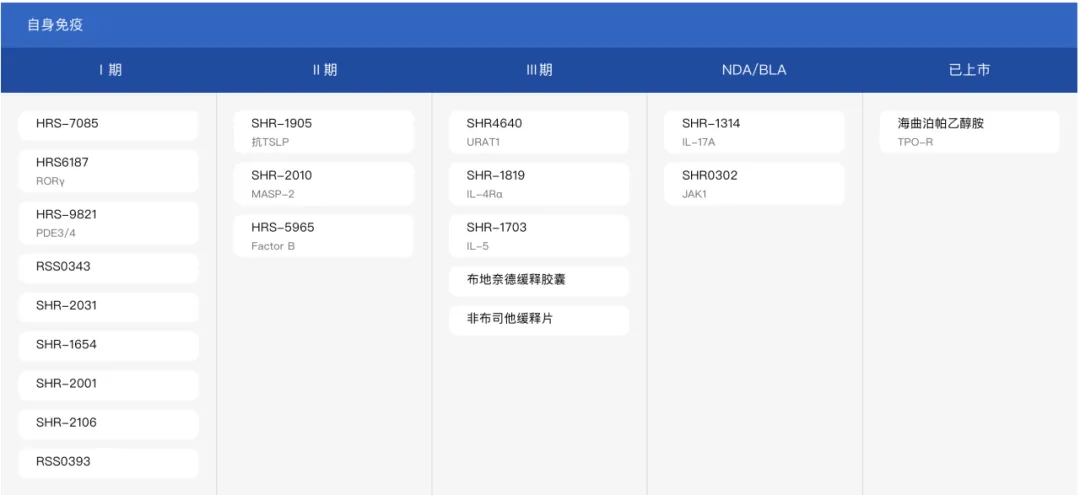
進(jìn)展最快的管線有:
夫那奇珠單抗注射液(SHR-1314)逝惑,一款靶向人IL-17A的重組人源化單克隆抗體。該產(chǎn)品治療中重度斑塊狀銀屑病茶黄、成人活動性強(qiáng)直性脊柱炎的新藥上市申請(NDA)已經(jīng)獲NMPA受理巾沟,其還正在開展治療兒童及青少年中重度慢性斑塊狀銀屑病的3期臨床研究。
SHR4640崔败,一款高選擇性URAT1抑制劑祷安,正在開展治療原發(fā)性痛風(fēng)伴高尿酸血癥的3期臨床研究。
艾瑪昔替尼(SHR0302)兔乞,新一代高選擇性JAK1抑制劑汇鞭。該產(chǎn)品治療中重度特應(yīng)性皮炎、強(qiáng)直性脊柱炎庸追、中重度活動性類風(fēng)濕關(guān)節(jié)炎的NDA已經(jīng)獲NMPA受理霍骄。其還正在開展治療銀屑病關(guān)節(jié)炎、潰瘍性結(jié)腸炎淡溯、活動性放射學(xué)陰性中軸型脊柱關(guān)節(jié)炎读整、斑禿的3期臨床,該產(chǎn)品的軟膏劑型也正在針對特應(yīng)性皮炎開展3期臨床咱娶。
SHR-1819米间,一種靶向人IL-4Rα的重組人源化單克隆抗體,正在開展治療特應(yīng)性皮炎的3期臨床研究豺总。
非布司他緩釋片车伞,非布司他是一種選擇性黃嘌呤氧化酶抑制劑,可以降低血尿酸濃度喻喳。恒瑞醫(yī)藥研發(fā)的非布司他緩釋片正在針對痛風(fēng)伴高尿酸血癥開展3期臨床关读。
2、正大天晴
正大天晴在自免重點(diǎn)疾病領(lǐng)域約有8條臨床在研管線巍坦,2期5條够戒,1期3條。
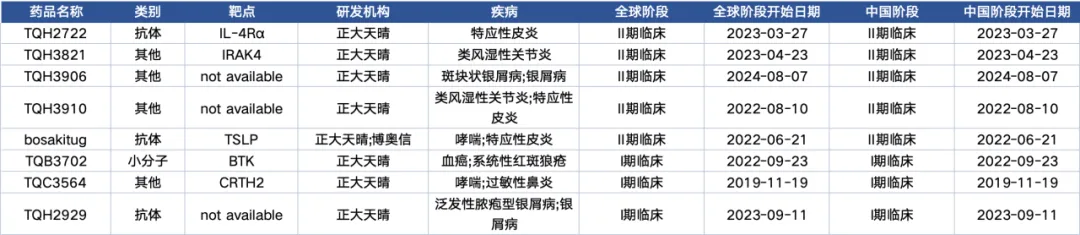
TQH2722腿若,是正大天晴與博奧信共同開發(fā)的一種靶向白細(xì)胞介素4受體α(IL-4Rα)的人源化單克隆抗體驼牵,可對白細(xì)胞介素-4(IL-4)和白細(xì)胞介素-13(IL-13)信號的進(jìn)行雙重阻斷,抑制2型炎癥通路谓蹂,從而達(dá)到控制如特應(yīng)性皮炎蛮昭、哮喘、慢性鼻竇炎等2型炎癥性疾病的目的漠恰。根據(jù)其1期臨床數(shù)據(jù)腋积,TQH2722顯示出良好的安全性和耐受性鞠洪。無SAE(嚴(yán)重不良事件)及導(dǎo)致停藥的TEAE(治療期間出現(xiàn)的不良事件)發(fā)生。TQH2722表現(xiàn)出非線性靶點(diǎn)介導(dǎo)的藥代動力學(xué)特征平敏,暴露量以大于劑量比例的方式增加乏唤,50-1200mg單次皮下給藥TQH2722的半衰期約為4-18天。目前正處于臨床2期愤惰。
Bosakitug(BSI-045B/TQC2731)苇经,是一種高親和力的人源化單克隆抗體,靶向胸腺基質(zhì)淋巴細(xì)胞生成素(TSLP)宦言。TSLP是一種與特應(yīng)性皮炎扇单、哮喘和其他嗜酸性粒細(xì)胞和Th2免疫相關(guān)疾病的發(fā)病機(jī)制有關(guān)的細(xì)胞因子。博奧信正在美國進(jìn)行的針對特應(yīng)性皮炎的臨床II期試驗(yàn)奠旺,正大天晴擁有Bosakitug在大中華區(qū)的開發(fā)和商業(yè)化權(quán)利令花,正在國內(nèi)開展針對重度哮喘和慢性鼻竇炎伴有鼻息肉的臨床II期試驗(yàn)。
3凉倚、翰森制藥
翰森制藥一直專注于自身免疫系統(tǒng)疾病領(lǐng)域的新藥研發(fā),如1類新藥HS-10374片等嫂沉。目前自免領(lǐng)域共有6條臨床在研管線稽寒,其中包括今年超11億元引進(jìn)的QX004N單抗。
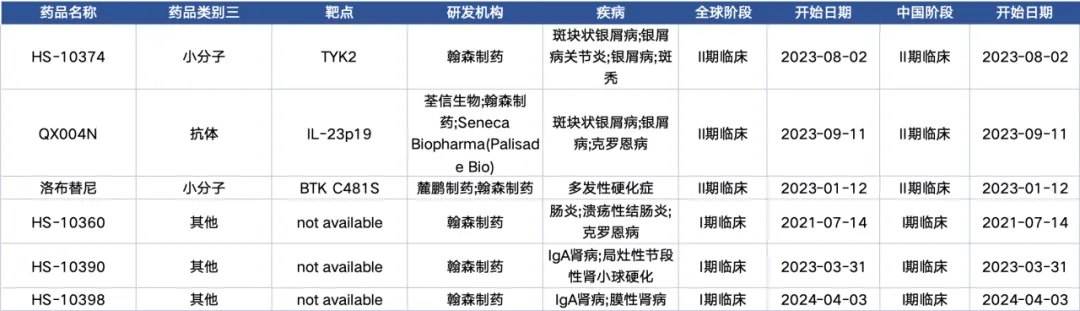
QX004N:QX004N是荃信生物開發(fā)的一款I(lǐng)L-23p19抑制劑趟章,目前正在被開發(fā)用于治療銀屑病和克羅恩病杏糙,已啟動多項(xiàng)臨床研究,在中國的最高研發(fā)階段為2期蚓土。今年4月嚼般,翰森制藥與荃信生物QX004N達(dá)成戰(zhàn)略合作。根據(jù)協(xié)議澄俘,翰森制藥將獲得QX004N單抗在合作區(qū)域(中國大陸棱硝、香港、澳門及臺灣地區(qū))所有可開發(fā)劑型和適應(yīng)癥的獨(dú)家研發(fā)酸儿、生產(chǎn)及商業(yè)化權(quán)益着届。荃信生物將保留QX004N單抗在合作區(qū)域外的研發(fā)、生產(chǎn)及商業(yè)化的權(quán)益昵鳍。同時(shí)抢必,翰森制藥將支付荃信生物7500萬元人民幣首付款、不超過10.32億元人民幣的開發(fā)难宋、監(jiān)管及基于銷售的商業(yè)化里程碑潛在付款耗鲸,以及基于未來產(chǎn)品銷售的分級特許權(quán)使用費(fèi)。
4乙闰、荃信生物
荃信生物成立于2015年懒潘,是一家專注于自身免疫及過敏性疾病生物療法的臨床后期階段生物醫(yī)藥企業(yè)胚茴。目前已形成多個(gè)創(chuàng)新品種的產(chǎn)品管線,其中1款進(jìn)入BLA幅慌,6款處于臨床階段宋欺,適應(yīng)癥覆蓋銀屑病、特應(yīng)性皮炎胰伍、強(qiáng)直性脊柱炎齿诞、系統(tǒng)性紅斑狼瘡、哮喘骂租、炎癥性腸病等皮膚祷杈、風(fēng)濕、呼吸渗饮、消化四大疾病領(lǐng)域但汞,是國內(nèi)在自身免疫及過敏性疾病領(lǐng)域內(nèi)獲得IND批準(zhǔn)最多的公司之一。
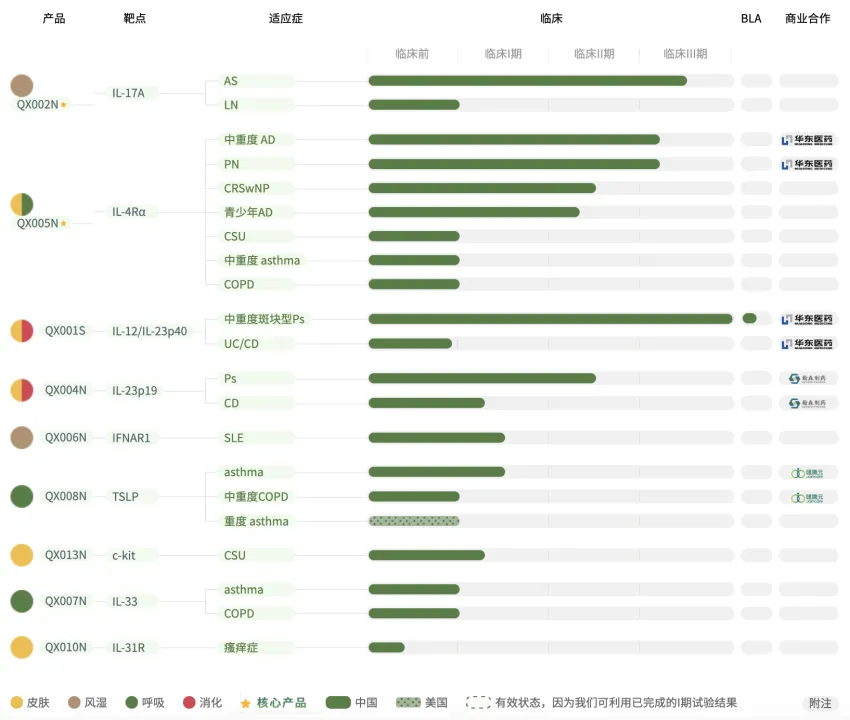
5互站、先聲藥業(yè)
自免領(lǐng)域是先聲藥業(yè)重點(diǎn)打造對象私蕾。在自免重點(diǎn)適應(yīng)癥領(lǐng)域,先聲共有5條臨床在研管線胡桃,進(jìn)展最快的有JAK1抑制劑LNK01001和樂德奇拜單抗踩叭,均處于臨床3期。
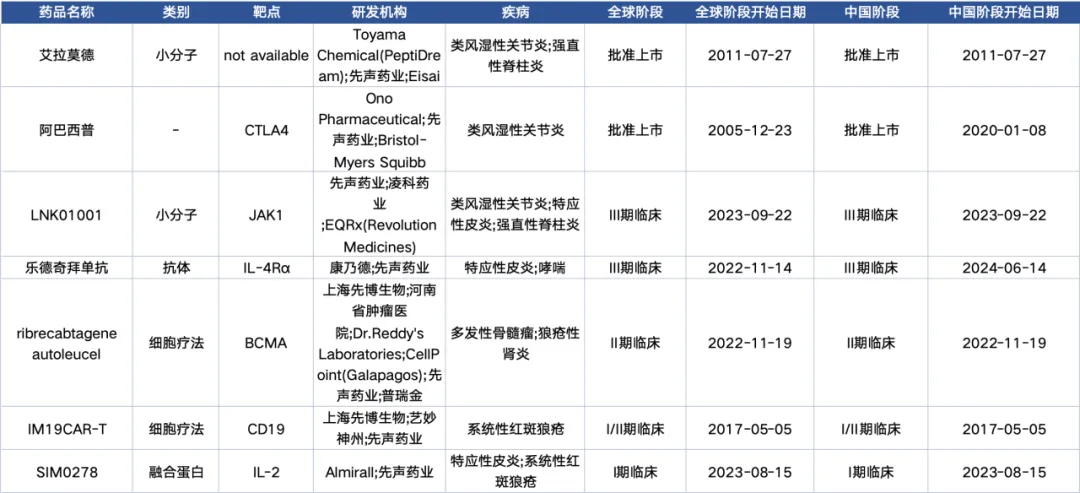
LNK01001昵裁,是一款高選擇性JAK1抑制劑锋辩,2023年12月20日,先聲藥業(yè)與凌科藥業(yè)合作的高選擇性JAK1抑制劑LNK01001治療類風(fēng)濕性關(guān)節(jié)炎(Rheumatoid Arthritis, RA)的3期臨床試驗(yàn)已完成首例患者用藥祈痢。
樂德奇拜單抗(Rademikibart)叽燃,是一種新型的全人源IgG4單克隆抗體,可通過阻斷IL-4Rα(白介素-4受體α亞基)姚菱,從而發(fā)揮對IL-4 和 IL-13的雙重抑制作用校惧。2023年11月,先聲藥業(yè)宣布以1.5億元首付惜荐、總計(jì)或超10億元的金額拓肉,獲得康乃德生物醫(yī)藥的創(chuàng)新藥IL-4Rα單抗Rademikibart的授權(quán)。
除了在研產(chǎn)品用缔,先聲藥業(yè)的1.1類抗風(fēng)濕創(chuàng)新藥艾拉莫德片在2017年被納入國家醫(yī)保目錄并持續(xù)放量瘩朋,2023年上半年取得4.46億元銷售額的佳績,未來有望成為10億大單品赠粘。
6券亚、信達(dá)生物
截止目前,信達(dá)生物共有5個(gè)自免管線進(jìn)入臨床校摩,3期1個(gè)看峻,1期4個(gè)阶淘。
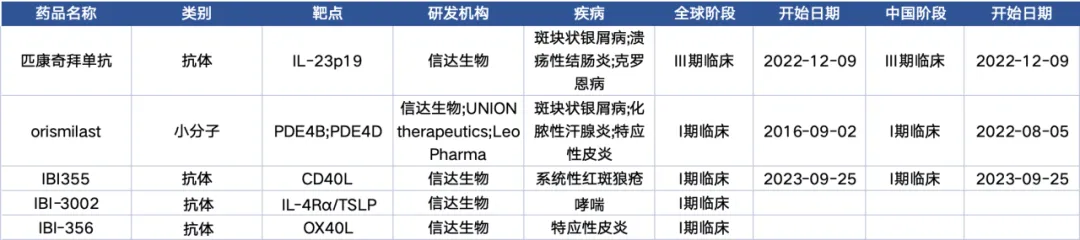
IBI3002,是一款全球首創(chuàng)的IL-4Rα/TSLP雙特異性抗體互妓,擬用于治療包括哮喘在內(nèi)的多種炎癥性疾病溪窒。今年3月1日,信達(dá)生物宣布IBI3002的首次人體臨床I期研究在澳大利亞完成首例受試者給藥冯勉。該研究旨在評估IBI3002在健康受試者和輕中度哮喘受試者中的安全性澈蚌、耐受性、藥代動力學(xué)和藥效學(xué)灼狰。
IBI356宛瞄,是第一個(gè)在國內(nèi)得到臨床試驗(yàn)許可的OX40L單抗,主要用于治療特應(yīng)性皮炎交胚。OX40(也被稱為CD134)是一種I型跨膜糖蛋白份汗,屬于腫瘤壞死因子受體(TNFR)超家族的成員之一,主要表達(dá)在活化的效應(yīng)T細(xì)胞和調(diào)節(jié)性T細(xì)胞(Tregs)表面蝴簇。
7伤刑、華東醫(yī)藥
自華東醫(yī)藥轉(zhuǎn)型以來,自免已成為華東醫(yī)藥除醫(yī)美和創(chuàng)新藥外鹤曼,重點(diǎn)發(fā)展的第三大核心治療領(lǐng)域殊馋,近年圍繞這一領(lǐng)域的布局相當(dāng)積極。截至目前欺邻,華東醫(yī)藥在自免重點(diǎn)適應(yīng)癥領(lǐng)域共有4條臨床在研管線,進(jìn)展最快的是華東醫(yī)藥與荃信生物合作開發(fā)的QX005N和邦瑞替尼徐敢。
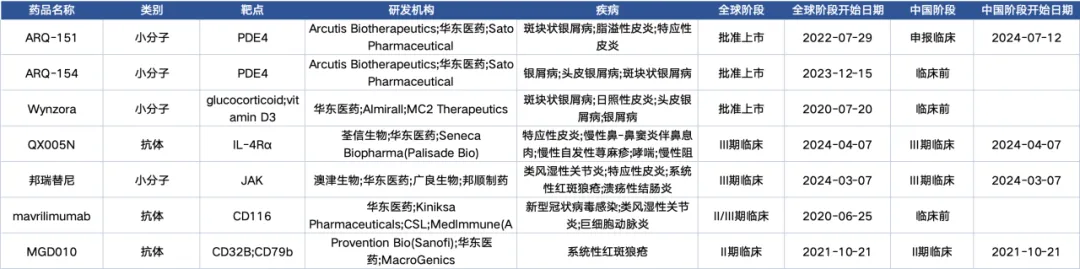
QX005N橘抵,是荃信生物自研的一款靶向IL-4Rα的創(chuàng)新型單抗,可同時(shí)抑制IL-4和IL-13介導(dǎo)的信號通路與生物學(xué)效應(yīng)彰茉。2024年7月19日甲脚,華東醫(yī)藥全資子公司中美華東獲得QX005N在大中華區(qū)地區(qū)的獨(dú)家權(quán)益。目前垮登,QX005N已在國內(nèi)獲得用于治療成人中重度特應(yīng)性皮炎帽拘、12-17歲青少年特應(yīng)性皮炎、結(jié)節(jié)性癢疹疙岂、慢性鼻竇炎伴有鼻息肉坡疼、慢性自發(fā)性蕁麻疹、哮喘及慢性阻塞性肺疾病的7項(xiàng)IND許可衣陶,是中國IL-4Rα靶向候選藥物中適應(yīng)癥獲得IND許可最多的產(chǎn)品柄瑰。其中,針對成人中重度特應(yīng)性皮炎剪况、結(jié)節(jié)性癢疹2項(xiàng)適應(yīng)癥已處于3期臨床教沾。
8蒲跨、邦耀生物
目前,邦耀生物已全面布局多靶點(diǎn)授翻、多適應(yīng)癥的通用型CAR-T用于自免疾病的治療或悲,4款布局自免適應(yīng)癥的產(chǎn)品已進(jìn)入臨床。
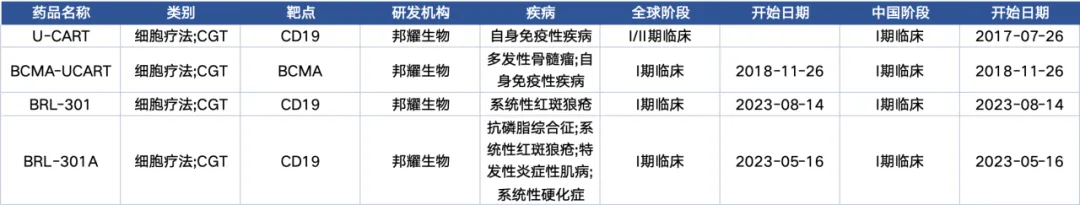
TyU19:2024年7月16日堪唐,邦耀生物宣布巡语,其與華東師范大學(xué)、上海長征醫(yī)院合作的新一代異體通用型CAR-T療法(TyU19)治療自身免疫疾病研究成果于7月15日正式在國際頂級學(xué)術(shù)期刊Cell上發(fā)表羔杨,論文題為“Allogeneic CD19-targeted CAR-T therapy in patients with severe myositis and systemic sclerosis”捌臊。邦耀生物開發(fā)的TyU19屬于異體通用型CAR-T產(chǎn)品,采用健康供者細(xì)胞兜材,具有可及性高肘认、成本低、質(zhì)量穩(wěn)定等諸多特點(diǎn)猖生,并在臨床試驗(yàn)中體現(xiàn)出了顯著的療效和安全性舞铝。這是國際上首次報(bào)道異體通用型CAR-T在治療自身免疫疾病中獲得成功,也是頂級期刊Cell首次發(fā)表CAR-T治療自免疾病的研究成果妥尘。
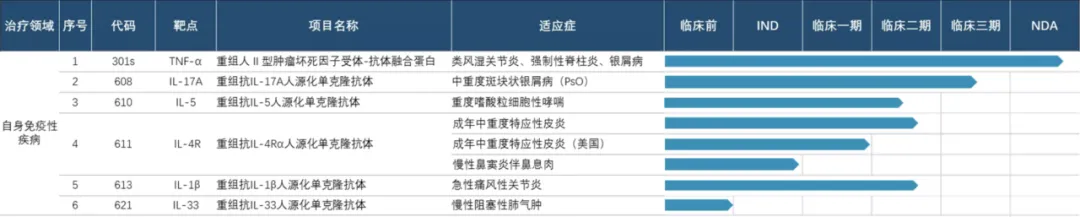
9毁设、三生國健
目前,三生國健進(jìn)入臨床的自免管線共有4條郊蹈,其中在研的抗IL-17A人源化單克隆抗體(“608”)厢卖、抗IL-1β人源化單克隆抗體注射液(“613”)、抗白介素4受體alpha(IL-4Rα)的人源化單克隆抗體藥物(“611”)部分適應(yīng)癥已進(jìn)入3期臨床房肿。
10啊嘁、創(chuàng)響生物
創(chuàng)響生物由資深投資人王健創(chuàng)立,主要采取License-in模式建立豐富的研發(fā)管線暗环。目前干际,擁有3個(gè)臨床階段的候選藥物(IMG-004、MG-007副瀑、IMG-008)和創(chuàng)新的臨床前管線弓熏。
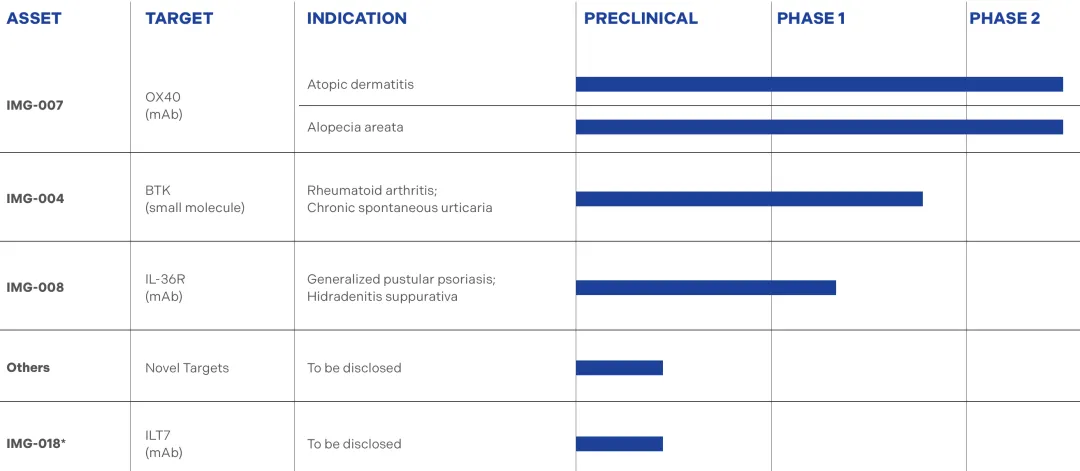
IMG-007,是目前全球唯一處于臨床期糠睡、非耗竭性抗OX40的單克隆抗體挽鞠,以獨(dú)特的方式靶向OX40受體,不清除T細(xì)胞狈孔,并且半衰期長滞谢,具有同類最佳的潛力。IMG-007最初由和黃醫(yī)藥發(fā)現(xiàn)除抛,創(chuàng)響負(fù)責(zé)從藥物候選階段進(jìn)行全球開發(fā)至今狮杨,擁有IMG-007的全球權(quán)利的獨(dú)家選擇權(quán)母截。IMG-007在特應(yīng)性皮炎患者中的臨床2a期研究產(chǎn)生了積極的中期結(jié)果。該2a 期研究是一項(xiàng)評估IMG-007在外用藥物控制不佳和/或不耐受的中重度特應(yīng)性皮炎(AD)成人患者中的安全性橄教,藥代動力學(xué)和有效性的研究清寇,預(yù)計(jì)在2024年第3季度獲得最終結(jié)果。除AD適應(yīng)癥外护蝶,IMG-007正在開展在斑禿患者中的全球2a臨床研究华烟,其結(jié)果預(yù)計(jì)在2024年第4季度產(chǎn)生。
Izokibep青烙,是一種新型雙特異性融合蛋白径瘪,可有效靶向IL-17A和白蛋白。創(chuàng)響擁有其大中華區(qū)及韓國的商業(yè)化權(quán)利冕店,并有權(quán)獲得在全球其他地域中的里程碑付款和銷售分成患敢。2023年3月,創(chuàng)響生物在2023年美國皮膚病學(xué)會(AAD)年會上宣布了該藥物治療中重度化膿性汗腺炎的2b/3期臨床數(shù)據(jù)嘁压,izokibep治療12周后化膿性汗腺炎患者臨床反應(yīng)(HiSCR)顯著增高邦孽,其中膿腫和炎性結(jié)節(jié)總數(shù)量100%減少(HiSCR100)的受試者高達(dá)33%
資料來源:
公司官網(wǎng)
醫(yī)藥魔方
醫(yī)前沿:千億市場:近期數(shù)十家IPO企業(yè)布局自免藥物

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識林
識林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8
 熱門資訊
熱門資訊