
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 細(xì)胞基因治療前沿
細(xì)胞基因治療前沿  2024-08-16
2024-08-16
 219
219
近日左敌,Immunocore公布2024上半年業(yè)績(jī):總營(yíng)收1.46億美元梯刚,同比增長(zhǎng)27.5%即钞;研發(fā)費(fèi)用1.09億美元浪谴,同比增長(zhǎng)45%胞仅。其中2024 Q2總營(yíng)收7540萬(wàn)美元(約5.4億元)捐下,同比增長(zhǎng)32%李狼。研發(fā)費(fèi)用為5107.2萬(wàn)美元毕模,同比增長(zhǎng)34%课枉。截至2024年6月30日属胖,現(xiàn)金及現(xiàn)金等價(jià)物為5.05億美元。
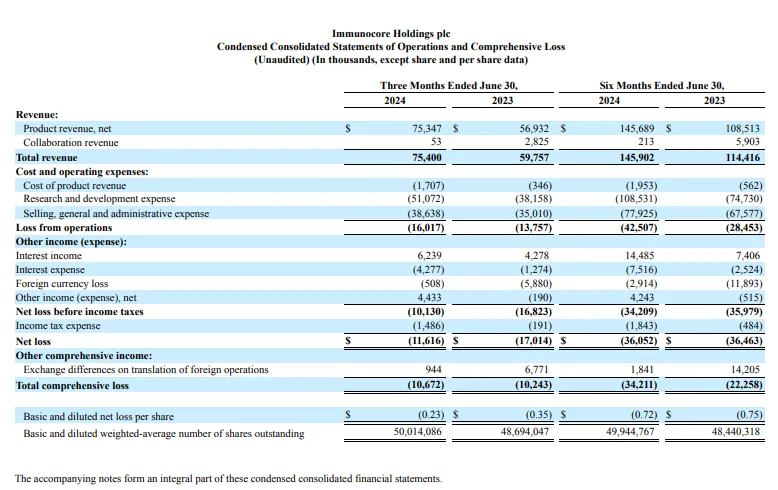
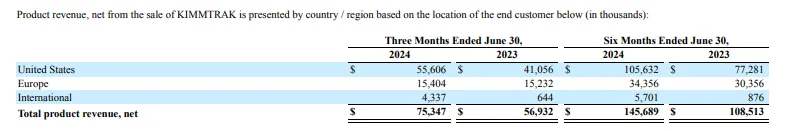
kimmtrak在2024 H1凈銷售額1.46億美元(約10.46億元),同比增長(zhǎng)34%莲疤;2024 Q2凈銷售額達(dá)到7534.7萬(wàn)美元(約5.4億元)恃定,同比增長(zhǎng)32%。在kimmtrak獲批的38個(gè)國(guó)家/地區(qū)中砍机,美國(guó)凈銷售額達(dá)到5560.6萬(wàn)美元寞殿,歐洲達(dá)到1540.4萬(wàn)美元,國(guó)際地區(qū)為433.7萬(wàn)美元铭莱。Immunocore將繼續(xù)推動(dòng)kimmtrak全球上市和關(guān)鍵市場(chǎng)的市場(chǎng)份額增長(zhǎng)骡尽。
作為全球首款獲得監(jiān)管批準(zhǔn)的T細(xì)胞受體(TCR)療法,kimmtrak是一款靶向gp100的TCR與靶向CD3的scFv的融合蛋白擅编。2022年1月攀细,kimmtrak在三期臨床數(shù)據(jù)中打敗了K藥和CTLA-4單抗,獲FDA批準(zhǔn)用于治療HLA-A*02:01基因型爱态、轉(zhuǎn)移性或不可切除的葡萄膜黑色素瘤谭贪,這是FDA批準(zhǔn)的首款治療不可切除或轉(zhuǎn)移性葡萄膜黑色素瘤的療法,也是首款獲得監(jiān)管批準(zhǔn)的TCR細(xì)胞療法锦担。美國(guó)定價(jià)kimmtrak為40萬(wàn)美元/年俭识。
公司的主導(dǎo)產(chǎn)品kimmtrak已在38個(gè)國(guó)家獲得批準(zhǔn),迄今已在全球19個(gè)國(guó)家上市吆豹,用于治療HLA-A*02:01陽(yáng)性的不可切除或轉(zhuǎn)移性葡萄膜黑色素瘤 (mUM) 患者鱼的。在瑞典和波蘭達(dá)成了報(bào)銷協(xié)議,預(yù)計(jì)將于2024年下半年上市痘煤。kimmtrak仍是大多數(shù)市場(chǎng)的標(biāo)準(zhǔn)治療方案凑阶。公司認(rèn)為kimmtrak有三大增長(zhǎng)點(diǎn),包括:繼續(xù)在全球擴(kuò)大mUM的治療范圍衷快,并有可能擴(kuò)展到2L+晚期皮膚黑色素瘤 (CM) 和葡萄膜黑色素瘤輔助治療領(lǐng)域宙橱。
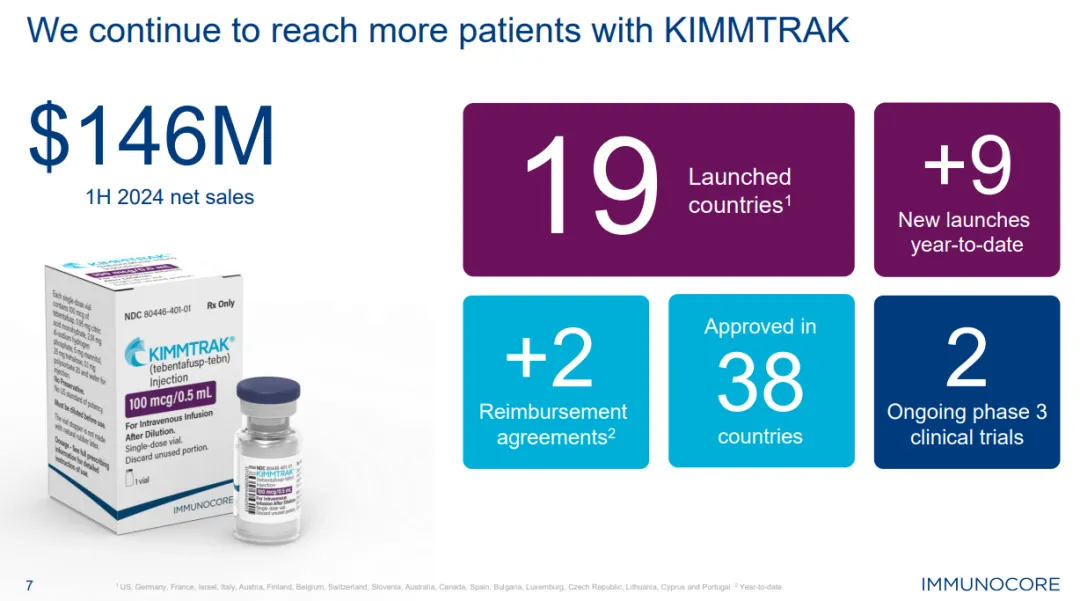
關(guān)于Immunocore
Immunocore是一家處于商業(yè)化階段的先鋒T細(xì)胞受體生物技術(shù)公司,致力于開(kāi)發(fā)和商業(yè)化新一代變革性藥物贬市,以滿足癌癥版掘、傳染病和自身免疫性疾病領(lǐng)域尚未得到滿足的需求。
Immunocore最初的治療重點(diǎn)是腫瘤學(xué)劈警,領(lǐng)先項(xiàng)目治療轉(zhuǎn)移性葡萄膜黑色素瘤(一種罕見(jiàn)的眼癌)的潛在療法——腫瘤TCR治療藥物KIMMTRAK已經(jīng)獲批上市昔疆。公司利用其專有的、靈活的遵盼、現(xiàn)成的ImmTAX平臺(tái)谤郑,Immunocore正在開(kāi)發(fā)多個(gè)治療領(lǐng)域的深層管線,包括腫瘤學(xué)和感染性疾病和自身免疫疾病的多個(gè)高級(jí)臨床前項(xiàng)目和早期臨床前項(xiàng)目刑映。
Immunocore研發(fā)管線
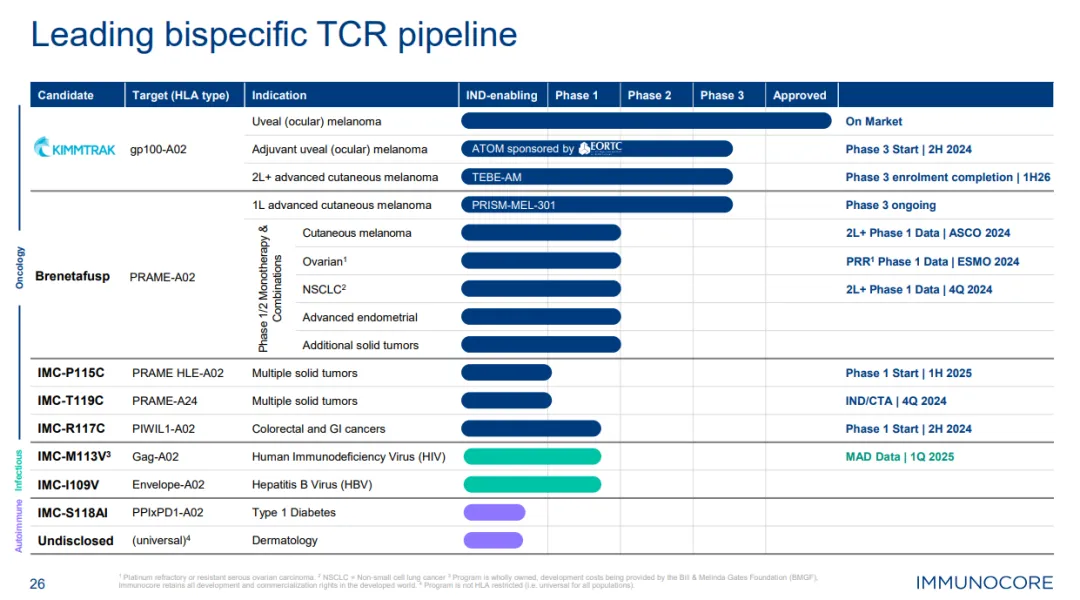
總結(jié)
TCR-T細(xì)胞治療已廣泛應(yīng)用于惡性黑素色瘤直呈、尿路上皮癌、直腸癌、食管癌忽畏、滑膜肉瘤等實(shí)體瘤患者惋涌,相關(guān)療效曾被NATURE等國(guó)際頂尖醫(yī)學(xué)刊物報(bào)道,國(guó)內(nèi)外多家藥企入局該領(lǐng)域赖钞。據(jù)不完全統(tǒng)計(jì)腰素,國(guó)內(nèi)布局TCR-T細(xì)胞療法的企業(yè)有香雪生命科學(xué)、來(lái)恩生物仁烹、百吉生物耸弄、星漢德咧虎、天科雅卓缰、華夏英泰、恒瑞源正砰诵、可瑞生物征唬、科士華生物、新景智源茁彭、鑌鐵生物总寒、鼎成肽源、立凌生物理肺、星銳醫(yī)藥摄闸、科銳邁德、因諾免疫妹萨、泛恩生物蟹故、科士華等,其中大部分企業(yè)的TCR-T產(chǎn)品都已經(jīng)進(jìn)入臨床研究階段剃杯,今年也有諸多企業(yè)取得進(jìn)展:
今年4月逾丑,科士華創(chuàng)新TCR-T細(xì)胞療法KSH01注射液獲批臨床;藥明巨諾啟動(dòng)MAGE-A4 TCR-T細(xì)胞療法的IIT臨床試驗(yàn)沽糕;5月 嘲孙,鼎成肽源KRAS G12D靶向TCR-T療法DCTY1102注射液的臨床試驗(yàn)申請(qǐng)獲得NMPA受理;靈識(shí)質(zhì)源完成天使輪融資启血,加速推動(dòng)TCR-T及TCR融合蛋白藥物技術(shù)開(kāi)發(fā)魂姆;7月,鑌鐵生物KRAS靶向TCR-T細(xì)胞療法IND申請(qǐng)獲受理户载;星漢德生物全新一代TCR-T細(xì)胞療法SCG142在美獲批I/II期臨床試驗(yàn)澜茁;香雪制藥TAEST16001注射液成功入選突破性治療藥物品種,是中國(guó)首個(gè)獲得IND批件并開(kāi)展臨床研究的TCR-T細(xì)胞產(chǎn)品征啦。
參考資料:?immunocore官網(wǎng)

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽