
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Insight數(shù)據(jù)庫(kù)
Insight數(shù)據(jù)庫(kù)  2024-08-22
2024-08-22
 76
76
8 月 21 日烤恃,國(guó)家藥監(jiān)局藥品審評(píng)中心顯示蒲赂,諾誠(chéng)健華奧布替尼片的新適應(yīng)癥上市申請(qǐng)受理(受理號(hào):CXHS2400078)装呢。Insight數(shù)據(jù)庫(kù)推測(cè)咙轩,該藥本次申報(bào)的新適應(yīng)癥可能為:初治的慢性淋巴細(xì)胞白血病/小淋巴細(xì)胞淋巴瘤蠕蹋。另外哀墓,諾誠(chéng)健華今日發(fā)布的上半年財(cái)報(bào)顯示显熏,奧布替尼上半年銷售額實(shí)現(xiàn)了 30% 的增長(zhǎng)至為 4.18 億元泽篮。

截圖來(lái)源:CDE官網(wǎng)
奧布替尼是諾誠(chéng)健華研發(fā)的一款不可逆布魯頓酪氨酸激酶(BTK)抑制劑盗尸,可用于治療淋巴瘤及自身免疫性疾病。2020 年 12 月,奧布替尼在國(guó)內(nèi)獲批用于既往至少接受過(guò)一種治療的成人慢性淋巴細(xì)胞白血财酶鳌(CLL)/小淋巴細(xì)胞淋巴瘤(SLL)患者以及成人套細(xì)胞淋巴瘤(MCL)患者鞍时;2023 年 4 月,奧布替尼又在國(guó)內(nèi)獲批用于治療復(fù)發(fā)/難治性邊緣區(qū)淋巴瘤(MZL)患者扣蜻。根據(jù)諾誠(chéng)健華今日發(fā)布的 2024 年中期業(yè)績(jī)報(bào)告顯示逆巍,奧布替尼 2024 年 Q2 銷售額為 2.53 億元,去年同期為 1.70 億元莽使,同比增長(zhǎng) 49%厚较;2024 年上半年銷售額為 4.18 億元,去年同期為 3.21 億元港苗,同比增長(zhǎng) 30%蚤岗。
根據(jù)奧布替尼正在開(kāi)展的臨床研究,Insight數(shù)據(jù)庫(kù)推測(cè)陌贪,該藥本次申報(bào)的新適應(yīng)癥可能為:初治的慢性淋巴細(xì)胞白血病/小淋巴細(xì)胞淋巴瘤变硬。
在 2023 年美國(guó)血液學(xué)會(huì)(ASH)年會(huì)上,諾誠(chéng)健華公布了奧布替尼想触、氟達(dá)拉濱粱宝、環(huán)磷酰胺和抗 CD20 單抗奧妥珠單抗(OFCG)一線治療 CLL 患者的臨床試驗(yàn) (cwCLL-001 研究)數(shù)據(jù)。結(jié)果顯示:
19 例患者完成了 3 周期的 OFCG 治療并可評(píng)估晾充。75%(15/20)的患者達(dá)到外周血 MRD 陰性玖膨,57.9%(11/19)的患者達(dá)到骨髓 MRD 陰性,ORR 和 CR/CRi 率分別為 100% (18/18) 和 38.9% (7/18)崭湾。
16 例患者完成 6 個(gè)周期赛邢,其中 14 例可評(píng)估,并且在第 4 至 6 周期期間無(wú)論采用何種策略均獲得了更深層次的緩解猛蔽,外周血 MRD 陰性率和骨髓 MRD 陰性率分別為 100% 和 85.7%戚嗅,ORR 和 CR 率分別為 100% 和 57.1%(8/14)。
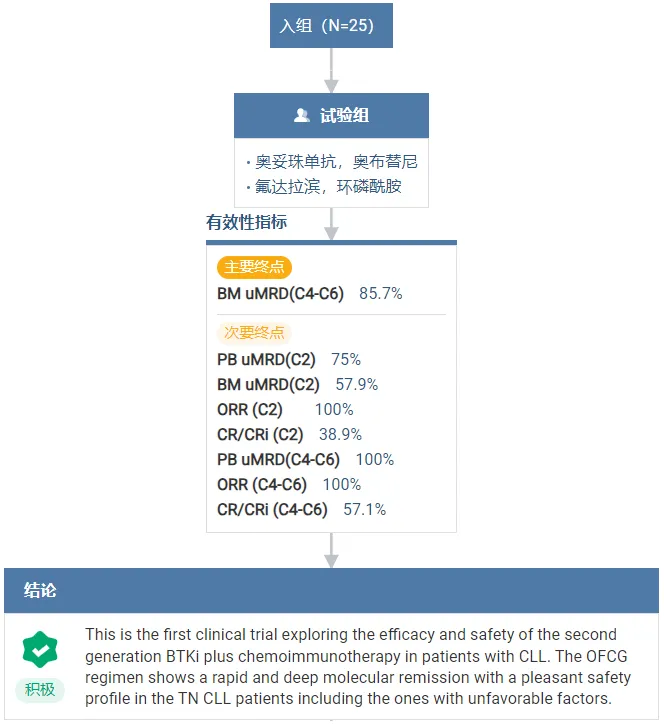
截圖來(lái)源:Insight數(shù)據(jù)庫(kù)
安全性方面枢舶,大多數(shù) AE 是輕微且可耐受的懦胞。最常見(jiàn)的 AE(任何等級(jí)≥10%)是中性粒細(xì)胞減少癥、白細(xì)胞減少癥和血小板減少癥凉泄。這些患者未發(fā)生 3 級(jí)以上的出血或心血管 AE躏尉。總體而言,OFCG 表現(xiàn)出良好的安全性后众。結(jié)論是 OFCG 方案在 TN CLL 患者(包括有不良因素的患者)中表現(xiàn)出快速胀糜、深度的分子緩解,且安全性良好蒂誉。
除了上述試驗(yàn)教藻,諾誠(chéng)健華還在進(jìn)行一項(xiàng)評(píng)價(jià)奧布替尼對(duì)比苯丁酸氮芥聯(lián)合利妥昔單抗治療處置的慢性淋巴細(xì)胞白血簿嗨А(CLL)/小淋巴細(xì)胞淋巴瘤(SLL)的隨機(jī)、對(duì)照括堤、開(kāi)放性碌秸、多中心 Ⅲ 期臨床試驗(yàn)(登記號(hào):CTR20201980、NCT04578613)沛专。試驗(yàn)的主要終點(diǎn)是無(wú)進(jìn)展生存期尖蚪,次要終點(diǎn)包括 IRC 和研究者評(píng)估的客觀緩解率(ORR)、緩解持續(xù)時(shí)間(DoR)讯翎、研究者評(píng)估的無(wú)進(jìn)展生存期(PFS)嫉簿、總生存期(OS)、安全性和耐受性以及微小殘留病灶(MRD)等最勤。
此外封鹦,奧布替尼已經(jīng)獲得 FDA 的突破性療法認(rèn)定,用于既往至少接受過(guò)一次治療的套細(xì)胞淋巴瘤(r/r MCL)坚矢,目前已經(jīng)完成患者入組挥桑,預(yù)計(jì)今年下半年向 FDA 遞交 NDA 上市申請(qǐng)。在國(guó)內(nèi)理秃,諾誠(chéng)健華正在開(kāi)展奧布替尼單藥或者聯(lián)合用藥的多中心、多適應(yīng)癥臨床試驗(yàn)豆玖,如一線治療彌漫性大 B 細(xì)胞淋巴瘤 MCD 亞型等適應(yīng)癥柴伪。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽