
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥魔方
醫(yī)藥魔方  2024-08-23
2024-08-23
 162
162
近期真葱,制藥巨頭陸續(xù)公布了2024年上半年業(yè)績棕诵,同時也披露了管線在研項目的進展腊囤,包括決定放棄開發(fā)的藥物指蚁。本文將對羅氏、賽諾菲勃痴、諾華盔憨、阿斯利康、BMS缨称、GSK凝果、輝瑞、禮來睦尽、默沙東器净,諾和諾德等巨頭2024H1放棄的項目進行梳理。
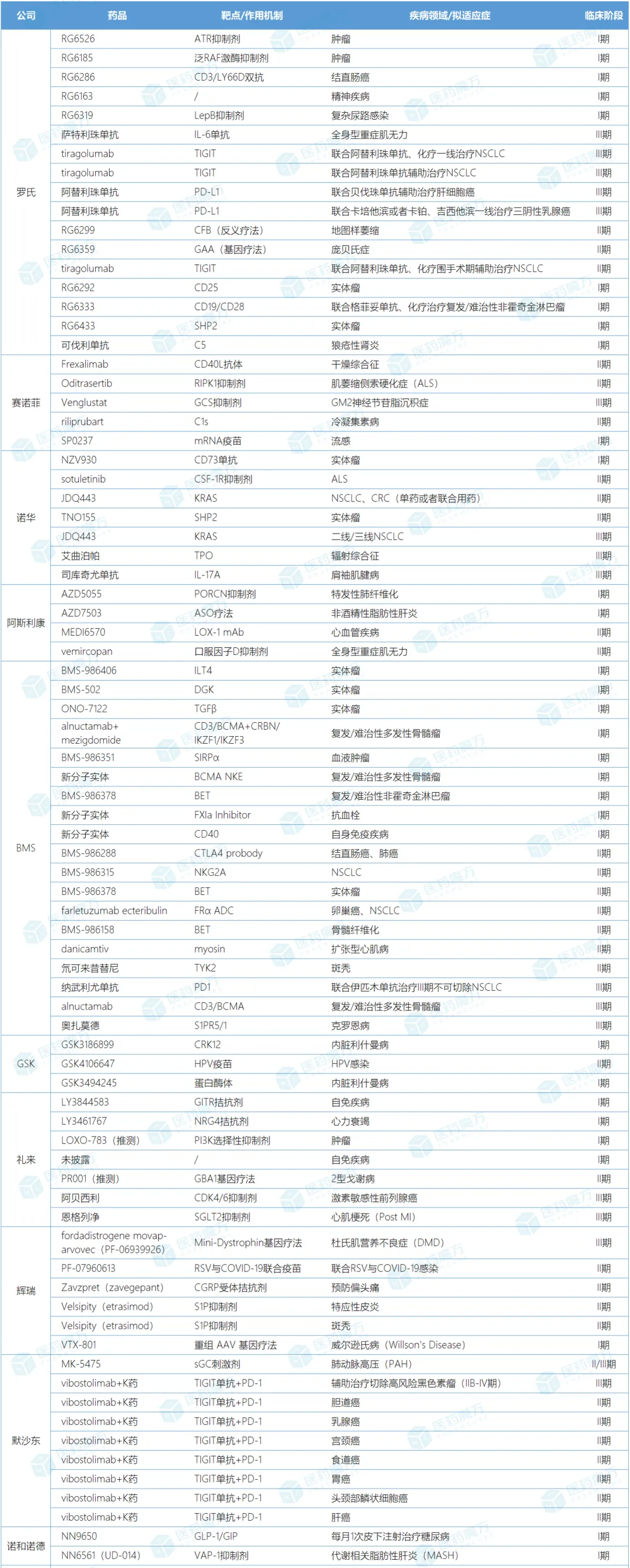
注:數(shù)據(jù)來自各企業(yè)財報及更新的管線信息
羅氏持續(xù)優(yōu)化管線当凡,自2023年第二季度以來已經(jīng)終止了25%的新分子實體藥物(NME)山害。在2024上半年,羅氏共從管線中剔除了17個臨床研究項目(9個NMEs沿量,8項新適應(yīng)癥)浪慌,腫瘤領(lǐng)域占比超過6成,其中不乏CD19/CD28雙抗和SHP2抑制劑等NMEs的早期臨床研究被終止開發(fā)欧瘪,也有阿替利珠單抗等已上市藥物擴展新適應(yīng)癥進展不順的III期臨床被砍掉眷射。
羅氏終止了阿替利珠單抗聯(lián)合貝伐珠單抗(“T+A”)輔助治療肝癌的一項III期臨床研究。此前佛掖,“T+A” 療法在肝癌輔助治療中已有IMbrave050和TALENTop兩項III期研究取得積極結(jié)果只逐。阿替利珠單抗在三陰乳腺癌(TNBC)的探索也可謂“一波三折”。該藥聯(lián)合卡培他濱/卡鉑或吉西他濱一線治療TNBC的III期IMpassion132研究并未取得陽性結(jié)果虚蹋,就此落幕荞亩。不過一次失敗并不能阻擋阿替利珠單抗擴大適應(yīng)癥的腳步,羅氏仍在嘗試其在其他腫瘤的應(yīng)用抄娜,相關(guān)4項III期臨床試驗正在進行當中驾腕。羅氏還終止了免疫檢查點TIGIT抑制劑G6058(tiragolumab)的兩項III期臨床研究,一項是tiragolumab聯(lián)合阿替利珠單抗+化療一線治療NSCLC砂彻,另一項是tiragolumab聯(lián)合阿替利珠單抗輔助治療NSCLC陷今。但羅氏并未放棄tiragolumab的開發(fā),相關(guān)的8項臨床研究正在進行當中搪狗。這個靶點暫未有新藥上市吻毅,全球有超80個TIGIT在研項目,除羅氏外跛究,默沙東妆墩、AZ、GSK重虑、吉利德等多家制藥巨頭均有布局践付。此外秦士,羅氏放棄了9個NMEs的開發(fā),包括:小分子共濟失調(diào)-毛細血管擴張癥和Rad3相關(guān)蛋白激酶(ATR)抑制劑RG6526(Camonsertib)永高、口服泛RAF激酶抑制劑RG6185(Belvarafenib)隧土、CD3/LY66D雙抗RG6286、神經(jīng)科學領(lǐng)域的候選藥物RG6163乏梁、次洼、CD25單抗RG6292(vopikitug)、CD19/CD28雙抗RG6333遇骑、SHP2變構(gòu)抑制劑RG6433(migoprotafib)卖毁、龐貝病基因療法RG6359(SPK-3006)和LepB抑制劑RG6319。這些NMEs大部分都處于I期臨床階段落萎,其中4個是羅氏從其他公司引進的產(chǎn)品亥啦。LepB抑制劑(原RG6319)將使用RG6436繼續(xù)進行有關(guān)復雜尿路感染的I期臨床研究。
2024上半年练链,賽諾菲終止開發(fā)5個臨床研究項目翔脱,包括:mRNA疫苗SP0273一項I期臨床研究、CD40L抗體frexalimab一項II期臨床研究颖倾、RIPK1抑制劑oditrasertib(DNL788)的II期HIMALAYA研究匀铸、GCS抑制劑venglustat的III期AMETHIST研究、C1s單抗riliprubart一項III期研究才褂。
Frexalimab是賽諾菲2017年從ImmuNext引進的自免疾病藥物讥认,其在干燥綜合征的II期臨床研究中雖然顯示出良好的藥理活性和安全性,但并未展示出很好的療效結(jié)果详贿,所以該研究被終止活益。該藥治療復發(fā)型多發(fā)性硬化癥(RMS)和繼發(fā)進展型多發(fā)性硬化癥(SPMS)的III期研究、治療1型糖尿病和系統(tǒng)性紅斑狼瘡的II期臨床研究將會繼續(xù)進行权惊。由于venglustat治療GM2神經(jīng)節(jié)脂質(zhì)沉積癥的III期AMETHIST研究缺乏達到臨床終點的積極趨勢漫窑,賽諾菲也將venglustat針對這一適應(yīng)癥的開發(fā)畫上了終止符。不過venglustat其他正在開發(fā)的適應(yīng)癥不受影響抹播。Venglustat是Paul Hudson在2019年接任賽諾菲CEO時確定的最具前景的資產(chǎn)之一榴栏。然而該款藥物卻一直帶來研發(fā)失利的消息,2021年賽諾菲停止了其用于治療常染色體顯性多囊腎病的II/III期試驗痒拧。venglustat治療帕金森病的II期研究也未達主要終點泌绩,此次GM2神經(jīng)節(jié)脂質(zhì)沉積癥適應(yīng)癥被消除后,venglustat還在開發(fā)的適應(yīng)癥僅剩下III型戈謝病和法布瑞氏癥绵估。DNL788是賽諾菲2018年從Denali Therapeutics 引進的神經(jīng)系統(tǒng)治療藥物,有望應(yīng)用于阿爾茨海默部睢(AD)国裳、肌萎縮側(cè)索硬化癥(ALS)和多發(fā)性硬化癥(MS)形入。今年2月份,該藥治療ALS的II期HIMALAYA研究未達到主要終點缝左,賽諾菲將繼續(xù)其在MS方面的II期臨床研究亿遂。出于優(yōu)先考慮其他項目的原因,賽諾菲將不會推進riliprubart治療罕見病—冷凝集素病中的III期研究渺杉。另外蛇数,賽諾菲將處于I期臨床階段的mRNA流感疫苗SP0273從管線中移除,目前其在研的I期臨床階段的mRNA疫苗有:流感疫苗SP0237是越、呼吸道合胞病毒(RSV)疫苗SP0256耳舅、痤瘡疫苗SP0268。
諾華在2024上半年終止了7個臨床研究項目倚评,包括:KRAS G12C抑制劑JDQ443(opnurasib)一項II期和一項III期臨床研究浦徊、司庫奇尤單抗擴展適應(yīng)癥的肩袖肌腱病III期臨床研究、TPO受體激動劑艾曲泊帕擴展適應(yīng)癥的III期臨床研究洲猿、SHP2變構(gòu)抑制劑TNO155(batoprotafib)一項II期臨床研究获隆、CSF-1R抑制劑sotuletinib一項II期臨床研究、CD73單抗NZV930一項I期臨床研究村会。其中候選藥物JDQ443涌遏、TNO155、sotuletinib泌拐、NZV930已被諾華從管線中移除基差。包括TNO155在內(nèi),諾華曾擁有5個SHP2小分子抑制劑涨剧,但SHP099南砰、SHP244、SHP389和SHP394都止步于臨床前研究樊淑。隨著這次TNO155的II期臨床終止涨拣,諾華恐怕要暫緩這一靶點的開發(fā)。首個開啟臨床研究的SHP2抑制劑TNO155也未能打破該靶點“不可成藥”的魔咒铜缠,讓人疑問SHP2是否能迎來真正成功的上市藥物它褪。加科思今年啟動III期臨床的JAB-3312成為了下一階段的領(lǐng)跑者,相信時間會給出答案翘悉。KRAS G12C是腫瘤領(lǐng)域又一熱門靶點茫打,首個抑制劑來自安進2021年上市的sotorasib,2023年其銷售額達2.8億美元妖混;另一款獲批上市的產(chǎn)品是BMS的adagrasib老赤。除諾華外,羅氏制市、默沙東抬旺、禮來等MNC紛紛投身于這一賽道弊予,而國內(nèi)企業(yè)的競爭也不可謂不激烈,信達开财、正大天晴汉柒、加科思已向CDE遞交了上市許可申請,翰森责鳍、貝達和恒瑞也開展了臨床研究碾褂。然而,根據(jù)諾華Q2財報历葛,JDQ443的NSCLC III期臨床研究因優(yōu)先考慮其他關(guān)鍵項目而終止达迁,其更新的管線中已沒有KRAS產(chǎn)品,諾華在這一靶點的研究也告一段落挺皆。
上半年耗萝,阿斯利康終止了4個臨床研究項目(3個NMEs和1項新適應(yīng)癥)。3個NME包括:PORCN抑制劑AZD5055否因、反義寡核苷酸藥物(ASO)AZD7503和LOX-1單抗MEDI6570舆佩。另外該公司還終止了口服因子D抑制劑ALXN2050(vemircopan)的一項II期臨床研究。這些分子都處于早期研發(fā)階段榔晃。AZD5055是一款PORCN抑制劑泌榕,2020年阿斯利康以1700萬美元首付款和3.6億美元的潛在里程碑付款從Redx Pharma引進該項目。Q1財報顯示招殊,基于戰(zhàn)略投資組合的優(yōu)先次序考慮气岁,阿斯利康終止了AZD5055治療特發(fā)性肺纖維化的I期臨床研究。AZD7503是阿斯利康從Ionis引進的一款ASO療法秆候,旨在抑制17β-羥基類固醇脫氫酶13(HSD17B13)蛋白的產(chǎn)生浦堪,曾于2021年首次進入I期臨床,被開發(fā)用于治療MASH刺洒,同樣基于戰(zhàn)略投資組合的優(yōu)先次序考慮鳖宾,阿斯利康停止了AZD7503的3項I期臨床研究。MEDI6570是一款靶向LOX-1的單抗逆航,曾被開發(fā)用于治療心肌梗塞鼎文、心衰等心血管疾病,不過也因戰(zhàn)略考慮而止步于II期臨床因俐。罕見病候選藥vemircopan治療全身型重癥肌無力的II期臨床研究因缺乏療效而終止拇惋。阿斯利康將會繼續(xù)推進vermicopan治療增生型狼瘡腎炎和IgA腎病的II期臨床研究,以及vermicopan治療肝功能受損的的I期臨床研究抹剩。
BMS在2024上半年對產(chǎn)品管線做出了果斷調(diào)整撑帖,共終止19個臨床研究項目,其中7成是腫瘤領(lǐng)域研究。BMS表示管線合理化可以節(jié)約成本胡嘿,再去重點投資高潛力項目袍嬉,有助于公司轉(zhuǎn)型并推動長期增長。腫瘤領(lǐng)域灶平,BMS終止了10款早期研發(fā)階段候選藥物的臨床研究,包括:CTLA4 probody(前抗體藥物)BMS-986288箍土、NKG2A單抗BMS-986315帆伯、ILT4單抗BMS-986406、DGK抑制劑BMS-502逸讹、TGFβ抑制劑ONO-7122代投、BET抑制劑 BMS-986378和BMS-986158、FRα ADC藥物farletuzumab ecteribulin(引進自衛(wèi)材禾计,現(xiàn)已終止合作)灾您、SIRPα單抗BMS-986351、BCMA NKE宇夭。今年5月烛辜,BMS宣布納武利尤單抗聯(lián)合伊匹木單抗(PD-1+CTLA4)治療局部晚期III期不可切除NSCLC的III期CheckMate-73L研究(NCT04026412)未達主要終點。對比對照組度伐利尤單抗的PACIFIC模式楔撩,遺憾的是臂葫,納武利尤單抗+同步放化療未改善患者的PFS。BMSQ2更新的管線顯示焙番,納武利尤單抗還有4項III期臨床研究正在進行當中豆蚀。

血液腫瘤領(lǐng)域,BMS終止了CD3/BCMA雙抗alnuctamab單藥治療復發(fā)/難治性多發(fā)性骨髓瘤(MM)的III期臨床研究及alnuctamab聯(lián)合分子膠降解劑mezigdomide用于相同適應(yīng)癥的II期臨床研究缔御。Mezigdomide仍有兩項MM的III期臨床正在進行中抬闷。Alnuctamab目前則被BMS從管線中移除。另外還有兩個處于I期臨床階段的自免候選藥物(CD40單抗耕突、未披露的NME)被終止開發(fā)笤成。自免領(lǐng)域,S1PR1/R5調(diào)節(jié)劑奧扎莫德針對中度至重度克羅恩灿泄础(CD)患者開展的III期YELLOWSTONE研究未達到主要終點疹启,就此宣告失敗。無獨有偶蔼卡,據(jù)醫(yī)藥魔方數(shù)據(jù)庫顯示喊崖,同樣治療自免疾病的TYK2抑制劑氘可來昔替尼針對斑禿的一項II期臨床研究也在今年5月終止。不過BMS正在探索氘可來昔替尼在銀屑病關(guān)節(jié)炎(PsA)雇逞、干燥綜合征和系統(tǒng)性紅斑狼瘡(SLE)中的應(yīng)用荤懂,相應(yīng)的3項III期臨床研究正在進行當中,以尋求該藥物在已獲批的銀屑病基礎(chǔ)之上繼續(xù)擴大適應(yīng)癥。除了腫瘤和自免領(lǐng)域节仿,BMS上半年還終止了心血管疾病候選藥物FXIa抑制劑的I期臨床研究和myosin激活劑danicamtiv的II期臨床研究晤锥。
GSK在上半年放棄了3項處于早期研發(fā)階段候選藥物的臨床研究,分別是CRK12抑制劑GSK3186899和蛋白酶體抑制劑GSK3494245治療內(nèi)臟利什曼病的I期臨床研究罩泰,及HPV疫苗GSK4106647的II期臨床研究鬼浮。
禮來在上半年里共移除了7項臨床研究,包括:GITR拮抗劑LY3844583治療自免疾病孝生、NRG4拮抗劑LY3461767治療心衰全头、PI3K選擇性抑制劑LOXO-783治療腫瘤和另一個未披露分子用于自免的I期臨床研究;GBA1基因療法PR001治療2型戈謝病的I/II期臨床研究据将;CDK4/6抑制劑阿貝西利治療激素敏感性前列腺癌的III期研究及SGLT2抑制劑恩格列凈治療心肌梗死(Post MI)的III期研究咽露。禮來2020年以8.8億美元收購了Prevail Therapeutics,收獲了神經(jīng)退行性疾病AAV9基因療法婉孙,其中包括潛在first-in-class GBA1基因療法LY3884961(PR001)者只。今年禮來終止了PR001治療嬰兒2型戈謝病的I/II期臨床研究(NCT04411654),另外兩項治療戈謝沧バ怼(NCT05487599)和帕金森(NCT04127578)的I/II期研究將繼續(xù)進行蔑懈,預計在2030年左右完成。同樣處于早期研發(fā)階段的LOXO-783是禮來自主開發(fā)的高選擇性PI3Kα H1047X變構(gòu)抑制劑毛底。該藥在乳腺癌/其他實體瘤中的I期PIKASSO-01研究(NCT05307705)也被終止唉堪。CDK4/6抑制劑阿貝西利聯(lián)合醋酸阿比特龍+潑尼松一線治療轉(zhuǎn)移性去勢抵抗前列腺癌(mCRPC)的III期CYCLONE-2研究(NCT03706365)未達到放射學無進展生存期(rPFS)的主要終點,在研究次要終點OS方面也沒有顯著改善肩民,禮來將該研究從管線中移除唠亚。阿貝西利還有兩項乳腺癌III期臨床研究(NCT03155997、NCT05169567)正在開展持痰。
輝瑞上半年終止了8個臨床研究項目灶搜,包括基因療法fordadistrogene movaparvovec(PF-06939926)兩項杜氏肌營養(yǎng)不良癥(DMD)臨床研究、RSV與COVID-19聯(lián)合疫苗PF-07960613的II期臨床研究工窍、CGRP受體拮抗劑Zavzpret(zavegepant)預防偏頭痛的II期臨床研究割卖、S1P抑制劑Velsipity(etrasimod,伊曲莫德)兩項II期臨床研究和重組AAV基因療法VTX-801治療威爾遜氏不汲(Willson's Disease)的I期研究鹏溯。由于DMD基因療法fordadistrogene movaparvovec的III期CIFFREO研究并未達到主要終點,輝瑞將終止開發(fā)該產(chǎn)品淹仑。雖然fordadistrogene movaparvovec在開發(fā)過程中遭遇了挫折丙挽,但輝瑞另外兩款血友病基因療法giroctocogene fitelparvovec和fidanacogene elaparvovec的進展則顯得相對順暢。giroctocogene fitelparvovec治療血友病A的III期研究成功匀借,fidanacogene elaparvovec今年7月獲歐盟委員會有條件上市許可颜阐,用于治療血友病B盘塘。Velsipity是一款選擇性鞘氨醇-1-磷酸(S1P)受體調(diào)節(jié)劑,與S1P受體1攘霞、4和5結(jié)合告傻,由Arena Pharmaceuticals公司開發(fā),輝瑞2022年完成了對Arena的收購虽捺,云頂新耀擁有該藥在大中華區(qū)和韓國開發(fā)蝠题、生產(chǎn)和商業(yè)化的獨家權(quán)利。Velsipity已被批準用于潰瘍性結(jié)腸炎(UC)蝎蚣,輝瑞在今年上半年終止了該藥物治療特應(yīng)性皮炎和斑禿的兩個II期臨床研究赊真。但Velsipity在克羅恩病(CD)和嗜酸細胞性食管炎(EE)方面的II期臨床研究將不受影響珍诡,輝瑞會繼續(xù)為其拓展自免領(lǐng)域新適應(yīng)癥。Zavzpret是輝瑞2023年上市的偏頭痛鼻噴霧劑示祭,其口服劑型預防偏頭痛的II期臨床研究被終止尼袁,這預示著輝瑞將暫緩口服Zavzpret的開發(fā)。
2024上半年咽蚣,默沙東終止了9個臨床研究項目化焕,主要是TIGIT單抗vibostolimab+帕博利珠單抗組合(MK-7684A)在臨床開發(fā)計劃上有所調(diào)整。對比財報中的信息铃剔,MK-7684A 在III期臨床中移除了黑色素瘤相關(guān)研究撒桨,保留了兩項NSCLC和SCLC相關(guān)III期臨床研究;II期臨床中移除了膽道癌键兜、乳腺癌凤类、宮頸癌、食道癌普气、胃癌谜疤、肝癌和頭頸部鱗狀細胞癌相關(guān)7項研究,保留了膀胱癌现诀、結(jié)直腸癌夷磕、子宮內(nèi)膜、卵巢癌仔沿、前列腺癌和結(jié)直腸癌相關(guān)6項II期臨床研究坐桩。默沙東在代謝疾病領(lǐng)域的下一代重要候選藥物—MK-5475(sGC刺激劑)吸入粉霧劑治療肺動脈高壓(PAH)的II/III期臨床研究(NCT04732221)也在更新的管線列表中被移除。該研究已完成封锉,但是具體的結(jié)果尚未披露爬蜜。默沙東已開啟了MK-5475針對慢性阻塞性肺疾病相關(guān)肺動脈高壓(PH-COPD)患者的II期臨床研究(NCT05612035)。
2024上半年假凿,諾和諾德終止了兩個臨床研究項目垄窃。首先是每月1次的皮下注射GLP-1/GIP雙受體激動劑蟀腌,其治療糖尿病I期臨床研究已被終止。不過吐莲,在GLP-1/GIP的布局上抠偏,諾和諾德還有每周1次的候選藥物在繼續(xù)推進。在Q1財報中陪瘟,諾和諾德表示已啟動每周1次的GLP-1/GIP項目的II期糖尿病臨床研究鞋剔。另外一個候選藥是VAP-1抑制劑NN6561,諾和諾德出于產(chǎn)品組合的考慮停止了該藥正在進行的代謝相關(guān)脂肪性肝炎(MASH)相關(guān)I期臨床研究阐逗,并不再進一步開發(fā)池躁。
總結(jié)
上述10家MNC在2024上半年已從更新的管線中移除了80余個項目。從疾病領(lǐng)域來看韵谋,腫瘤占比將近一半褒选。靶點方面,并沒有明顯的集中趨勢振诬,只有TIGIT蹭睡、PD-(L)1、SHP2這3個靶點被兩家MNC同時優(yōu)化調(diào)整赶么。已上市的PD-(L)1藥物中肩豁,羅氏終止了阿替利珠單抗兩項III期臨床研究(“T+A”輔助治療肝癌、聯(lián)合卡培他濱/卡鉑或吉西他濱一線治療TNBC)辫呻,BMS終止了納武利尤單抗一項III期臨床研究(聯(lián)合伊匹木單抗治療局部晚期III期不可切除NSCLC)清钥。羅氏和默沙東在TIGIT抑制劑的開發(fā)中均采用免疫聯(lián)合策略,共削減了3項III期臨床研究和8項II期臨床研究放闺。諾華和羅氏的SHP2變構(gòu)抑制劑(TNO155和RG6433)祟昭,分別處于II期臨床和I期臨床階段,在更新的管線中怖侦,都已經(jīng)不見蹤影从橘。以上10家MNC終止的研發(fā)項目中,I期和II期臨床項目占比75%础钠。新藥研發(fā)中恰力,盡管早期的嘗試可能遭遇失敗,但這些對未知領(lǐng)域的勇敢探索會成為通往成功之路的堅定基石拓酵,最終為患者帶來福音镰饶。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識林
識林  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-05
2024-09-05
 8
8

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 8
8