
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 精準(zhǔn)藥物
精準(zhǔn)藥物  2024-09-19
2024-09-19
 172
172
2024年9月17日花盐,亞盛醫(yī)藥股票暴漲7%拆鹉,市值達(dá)到112.9億港幣孟辑,創(chuàng)近2年新高候赏。近期翔悠,亞盛醫(yī)藥披露了其唯一上市產(chǎn)品奧雷巴替尼的新進(jìn)展:近日在2024年歐洲腫瘤內(nèi)科學(xué)會(huì)(ESMO)年會(huì)上番宁,以小型口頭報(bào)告形式公布公司原創(chuàng)1類新藥奧雷巴替尼(GZD824, HQP1351)治療琥珀酸脫氫酶(SDH)缺陷型胃腸間質(zhì)瘤(GIST)的臨床研究成果。奧雷巴替尼在SDH缺陷型GIST中顯示出了持續(xù)的臨床療效氮昧,并為這種罕見疾病的未來研究提供了基準(zhǔn)框杜。MOA研究顯示,奧雷巴替尼通過調(diào)節(jié)參與血管生成袖肥、凋亡咪辱、增殖和存活等多種信號(hào)通路來發(fā)揮抗腫瘤活性。
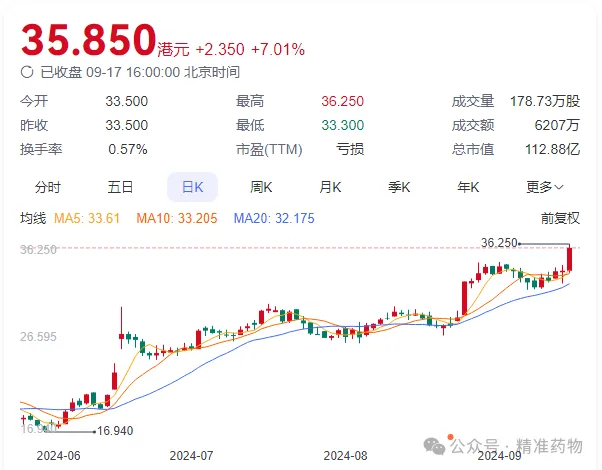
奧雷巴替尼是公司唯一上市產(chǎn)品椎组,奧雷巴替尼是一款口服第三代BCR-ABL抑制劑梧乘,目前已有兩項(xiàng)適應(yīng)癥獲批上市,分別為:1)治療任何TKI耐藥庐杨、并伴有T315I突變的慢性髓細(xì)胞白血惭〉鳌(CML)慢性期(-CP)和加速期(-AP)的成年患者;2)治療對(duì)一代和二代TKI耐藥和/或不耐受的CML-CP成年患者律愉。
據(jù)2024年8月份亞盛醫(yī)藥發(fā)布的公告顯示臭呀,報(bào)告期內(nèi),亞盛醫(yī)藥收入創(chuàng)新高俘巡,實(shí)現(xiàn)收入人民幣8.24億元聊树,較去年同比增長477%,主要來源于產(chǎn)品銷售收入和對(duì)外合作授權(quán)收入等变抛。公司首次實(shí)現(xiàn)扭虧為盈峦筏,凈利潤達(dá)人民幣1.63億元。報(bào)告期內(nèi):
奧雷巴替尼(GZD824,HQP1351)實(shí)現(xiàn)銷售收入人民幣1.13億元涡拾,較去年下半年環(huán)比增長120%蒂鹏,較去年上半年同比增長5%。
與跨國制藥企業(yè)武田就奧雷巴替尼(GZD824,HQP1351)簽署了一項(xiàng)獨(dú)家選擇權(quán)協(xié)議胆褪。該合作總交易額達(dá)人民幣93.6億元艳禁,包含7.2億元的選擇權(quán)付款,和共計(jì)86.4億元的選擇權(quán)行使費(fèi)及額外的潛在里程碑付款狰绪。同時(shí)叮廉,公司還將獲得基于年度銷售額雙位數(shù)的遞增銷售分成。截至目前棍鳖,此項(xiàng)合作為國內(nèi)小分子腫瘤藥領(lǐng)域的最大的對(duì)外權(quán)益許可炮叶。此外,亞盛醫(yī)藥還獲得武田的股權(quán)投資渡处。該合作充分彰顯了耐立克?在全球的臨床和商業(yè)化價(jià)值镜悉,也為其將來的全球商業(yè)化進(jìn)程奠定了基石。目前,亞盛醫(yī)藥已收到武田人民幣7.2億元的選擇權(quán)付款和人民幣5.4億元的股權(quán)投資款項(xiàng)积瞒。
截至2024年6月30日,奧雷巴替尼(GZD824,HQP1351)的全國準(zhǔn)入醫(yī)院和DTP藥房共達(dá)到670家登下,其中準(zhǔn)入醫(yī)院數(shù)量較去年底增長達(dá)79%茫孔。繼去年11月新適應(yīng)癥獲批至今年6月30日,耐立克?已獲20個(gè)省83個(gè)城市114個(gè)項(xiàng)目的重特大疾病補(bǔ)充保險(xiǎn)或惠民保報(bào)銷被芳。
2024年1月缰贝,該藥物獲納入美國國家綜合癌癥網(wǎng)絡(luò)(NCCN)慢性髓細(xì)胞白血病(CML)治療指南畔濒;此外剩晴,奧雷巴替尼(GZD824,HQP1351)于報(bào)告期內(nèi)獲2024 CSCO惡性血液病診療指南升級(jí)推薦,涉及CML恬皆、費(fèi)城染色體陽性急性淋巴細(xì)胞白血才樯(Ph+ ALL)領(lǐng)域的治療,并新增多項(xiàng)I級(jí)推薦众附。
今年7月沉南,奧雷巴替尼(GZD824,HQP1351)在中國澳門獲批上市,獲批的適應(yīng)癥分別為治療任何酪氨酸激酶抑制劑(TKI)耐藥刮跟、并伴有T315I突變的CML慢性期(-CP)和加速期(-AP)的成年患者劣晾;以及治療對(duì)一代和二代TKI耐藥和/或不耐受的CML-CP成年患者。這是該藥物繼在中國內(nèi)地獲批上市后的又一重大里程碑唬垦。
奧雷巴替尼(GZD824)研發(fā)歷程
2008年莫诺,中國科學(xué)院廣州生物醫(yī)藥與健康研究院丁克團(tuán)隊(duì)立項(xiàng)三代ABL抑制劑研發(fā)項(xiàng)目。
2011年1月9日些吨,中國科學(xué)院廣州生物醫(yī)藥與健康研究院組建的艾比克創(chuàng)業(yè)團(tuán)隊(duì)(王德平畸玲、張章等)的"抗白血病1類新藥DP605(即GZD824)的臨床前研究項(xiàng)目"獲得中科院第四界青年創(chuàng)業(yè)大賽唯一金獎(jiǎng);
2013年3月21日林葬,中國科學(xué)院廣州生物醫(yī)藥與健康研究院官網(wǎng)披露了GZD824的臨床前數(shù)據(jù):
中科院廣州生物醫(yī)藥與健康研究院丁克博士帶領(lǐng)團(tuán)隊(duì)經(jīng)過近4年的技術(shù)攻關(guān)饰吕,成功設(shè)計(jì)和合成了芳基炔類和三氮唑苯甲酰胺兩類Bcr-Abl小分子抑制劑「粜模化合物在多種激酶白群、細(xì)胞和動(dòng)物模型中可有效克服Bcr-AblT315I突變誘發(fā)的耐藥問題。
化合物GZD824可以以pM的IC50值抑制Bcr-AblWT及Bcr-AblT315I等耐藥突變體的激酶活性(分別為0.34和0.68 nM)硬霍,并對(duì)P-loop區(qū)突變(E255K/V)等有效帜慢。化合物在多種細(xì)胞和動(dòng)物模型中表現(xiàn)出優(yōu)異抗腫瘤活性(針對(duì)K562唯卖,Ku812等CML腫瘤細(xì)胞的IC50為0.2~10 nM粱玲;針對(duì)攜帶Bcr-AblT315I 突變體的Ba/F3細(xì)胞的IC50約為7 nM;在1.0-20.0 mg/kg/day 的口服劑量下完全抑制腫瘤生長)和較好的安全性指標(biāo)及優(yōu)異的藥代動(dòng)力學(xué)性質(zhì)(大鼠口服生物利用度約為48.7%;體內(nèi)半衰期T1/2約為8-10小時(shí))抽减。
目前允青,GZD824已被確定為候選藥物,正在進(jìn)行規(guī)范的臨床前評(píng)價(jià)卵沉。以該項(xiàng)目為基礎(chǔ)颠锉,研究團(tuán)隊(duì)還獲得2011年“第四屆中國科學(xué)院青年創(chuàng)業(yè)大賽”金獎(jiǎng)。
該項(xiàng)研究獲得國家新藥創(chuàng)制重大專項(xiàng)史汗、廣東省新藥創(chuàng)制重大專項(xiàng)足贴、廣州市重大專項(xiàng)以及中科院交叉團(tuán)隊(duì)項(xiàng)目等資助。部分結(jié)果已在藥物化學(xué)期刊J. Med. Chem. 發(fā)表[J. Med. Chem. 2013, 56(3), 879-894姥勤;J. Med. Chem. 2012, 55 (22), 10033-10046]哮寨。
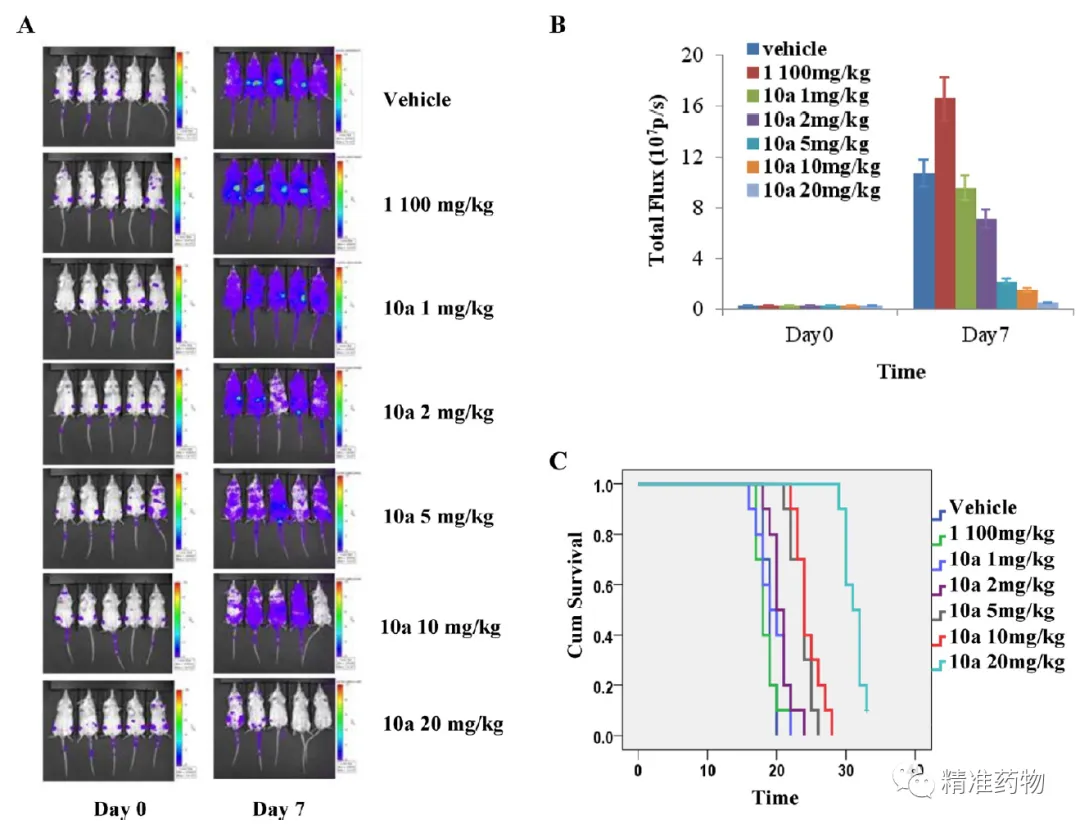
HQP1351(GZD824,10a)體內(nèi)克服T315I耐藥(來源:JMC, 2013, 56(3):879-894.)
2013年,GZD824轉(zhuǎn)讓給廣州順健生物醫(yī)藥科技有限公司施俩,更名為HQP1351進(jìn)行后期開發(fā)瞎遗。
2015年4月,亞盛向CFDA提交HQP1351用于治療耐藥性CML患者的IND披蛔。
2016年 2月悦浙,HQP1351獲得臨床批準(zhǔn),并于當(dāng)年啟動(dòng)I期臨床試驗(yàn)嗤雪。
2018年8月挟七,亞盛向CDE匯報(bào)了I期結(jié)果,并積極溝通Ⅱ期方案妥析。
2018年12月相贺,HQP1351的Ⅱ期臨床方案獲得通過,并獲準(zhǔn)在完成Ⅱ期試驗(yàn)后即可提交新藥上市申請(qǐng)(NDA)省咨。
2019年8月肃弟,完成治療AP-CML患者的臨床試驗(yàn)的招募;9月零蓉,啟動(dòng)CP-CML的招募(招股書信息)笤受。
2018年12月3日,江倩教授在2018 ASH會(huì)場(chǎng)口頭報(bào)告了HQP1351的中國I臨床臨床研究進(jìn)展:
HQP1351治療對(duì)TKI耐藥的CML患者的Ⅰ期臨床試驗(yàn)在中國開展敌蜂,共入組11個(gè)劑量組(1mg遞增到60mg)箩兽;
截止到2018年10月底,該項(xiàng)研究共入組100例CML患者(86例CP患者, 14例AP患者)章喉;
HQP1351在除60mg劑量組外的所有劑量組均耐受良好汗贫。沒有患者因?yàn)橹委熛嚓P(guān)的不良事件(TRAEs)而退出研究。
60mg劑量組的3例患者中2例出現(xiàn)劑量限制毒性(DLT)秸脱,50mg 被認(rèn)為是最大耐受劑量(MTD)落包;在可評(píng)估病例中,CP病人完全血液學(xué)緩解(CHR)率為96%,AP病人CHR率為85%咐蝇;
在66例可評(píng)估CP病例中涯鲁,主要細(xì)胞遺傳學(xué)緩解(MCyR)率為67%。特別是在帶有T315I突變的CP病例中法雄,MCyR率高達(dá)78%用兵。
2019年5月27日,亞盛醫(yī)藥招股書披露了HQP1351的I期臨床研究數(shù)據(jù)(101 名患者當(dāng)中有92 人仍然在接受治療袁朗,最長治療期限為31個(gè)月):
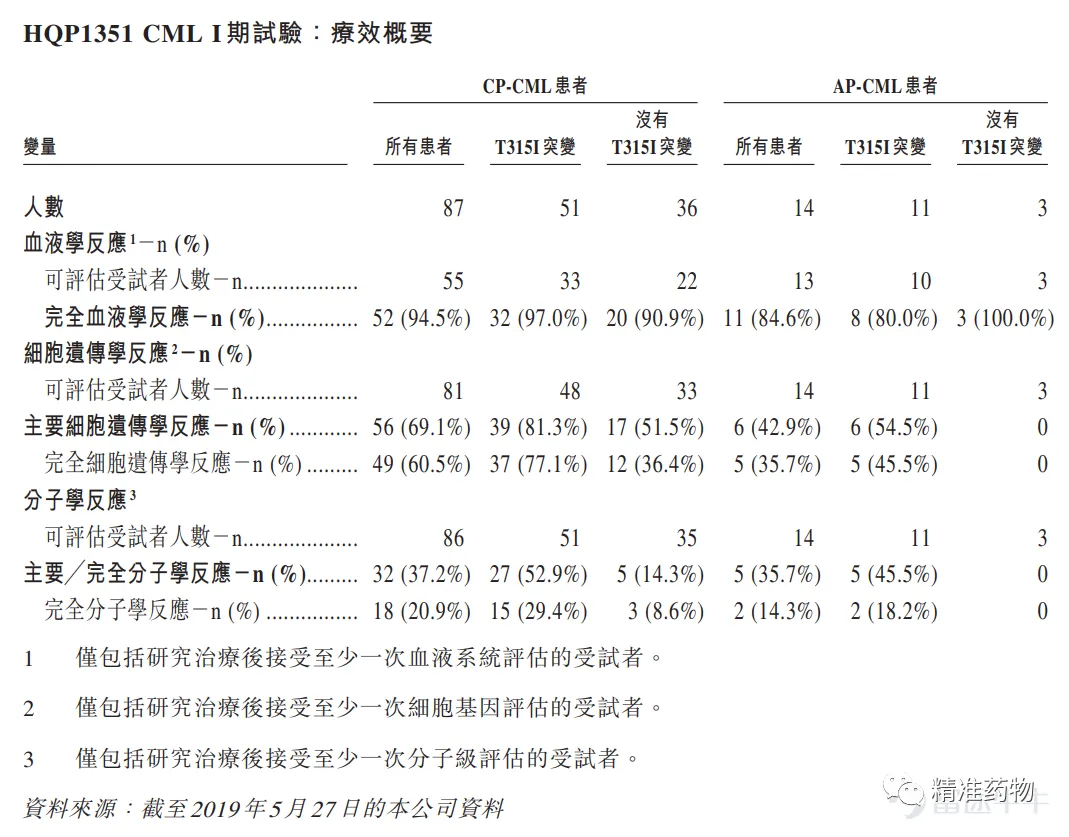
亞盛醫(yī)藥招股書資料
2019年7月22日,亞盛醫(yī)藥宣布叶偶,HQP1351獲準(zhǔn)在美國進(jìn)行臨床Ib試驗(yàn)跃渠,用于治療針對(duì)TKI(酪氨酸激酶抑制劑)耐藥的慢性髓性白血病(CML)锯运。
2019年12月11日沛四,亞盛醫(yī)藥宣布,該項(xiàng)臨床研究的主要研究者蛔颖、北京大學(xué)人民醫(yī)院血液科副主任江倩教授為報(bào)告人在第61屆美國血液學(xué)會(huì)(American Society of Hematology糊晋,ASH)年會(huì)上再次以口頭報(bào)告的形式公布了HQP1351的I期臨床進(jìn)展數(shù)據(jù),該研究獲得本屆ASH年會(huì)“最佳研究”(Best of ASH)提名政拾。數(shù)據(jù)顯示:
HQP1351針對(duì)TKI耐藥的CML慢性期(CP)或加速期(AP)患者的I 期臨床試驗(yàn)在中國開展际器,共入組11個(gè)劑量組(1mg遞增到60mg),最終確定60mg QOD為劑量限制性毒性(DLT)劑量贸桶, 50mg QOD為最大耐受劑量(MTD)舅逸,40mg QOD為II期臨床推薦用藥量(RP2D)。
截止到2019年5月27日皇筛,該項(xiàng)研究共入組101例CML患者(87例CP患者, 14例AP患者),中位隨訪時(shí)間為12.8個(gè)月(1.2~31.5)琉历。CP患者的18個(gè)月無進(jìn)展生存率(PFS)為94%,AP患者為61%水醋。
HQP1351在除60mg劑量組外的所有劑量組均耐受良好旗笔。治療相關(guān)不良反應(yīng)(TRAE)中,大多數(shù)非血液學(xué)不良反應(yīng)是1級(jí)或2級(jí)拄踪,最常見的3級(jí)/4級(jí)血液學(xué)TRAE是血小板減少(50%)蝇恶。TRAE 的發(fā)生率隨治療時(shí)間延長而降低。沒有治療相關(guān)性死亡或5級(jí)不良事件發(fā)生惶桐。
HQP1351對(duì)CML患者顯示出有效的抗白血病活性艘包,治療患者獲得了較高的反應(yīng)率。且隨著治療時(shí)間的延長耀盗,緩解率和緩解深度都會(huì)增加想虎。所有可評(píng)估患者中,CP患者的完全血液學(xué)緩解(CHR)率為95%, AP患者的CHR率為85%桶悍。
在95例可評(píng)估的基線非完全遺傳學(xué)緩解(non-CCyR)患者中乐跺,CP患者主要細(xì)胞遺傳學(xué)反應(yīng)(MCyR)率為69%,其中61%獲得了完全細(xì)胞遺傳學(xué)反應(yīng)(CCyR)讼逐;AP患者M(jìn)CyR率為43%症忽,其中36%獲得CCyR。
可評(píng)估患者中凸翩,37%的CP患者和36%的AP患者達(dá)到主要分子生物學(xué)緩解(MMR)牙晰。
在伴有高度耐藥的T315I突變的患者中,HQP1351顯示了卓越的療效肪麦。在CP伴有T315I的患者中较谣,MCyR率達(dá)到了82%,其中CCyR率高達(dá)78%孩最。
2019年12月公開信息顯示趾赡,HQP1351已在中國啟動(dòng)針對(duì)GIST患者的Ib期臨床試驗(yàn)。同時(shí)在美國的臨床Ib期研究也已啟動(dòng)眯找。
2020年5月4日好勤,亞盛醫(yī)藥宣布,美國食品和藥品監(jiān)督管理局(FDA)已授予公司核心在研品種HQP1351孤兒藥資格認(rèn)定啼染,用于治療慢性髓性白血惭绾稀(CML)。
2020年5月7日迹鹅,亞盛醫(yī)藥5月7日宣布形纺,美國食品和藥品監(jiān)督管理局(FDA)已授予公司核心在研品種HQP1351快速通道資格(FTD),用于治療對(duì)現(xiàn)有酪氨酸激酶抑制劑(TKI)治療失敗的特定基因突變的慢性髓性白血餐叫馈(CML)患者逐样。
2020年6月18日,亞盛醫(yī)藥宣布已經(jīng)向NMPA提交HQP1351的上市申請(qǐng)打肝。
2020年9 月 29 日脂新,亞盛藥業(yè)首次對(duì)外公布HQP1351的中文通用名為奧瑞巴替尼片。
2020年10月21日粗梭,亞盛醫(yī)藥宣布争便,該公司全資子公司順健生物的1類新藥奧瑞巴替尼片(HQP1351的擬定中文通用名)已正式被中國家藥品監(jiān)督管理局新藥審評(píng)中心(CDE)納入優(yōu)先審評(píng)。
2021年11月12日断医,NMPA官網(wǎng)公示滞乙,奧瑞巴替尼(GZD824,HQP1351)新藥上市申請(qǐng)的審評(píng)審批狀態(tài)已更新為“在審批“葡谅。
2021年11月25日脱处,NMPA批準(zhǔn)奧雷巴替尼(GZD824卸能,HQP1351)上市申請(qǐng)。
2023年11月17日忍抗,亞盛醫(yī)藥宣布奧雷巴替尼片(GZD824延坡,HQP1351)用于對(duì)一代和二代酪氨酸激酶抑制劑(TKI)耐藥和/或不耐受的慢性髓細(xì)胞白血病慢性期(CML-CP)成年患者的適應(yīng)癥獲得了國家藥品監(jiān)督管理局(NMPA)批準(zhǔn)。
2024年1月付厦,奧雷巴替尼(GZD824舵博,HQP1351)獲納入美國國家綜合癌癥網(wǎng)絡(luò)(NCCN)慢性髓細(xì)胞白血病(CML)治療指南超默;
2024年蟆盖,奧雷巴替尼(GZD824,HQP1351)獲2024 CSCO惡性血液病診療指南升級(jí)推薦园环,涉及CML多梦、費(fèi)城染色體陽性急性淋巴細(xì)胞白血病(Ph+ ALL)領(lǐng)域的治療韭寸,并新增多項(xiàng)I級(jí)推薦春哨。
2024年6月11日荆隘,亞盛醫(yī)藥宣布奧雷巴替尼的新適應(yīng)癥臨床試驗(yàn)申請(qǐng)獲得中國國家藥監(jiān)局藥品審評(píng)中心(CDE)批準(zhǔn)恩伺,該公司將開展一項(xiàng)全球注冊(cè)3期臨床研究,評(píng)估奧雷巴替尼治療系統(tǒng)性全身治療失敗的琥珀酸脫氫酶(SDH)缺陷型胃腸間質(zhì)瘤(GIST)患者的效果椰拒。
2024年6月14日晶渠,亞盛醫(yī)藥宣布與武田就耐立克(奧雷巴替尼)簽署了一項(xiàng)獨(dú)家選擇權(quán)協(xié)議。一旦選擇權(quán)被行使燃观,武田將獲得開發(fā)及商業(yè)化奧雷巴替尼的全球權(quán)利許可褒脯,惟中國大陸、中國香港特別行政區(qū)缆毁、中國澳門特別行政區(qū)番川、中國臺(tái)灣等地區(qū)除外。在協(xié)議簽署后脊框,亞盛醫(yī)藥將收到1億美元的選擇權(quán)付款颁督,并有資格獲得最高約12億美元的選擇權(quán)行使費(fèi)和額外的潛在里程碑付款,以及基于年度銷售額提成的雙位數(shù)比例特許權(quán)使用費(fèi)浇雹。此外沉御,武田制藥將購買亞盛醫(yī)藥的少數(shù)股權(quán)。
2024年7月2日依筝,亞盛醫(yī)藥宣布芋甸,已于2024年7月2日收到武田支付的選擇權(quán)付款1億美元;此前亞盛制藥收到武田制藥7500萬美元股權(quán)投資款項(xiàng)剪莲。
2024年7月8日谬咽,奧雷巴替尼(GZD824叙傅,HQP1351)正式獲中國澳門特別行政區(qū)藥物監(jiān)督管理局(ISAF)批準(zhǔn)上市;適應(yīng)癥包括治療任何酪氨酸激酶抑制劑(TKI)耐藥污兄、并伴有 T315I 突變的慢性髓細(xì)胞白血灿ヅ荨(CML)慢性期(-CP)和加速期(-AP)的成年患者;以及治療對(duì)一代和二代 TKI 耐藥和/或不耐受的 CML-CP 成年患者午四。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 識(shí)林
識(shí)林  2024-11-26
2024-11-26
 2
2

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 賽柏藍(lán)
賽柏藍(lán)  2024-11-26
2024-11-26
 2
2

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 村夫日記LatitudeHealth
村夫日記LatitudeHealth  2024-11-26
2024-11-26
 2
2
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽