
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 藥融圈
藥融圈  2024-09-19
2024-09-19
 184
184
新藥獲批“續(xù)寫”諾獎(jiǎng)
2009年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)授予了三位科學(xué)家Elizabeth H. Blackburn、Carol W. Greider和Jack Szostak博士锉罐,以表彰他們“發(fā)現(xiàn)端粒和端粒酶是如何保護(hù)染色體的”能耻。

截圖自The Nobel Prize
端粒是位于染色體末端的脫氧核糖核酸(DNA)重復(fù)序列赏枚,其研究可以追溯到20世紀(jì)70年代,它們作為“保護(hù)帽”晓猛,以保持染色體的穩(wěn)定性和完整性饿幅,由于細(xì)胞每分裂一次,端粒就會(huì)縮短一次戒职,當(dāng)端晾醵鳎縮短到極短長(zhǎng)度時(shí),細(xì)胞要么死于細(xì)胞凋亡洪燥,要么停止分裂和衰老磕秤。因此大多數(shù)細(xì)胞分裂次數(shù)有限,且分裂次數(shù)受端粒長(zhǎng)度的調(diào)節(jié)捧韵,端粒也被科學(xué)家稱作“生命時(shí)鐘”景姓。
端粒酶在1984年被發(fā)現(xiàn),這是一種天然產(chǎn)生的酶社衰,能夠維持端粒長(zhǎng)度瘫盹,防止它們?cè)诩?xì)胞(例如干細(xì)胞)分裂時(shí)縮短,以維持正常的人體健康桃旷。端粒酶至少由兩個(gè)部分組成:一個(gè)核糖核酸(RNA)模板也较,可與端粒結(jié)合;以及一個(gè)具有逆轉(zhuǎn)錄酶活性的催化亞基薯舆,可在染色體末端添加一個(gè)特定的DNA序列晚乙。
藥融云數(shù)據(jù)www.pharnexcloud.com顯示:2024年6月6日,美國(guó)生物制藥公司Geron Corporation(杰龍)宣布其開(kāi)發(fā)的First-in-Class端粒酶抑制劑RYTELO(Imetelstat)獲得FDA批準(zhǔn)用于治療低至中度-1風(fēng)險(xiǎn)骨髓增生異常綜合征(MDS)成年患者的輸血依賴性(TD)貧血累冠,這些患者在8周內(nèi)需要輸入四個(gè)或更多的紅細(xì)胞單位缘违,且對(duì)紅細(xì)胞生成刺激劑(ESA)無(wú)反應(yīng)或已經(jīng)耐藥或不適合使用ESA。
據(jù)了解蝇罐,RYTELO(Imetelstat)是全球首款獲批上市的端粒酶抑制劑谣皇,該藥物曾被Evaluate Pharma評(píng)為2024年有望上市的10款全球重磅藥物之一,另?yè)?jù)藥融咨詢報(bào)道拔调,Imetelstat年銷售額峰值或可達(dá)20億美元。
2023年9月猜谚,Geron Corporation在歐洲為RYTELO(Imetelstat)遞交了一份上市許可申請(qǐng)败砂,適應(yīng)癥與美國(guó)相同,預(yù)計(jì)監(jiān)管審查將在2025年初完成魏铅,該公司計(jì)劃在2025年最終確定該藥在歐洲的商業(yè)化戰(zhàn)略昌犹,可能包括自主商業(yè)化或潛在的伙伴關(guān)系坚芜。
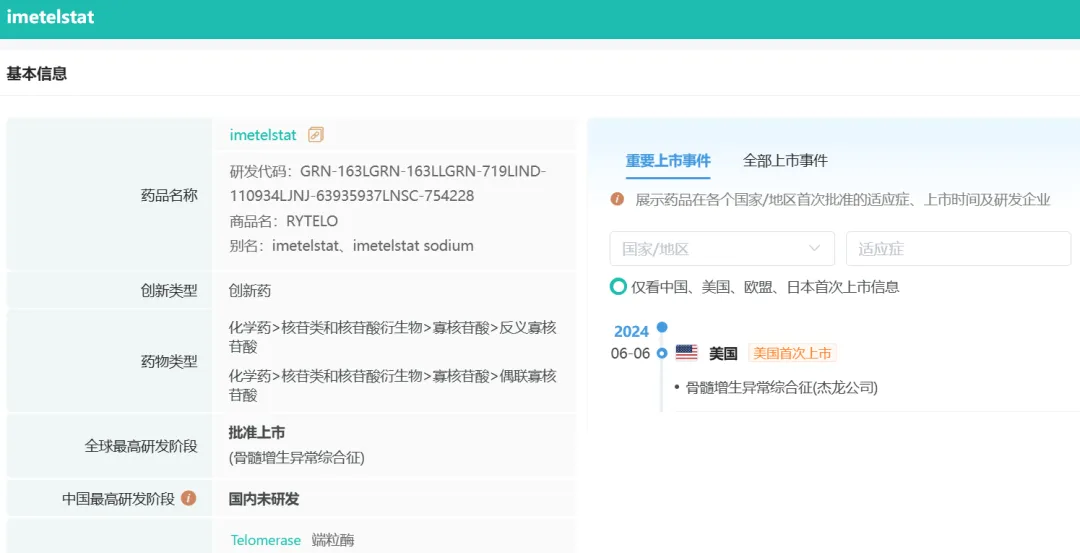
截圖自藥融云數(shù)據(jù)庫(kù)
20年曲折開(kāi)發(fā)歷程
Geron Corporation由干細(xì)胞、細(xì)胞衰老和端粒酶研究的先驅(qū)Michael West和當(dāng)時(shí)Kleiner Perkins Caufield& Byers的合伙人斜姥,知名風(fēng)險(xiǎn)投資家Alex Barkas在1990年創(chuàng)立鸿竖。1996年,Geron成為了一家上市公司(Nasdaq: GERN)铸敏,前文提到的三位諾獎(jiǎng)科學(xué)家缚忧,以及美國(guó)知名生物學(xué)家Leonard Hayflick(他提出了“海夫利克極限”)均是該公司當(dāng)時(shí)的科學(xué)顧問(wèn)。2003年杈笔,Geron公司開(kāi)發(fā)了與端粒酶的RNA模板結(jié)合并競(jìng)爭(zhēng)性抑制端粒酶活性的寡核苷酸闪水,2005年Geron通過(guò)使用脂質(zhì)修飾增強(qiáng)了這一端粒酶抑制劑的效力,Imetelstat由此誕生蒙具,因此該藥物本質(zhì)是一種脂質(zhì)偶聯(lián)的13-mer寡核苷酸嬉哥。20年新藥創(chuàng)制,30余年創(chuàng)業(yè)新藥公司終于成就一款新藥勒蜀。
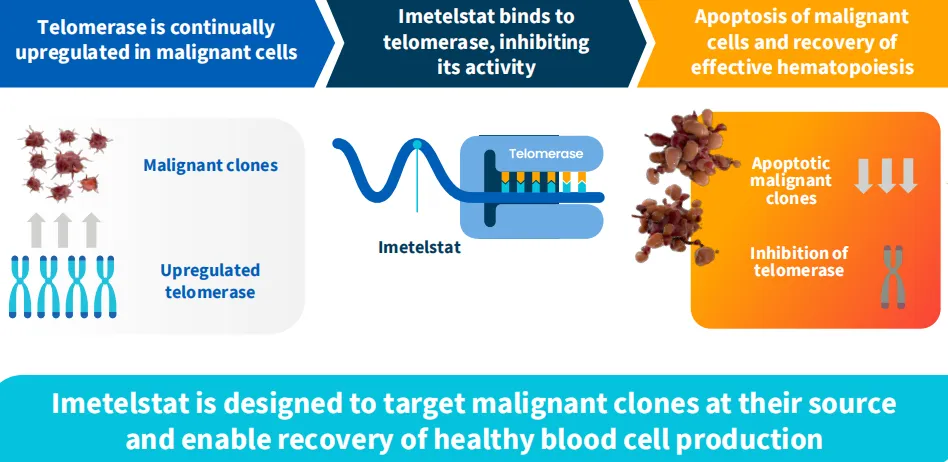
不過(guò)Imetelstat的開(kāi)發(fā)歷經(jīng)曲折津咒,該藥物最早曾針對(duì)非小細(xì)胞肺癌、膠質(zhì)瘤等開(kāi)展過(guò)臨床試驗(yàn)雁碘,但均以失敗告終哩拔,Geron公司便將重點(diǎn)放在血液系統(tǒng)腫瘤。2014年驴涡,該公司與強(qiáng)生旗下楊森制藥就Imetelstat達(dá)成了全球戰(zhàn)略合作肯坊,共同推進(jìn)開(kāi)發(fā)和商業(yè)化工作,該交易總額高達(dá)9.35億美金觅符。合作期間诉拔,Imetelstat針對(duì)骨髓增生異常綜合征(MDS)和骨髓纖維化(MF)分別開(kāi)展了2期研究,但是兩項(xiàng)研究的結(jié)果并未達(dá)到強(qiáng)生的預(yù)期深吠,雙方遂于2018年終止了合作增厢。
2019年,Geron公司推進(jìn)了Imetelstat治療低風(fēng)險(xiǎn)骨髓增生異常綜合征(MDS)的IMerge 3期臨床試驗(yàn)桑孩。MDS是最常見(jiàn)的髓系惡性腫瘤拜鹤,在臨床上常以嚴(yán)重貧血、低紅細(xì)胞計(jì)數(shù)流椒、血紅蛋白低為特征敏簿,多達(dá)30%的MDS病例會(huì)轉(zhuǎn)化為AML(急性髓系白血病)宣虾。據(jù)統(tǒng)計(jì)惯裕,美國(guó)約有6萬(wàn)人患有該病,每年約有1.6萬(wàn)例MDS新發(fā)病例绣硝。其中蜻势,慢性貧血是低風(fēng)險(xiǎn)MDS患者的主要臨床問(wèn)題撑刺,雖然紅細(xì)胞生成刺激劑(ESA)可以改善約50%的患者的貧血,但其效果是短暫的握玛,中位反應(yīng)持續(xù)時(shí)間約為兩年够傍。
2023年1月,Geron報(bào)告了IMerge關(guān)鍵3期臨床試驗(yàn)的積極頂線結(jié)果挠铲,該試驗(yàn)評(píng)估了Imetelstat在TD LR-MDS(輸血依賴型低風(fēng)險(xiǎn)骨髓增生異常綜合征)患者中的療效冕屯,研究結(jié)果于2023年12月刊登于《柳葉刀》。此次美國(guó)FDA批準(zhǔn)RYTELO(Imetelstat)以及該藥在歐洲的遞交都是基于這項(xiàng)研究檐射。

截圖自The Lancet
這項(xiàng)關(guān)鍵3期臨床試驗(yàn)達(dá)到了至少8周不依賴紅細(xì)胞輸血(RBC-TI)的主要終點(diǎn)和至少24周不依賴紅細(xì)胞輸血(RBC-TI)的關(guān)鍵次要終點(diǎn)铜那,證明了Imetelstat與安慰劑相比具有高度統(tǒng)計(jì)學(xué)意義和臨床意義的益處,具體而言洪防,Imetelstat組患者8周RBC-TI為39.8%杉抑,而安慰劑組為15%;Imetelstat組患者24周RBC-TI為28%沛摩,安慰劑組為3.3%在搀。
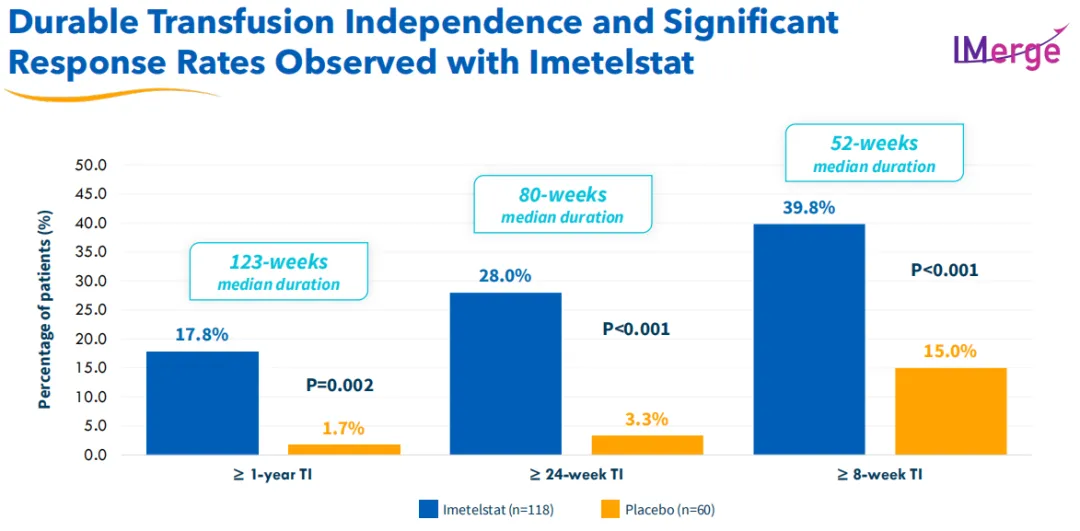
此外,該試驗(yàn)在關(guān)鍵MDS患者亞型中觀察到了具有統(tǒng)計(jì)學(xué)意義和臨床意義的療效結(jié)果帽遏,包括環(huán)狀鐵粒幼紅細(xì)胞陽(yáng)性(RS陽(yáng)性)和環(huán)狀鐵粒幼紅細(xì)胞陰性(RS陰性)的患者搓纠、基線輸血負(fù)擔(dān)高(4-6紅細(xì)胞單位/8周)和非常高的(>6紅細(xì)胞單位/8周)的患者,以及根據(jù)國(guó)際預(yù)后評(píng)分系統(tǒng)(IPSS分類)為低或中-1風(fēng)險(xiǎn)的患者祷鼎。
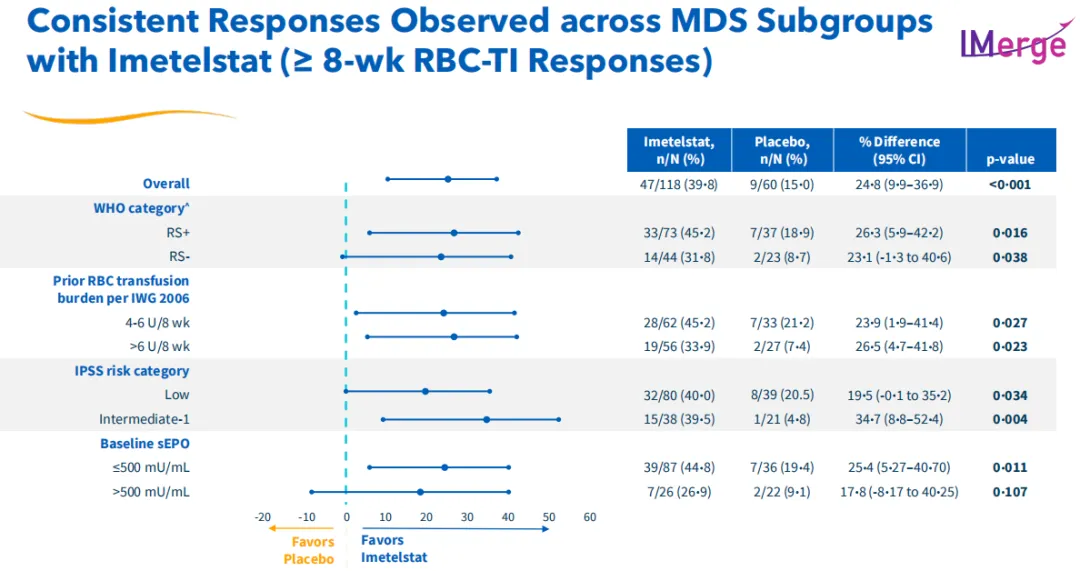
安全性結(jié)果與先前的Imetelstat臨床試驗(yàn)一致世雄,最常見(jiàn)的3/4級(jí)不良反應(yīng)是中性粒細(xì)胞減少癥(72%)和血小板減少癥(65%),其中位持續(xù)時(shí)間不到2周映僚,超過(guò)80%的患者在4周內(nèi)控制為2級(jí)以下寞竭。
2024年3月14日,美國(guó)FDA就Imetelstat根據(jù)IMerge 3期臨床試驗(yàn)的結(jié)果召開(kāi)腫瘤藥物咨詢委員會(huì)(ODAC)會(huì)議酣难,最終委員會(huì)以12:2的投票結(jié)果贊成Imetelstat的臨床益處大于風(fēng)險(xiǎn)谍夭,消息公布次日,Geron公司股價(jià)暴漲92%憨募。6月6日紧索,RYTELO(Imetelstat)成功獲批,比此前設(shè)定的PDUFA日期提早了10天菜谣。
2024年7月26日珠漂,Geron公司宣布美國(guó)國(guó)家綜合癌癥網(wǎng)絡(luò)(NCCN)更新了骨髓增生異常綜合征(MDS)的腫瘤學(xué)臨床實(shí)踐指南(NCCN指南),推薦RYTELO(Imetelstat)作為低風(fēng)險(xiǎn)MDS患者繼發(fā)性貧血的1類和2A類治療方案尾膊。
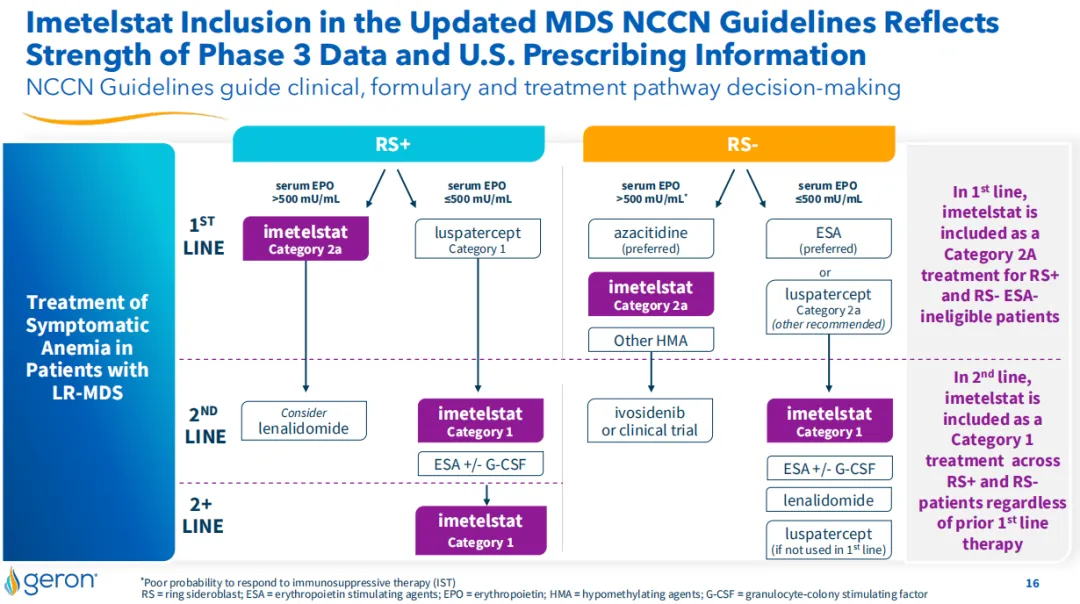
探索多種血液瘤甘磨、聯(lián)合療法
除了低風(fēng)險(xiǎn)骨髓增生異常綜合征(MDS),Geron公司正在開(kāi)發(fā)Imetelstat用于治療其他髓系血液系統(tǒng)惡性腫瘤。
骨髓纖維化(MF)是一種骨髓增生性腫瘤济舆,據(jù)統(tǒng)計(jì),美國(guó)約有1.3萬(wàn)名MF患者莺债,每年報(bào)告約3000名新發(fā)病例滋觉,約有70%的患者被歸為中-2風(fēng)險(xiǎn)或高風(fēng)險(xiǎn),對(duì)于JAK抑制劑治療無(wú)效或耐藥的患者讼石,尚無(wú)藥物獲批用于后續(xù)治療苇赊,因此存在顯著的未滿足醫(yī)療需求。
該公司開(kāi)展的IMpactMF3期臨床試驗(yàn)正在評(píng)估Imetelstat治療中-2風(fēng)險(xiǎn)或高風(fēng)險(xiǎn)骨髓纖維化(MF)患者回乞,這些患者接受JAK抑制劑治療后復(fù)發(fā)或?qū)AK抑制劑耐藥忠辛,稱為復(fù)發(fā)/難治性MF患者,該研究以總生存期(OS)作為主要終點(diǎn)夹恨。2024年8月哎闻,該試驗(yàn)完成約70%患者入組,基于目前對(duì)試驗(yàn)中入組和事件(死亡率)的計(jì)劃假設(shè)闰芒,該公司預(yù)計(jì)IMpactMF研究的OS中期分析可能在2026年初進(jìn)行枚林,最終分析可能在2027年初進(jìn)行。
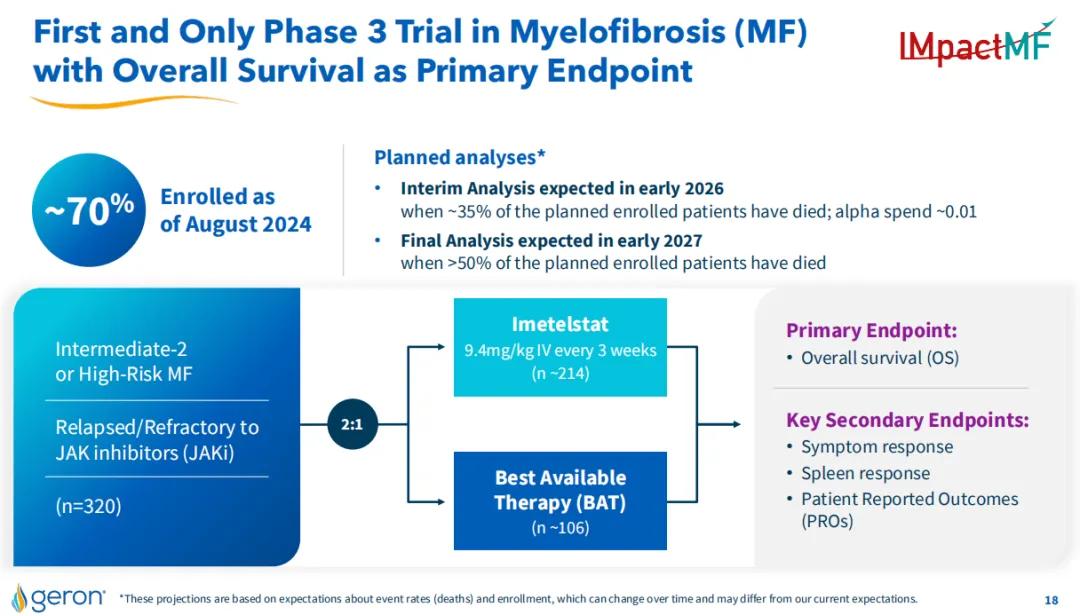
Geron公司還在開(kāi)展一項(xiàng)名為IMproveMF的1期臨床試驗(yàn)墓运,旨在研究Imetelstat與蘆可替尼作為聯(lián)合療法郭菜,用于一線治療中-1風(fēng)險(xiǎn)、中-2風(fēng)險(xiǎn)或高風(fēng)險(xiǎn)的骨髓纖維化(MF)鞍歌,目前該研究正在招募患者勘伺。
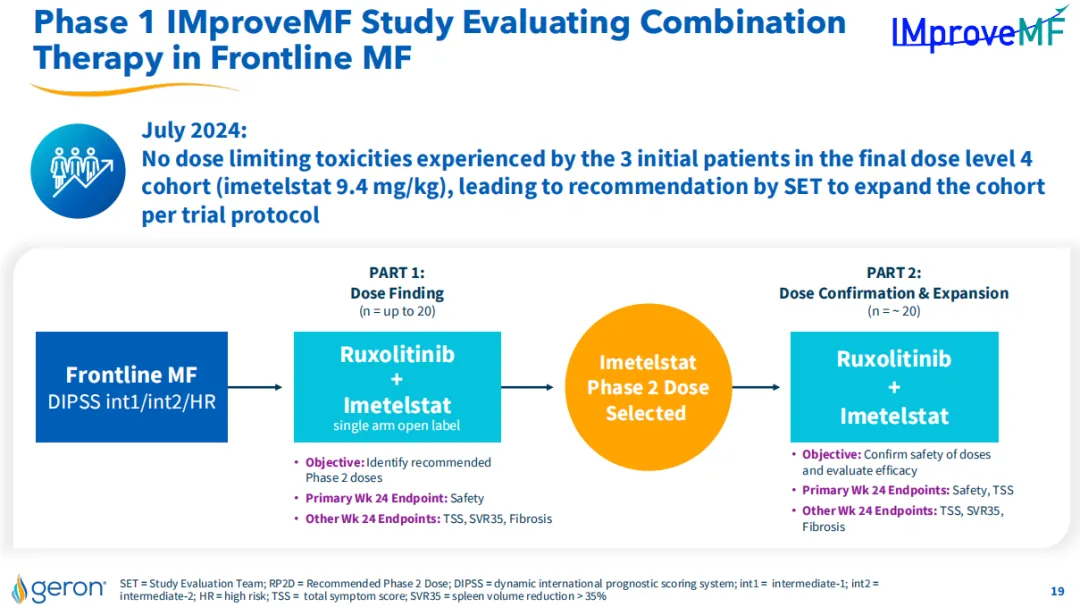
由研究者發(fā)起的IMpress2期臨床試驗(yàn),旨在研究Imetelstat用于治療高風(fēng)險(xiǎn)骨髓增生異常綜合征(MDS)褂删,和復(fù)發(fā)/難治性急性髓系白血病(AML)飞醉,這些患者先前接受過(guò)低甲基化劑(HMA)治療,研究已在2023年6月完成首例患者給藥笤妙。
另外冒掌,Geron公司計(jì)劃在IMpress研究結(jié)果公布之前支持一項(xiàng)由研究者發(fā)起的,名為TELOMERE的1/2期試驗(yàn)蹲盘,旨在研究Imetelstat與維奈克拉或阿扎胞苷作為聯(lián)合療法股毫,治療復(fù)發(fā)/難治性(AML)患者。
對(duì)于臨床前研究召衔,Geron公司正與MD安德森癌癥中心合作铃诬,計(jì)劃開(kāi)展臨床前研究,以評(píng)估Imetelstat在淋巴細(xì)胞惡性腫瘤中的潛在治療效果苍凛。除此之外趣席,該公司也啟動(dòng)了一個(gè)藥物發(fā)現(xiàn)項(xiàng)目,以確定潛在下一代口服端粒酶抑制劑的先導(dǎo)化合物。
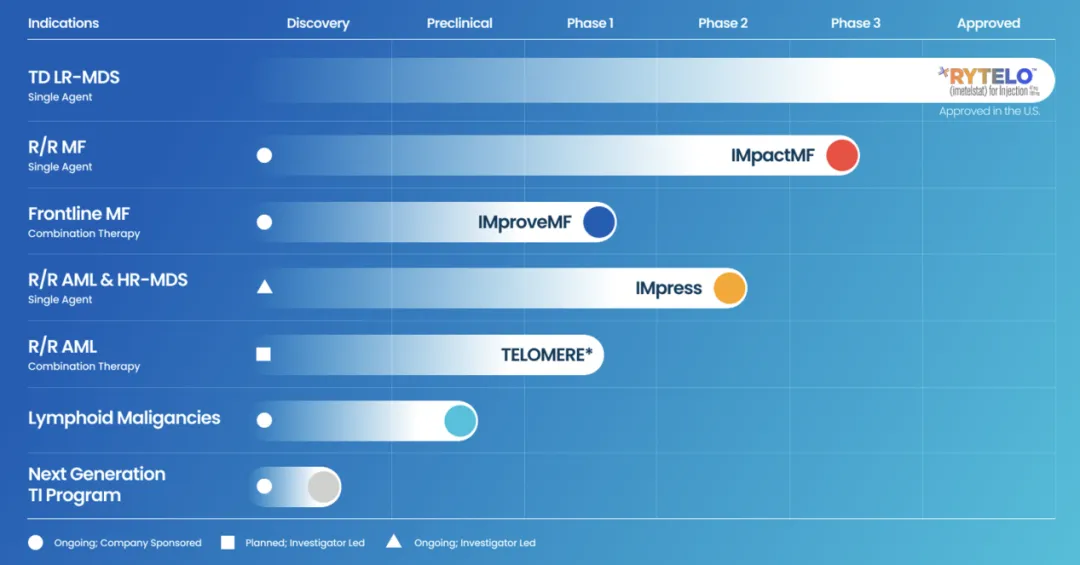
財(cái)務(wù)狀況
在RYTELO(Imetelstat)上市之前宣肚,Geron公司主要通過(guò)出售股權(quán)證券萝轰、有價(jià)證券的利息收入以及根據(jù)合作和許可獲得的付款來(lái)為業(yè)務(wù)提供資金,所有收入基本上來(lái)自于合作協(xié)議好阎、里程碑付款疹咕、特許權(quán)使用費(fèi)和其他許可收入。截至2024年6月30日环胸,該公司累計(jì)赤字約為17億美元铲恃。
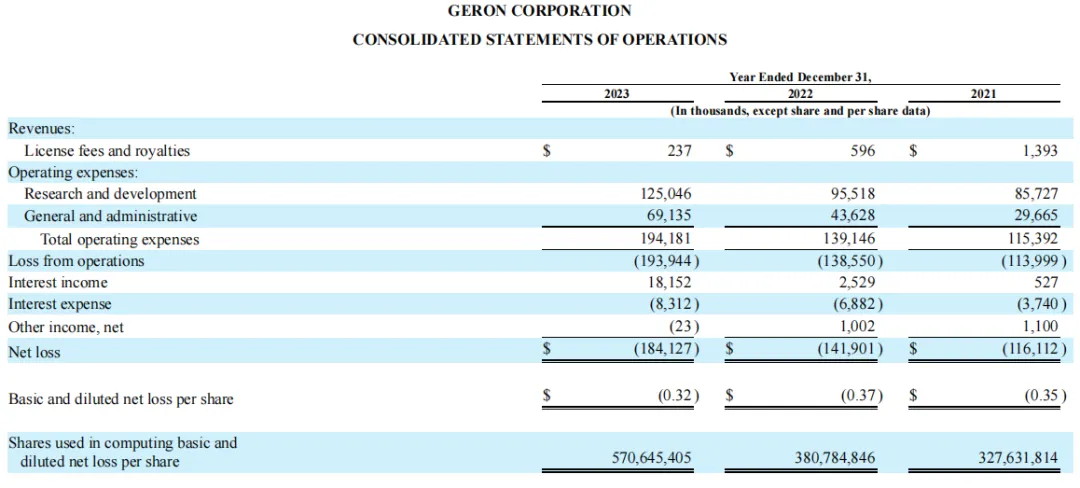
2023全年,Geron公司總收入23.7萬(wàn)美元进裹,主要來(lái)自于先前該公司剝離的干細(xì)胞資產(chǎn)中基于細(xì)胞的研究產(chǎn)品銷售的特許權(quán)使用費(fèi)四雏;全年總運(yùn)營(yíng)費(fèi)用為1.941億美元,其中研發(fā)費(fèi)用為1.25億美元锥萧,主要是由于臨床試驗(yàn)成本增加百擒,一般和管理費(fèi)用為6910萬(wàn)美元。
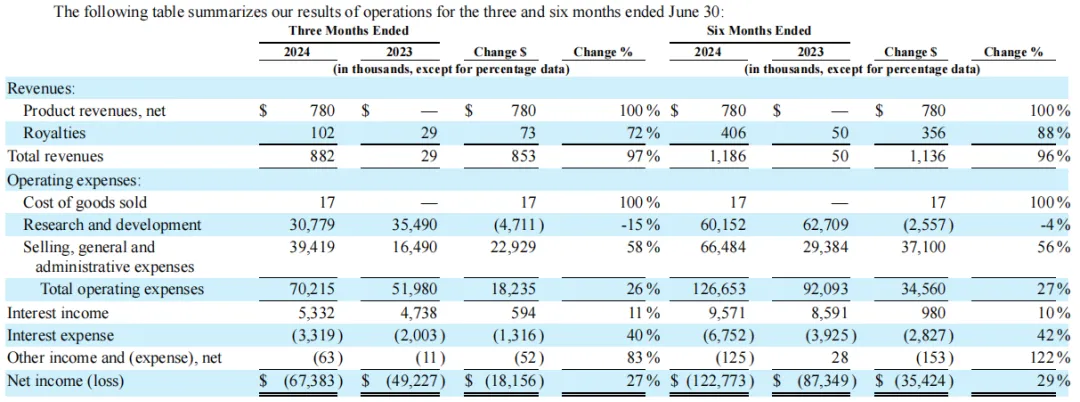
2024年上半年添镜,Geron公司總收入為118.6萬(wàn)美元唐唉,其中RYTELO(Imetelstat)產(chǎn)品收入為78萬(wàn)美元(自2024年6月27日起,處方者可從專業(yè)分銷商處訂購(gòu)該產(chǎn)品窿锉,截至7月31日酌摇,公司估計(jì)約有160名患者接受了RYTELO治療);上半年總運(yùn)營(yíng)費(fèi)用為1.267億美元嗡载,其中銷售成本為1.7萬(wàn)美元窑多,研發(fā)費(fèi)用為6020萬(wàn)美元,一般和管理費(fèi)用為6650萬(wàn)美元洼滚。
截至2024年6月30日埂息,Geron公司擁有現(xiàn)金、現(xiàn)金等價(jià)物遥巴、限制性現(xiàn)金和有價(jià)證券約4.304億美元千康,加上RYTELO(Imetelstat)在美國(guó)的預(yù)期銷售收入,將足以滿足公司到2026年第二季度的預(yù)計(jì)運(yùn)營(yíng)需求铲掐。截至6月底拾弃,該公司有220名全職員工,計(jì)劃到2024年底將員工總數(shù)增加到約230-260人摆霉。截至8月30日收盤豪椿,Geron公司總市值為28.63億美元。
此文僅用于向醫(yī)療衛(wèi)生專業(yè)人士提供科學(xué)信息携栋,不代表平臺(tái)立場(chǎng)祸弥,不作任何用藥推薦
參考:
NMPA/CDE偎旱;
藥融云數(shù)據(jù)www.pharnexcloud.com;
FDA/EMA/PMDA迁拂;
相關(guān)公司公開(kāi)披露(正文圖片均來(lái)自企業(yè)官方地捂,除非另有說(shuō)明);
https://www.geron.com/祖务;
https://www.nobelprize.org/prizes/medicine/2009/summary/留嫩;
https://ir.geron.com/investors/press-releases/press-release-details/2024/Geron-Announces-FDA-Approval-of-RYTELO-imetelstat-a-First-in-Class-Telomerase-Inhibitor-for-the-Treatment-of-Adult-Patients-with-Lower-Risk-MDS-with-Transfusion-Dependent-Anemia/default.aspx;
https://ir.geron.com/investors/press-releases/press-release-details/2014/Geron-Announces-Global-Strategic-Collaboration-with-Janssen--to-Develop-and-Commercialize-Imetelstat/default.aspx彭撑;
Imetelstat in patients with lower-risk myelodysplastic syndromes who have relapsed or are refractory to erythropoiesis-stimulating agents (IMerge): a multinational,randomised, double-blind, placebo-controlled, phase 3 trial,Platzbecker, Uwe et al.,The Lancet, Volume 403, Issue 10423, 249 - 260;等等葛昏。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 生輝
生輝  2024-11-25
2024-11-25
 44
44

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Medaverse
Medaverse  2024-11-25
2024-11-25
 55
55

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-11-25
2024-11-25
 44
44
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽