
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-09-25
2024-09-25
 218
218
今日(9月24日),中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心(CDE)官網(wǎng)剛剛公示贴祷,諾華(Novartis)镥[177Lu] 特昔維匹肽注射液擬納入優(yōu)先審評(píng)脸婉,適用于治療前列腺特異性膜抗原(PSMA)陽(yáng)性轉(zhuǎn)移性去勢(shì)抵抗性前列腺癌(mCRPC) 誓拉、已接受雄激素受體通路抑制和紫杉類化療的成年患者。公開(kāi)資料顯示尝赵,這是諾華研發(fā)的PSMA靶向放射性配體療法Pluvicto(lutetium 177Lu vipivotide tetraxetan篓羊,曾用名177Lu-PSMA-617),此前已于2022年3月獲美國(guó)FDA批準(zhǔn)治療上述前列腺癌患者弓呵。
同時(shí)六赢,諾華申報(bào)的放射性藥物鎵[68GGa]戈澤肽注射液配制用藥盒也被擬納入優(yōu)先審評(píng),該產(chǎn)品經(jīng)鎵-68放射性標(biāo)記后可作為放射性診斷試劑使用溃蛙,適用于通過(guò)正電子發(fā)射斷層掃描(PET)在前列腺癌成年患者中識(shí)別PSMA陽(yáng)性病灶灌旧。
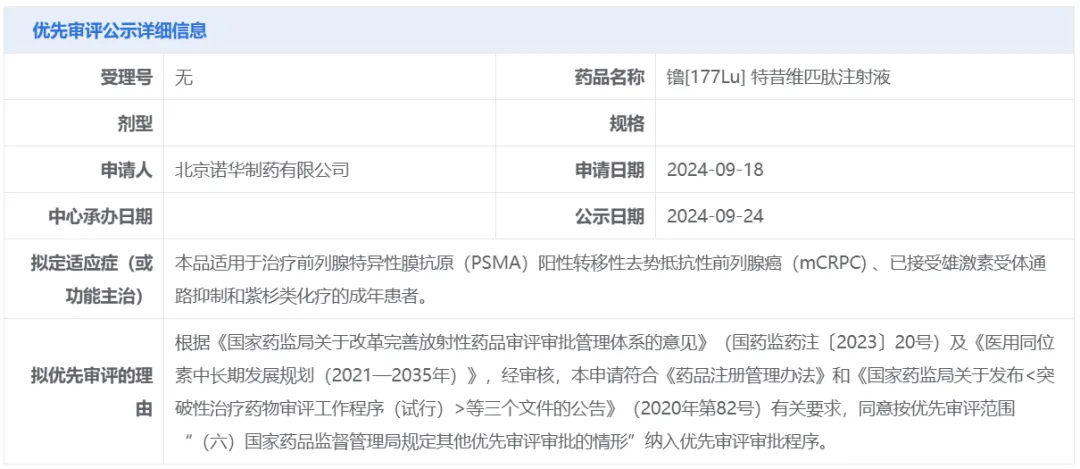
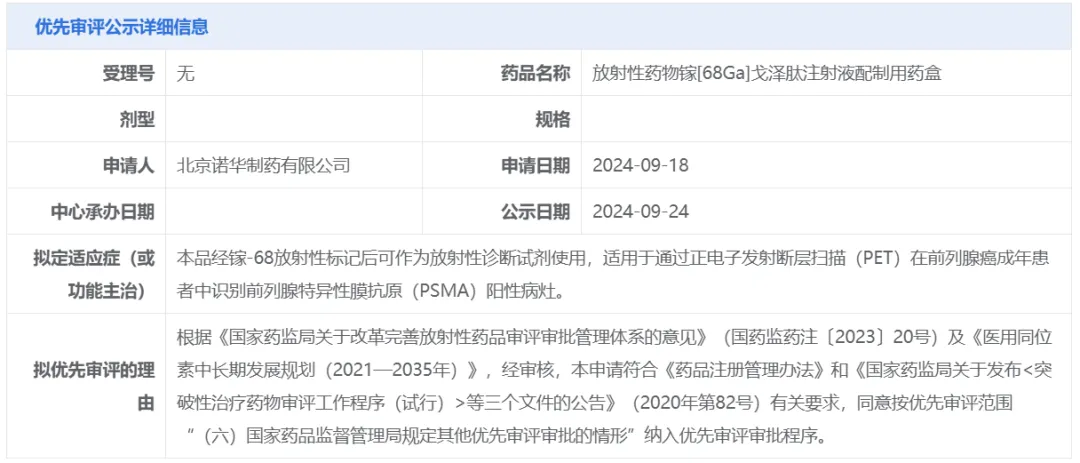
截圖來(lái)源:CDE官網(wǎng)
放射性藥物可以利用同一配體分別開(kāi)發(fā)針對(duì)特定靶點(diǎn)的診斷和治療產(chǎn)品,具有獨(dú)特的“診療一體化”優(yōu)勢(shì)绰筛,因此近年來(lái)備受行業(yè)看好枢泰。根據(jù)此前發(fā)表在Nature Reviews Clinical Oncology上的一篇綜述介紹描融,諾華開(kāi)發(fā)的靶向PSMA的放射性藥物Pluvicto獲批是該領(lǐng)域的重要進(jìn)展,這標(biāo)志著放射性藥物開(kāi)始用于治療前列腺癌這類更為常見(jiàn)的惡性腫瘤衡蚂。
Pluvicto是一款將靶向PSMA的小分子化合物與放射性同位素(177Lu)連接在一起的放射性配體療法窿克。它可與表達(dá)PSMA的前列腺癌細(xì)胞結(jié)合,放射性同位素釋放的輻射能量會(huì)損害腫瘤細(xì)胞毛甲,引發(fā)細(xì)胞死亡年叮。由于Pluvicto釋放的輻射只能在很短距離里起作用,因此限制了藥物對(duì)周圍健康細(xì)胞的損害玻募。
值得一提的是只损,Pluvicto還入選了日前剛剛出爐的2024年度蓋倫獎(jiǎng)(Prix Galien USA Awards)最佳藥品獎(jiǎng)的候選名單。
2022年3月七咧,諾華宣布FDA已經(jīng)批準(zhǔn)該公司的Pluvicto上市跃惫,用于治療PSMA陽(yáng)性轉(zhuǎn)移性去勢(shì)抵抗性前列腺癌(mCRPC)患者。他們已經(jīng)接受過(guò)基于紫杉烷的化療和雄激素受體信號(hào)通路抑制劑治療顿储。新聞稿指出溺联,Pluvicto是首款FDA批準(zhǔn)用于治療這類mCRPC患者的靶向放射配體療法。
FDA這一批準(zhǔn)是基于一項(xiàng)關(guān)鍵性3期臨床試驗(yàn)VISION研究的積極結(jié)果遮店。試驗(yàn)結(jié)果顯示捻境,與標(biāo)準(zhǔn)治療相比,添加Pluvicto將患者的死亡風(fēng)險(xiǎn)降低38%戳酒,Pluvicto同時(shí)顯著降低患者出現(xiàn)放射學(xué)疾病進(jìn)展或死亡的風(fēng)險(xiǎn)炸鹅。而且,在基線攜帶可評(píng)估疾病的患者中伟杂,Pluvicto組的總緩解率為30%伍愕,標(biāo)準(zhǔn)治療對(duì)照組這一數(shù)值為2%。
此外户犯,在2023年歐洲腫瘤內(nèi)科學(xué)會(huì)(ESMO)大會(huì)上蓉庆,諾華還宣布Pluvicto的3期PSMAfore臨床研究達(dá)到了影像學(xué)無(wú)進(jìn)展生存(rPFS)這一主要終點(diǎn)。與換用另一個(gè)雄激素受體通路抑制劑(ARPI)相比糜透,經(jīng)Pluvicto治療的患者降低59%的影像學(xué)進(jìn)展風(fēng)險(xiǎn)撤宽。數(shù)據(jù)截止日期延長(zhǎng)至中位8.6個(gè)月的研究隨訪時(shí)間后,更新的rPFS結(jié)果分析證實(shí)了該產(chǎn)品穩(wěn)定的臨床獲益粤咪,相比換用另一個(gè)ARPI谚中,該產(chǎn)品延長(zhǎng)了影像學(xué)無(wú)進(jìn)展生存期超過(guò)兩倍以上(rPFS,中位時(shí)間:12.0個(gè)月 vs 5.6個(gè)月)寥枝。

根據(jù)中國(guó)藥物臨床試驗(yàn)登記與信息公示平臺(tái)官網(wǎng)宪塔,諾華在中國(guó)開(kāi)展了PSMAddition 3期臨床研究,該研究旨在轉(zhuǎn)移性激素敏感性前列腺癌(mHSPC)成年男性患者中比較177Lu-PSMA-617聯(lián)合標(biāo)準(zhǔn)治療與單獨(dú)標(biāo)準(zhǔn)治療的療效和安全性。這也正是該產(chǎn)品在中國(guó)擬納入優(yōu)先審評(píng)的適應(yīng)癥某筐。
本次這款放射性療法在中國(guó)擬納入優(yōu)先審評(píng)比搭,意味著該產(chǎn)品有望加速來(lái)到患者身邊。
參考資料:
[1]中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心官網(wǎng).Retrieved Sep 24 , 2024, from https://www.cde.org.cn/main/xxgk/listpage/da6efd086c099b7fc949121166f0130c
[2]諾華放射配體療法全球III期PSMAfore研究達(dá)到主要終點(diǎn)南誊,在未經(jīng)化療的mCRPC患者中展現(xiàn)出超過(guò)兩倍的影像學(xué)無(wú)進(jìn)展生存獲益. Retrieved Oct 24, 2023. From https://mp.weixin.qq.com/s/y19oWFASbzO2Vv2di2Qr0Q

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 生輝
生輝  2024-11-25
2024-11-25
 39
39

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Medaverse
Medaverse  2024-11-25
2024-11-25
 49
49

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-11-25
2024-11-25
 39
39
 熱門資訊
熱門資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽